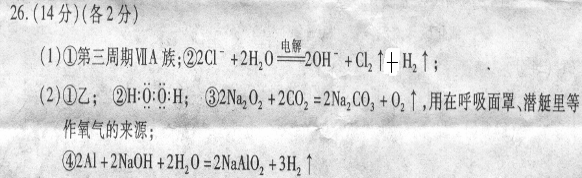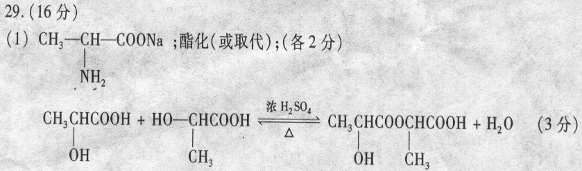高三化学招生适应性考试试卷
理科综合能力测试(化学部分)
相对原子质量:H. 1 Al . 27 Cl. 35.5 C. 12 O. 16 Fe. 56 Ag. 108
6、根据你的经验,下列说法错误的是( )
A,加碘食盐不是加有I2的食盐 B,纯碱不是纯净的烧碱
C,干冰不是水形成的冰 D,碘酒不是含有I2的酒精溶液
7、下列各组离子,在强碱溶液中可以大量共存的是( )
A,Na+.AlO2―.Cl―.CO32- B,NH4+.Na+. K+. Ba2+
C,Br-.NO3-.Cu2+.Ba2+ D,Na+. NO3-. SO42-. HCO3-
8、中学化学实验中,有关仪器的下端必须插入液面以下的是( )
①制备乙烯时用的温度计②制备氯气装置中分液漏斗的下端③吸收HCl气体时将HCl气体溶于水的导管④简易装置制H2用于加稀硫酸的长颈漏斗的下端⑤分馏石油时用的温度计⑥制取乙酸乙酯时,将蒸汽导入盛有饱和碳酸钠溶液试管中的导管
A,①②④ B,①②③⑥ C,①④ D,①③④⑤⑥
9、下列叙述中正确的是( )
A,组成元素全部是非金属元素的离子一定阴离子
B,在氧化还原反应中,非金属单质一定是氧化剂
C,某原诉有化合态变成游离态,该元素一定被氧化
D,金属单质在氧化还原反应中,该元素一定被氧化
10、在一恒容密闭容器中,某一反应物,生成物都为气体, C两种物质的百分含量(A%. C%)随温度的变化
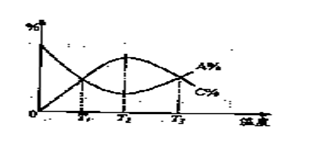
曲线如右图所示。下列说法正确的是( )
A,该可逆反应中C是反应物,A是生成物。
B,该可逆反应在温度T1.T3时正 逆反应速率相等
C,该可逆反应在温度T2时达到化学平衡。
D,该可逆反应的正反应是吸热反应。
11、在相同的温度和压强下,4个容器分别装有4种气体。已知容器中的气体和容积分别是:①Cl2. 100ml ②O2.200ml ③CO. 300ml ④CH4. 600ml。则四个容器中气体的质量由大到小的顺序是( )
A, ①>②>③>④ B, ②>①>④>③
C,③>④>②>① D,④>③>①>②
12、常温下,有pH相同的四种一元酸 HA. HB. HC . HD各20ml,分别与足量的镁粉反应在相同状况下产生H2的体积大小顺序是:HD>HC>HA=HB,则下列叙述正确的是( )
A,HA. HB可能都是强酸 B,HD可能是强酸
C,等物质的量浓度的NaC溶液和NaD溶液的pH,NaD的大。
D,四种酸分别与镁粉反应,开始时的速率相等。
13、某同学对离子方程式:xR2++yH++O2 == mR3++nH2O作出的下列结论,正确的是( )
A,根据电荷守恒:x+y = m B,根据电子得失守恒:x=2
C,根据原子守恒:x=m D,根据质量守恒:x+y+1=n+m
26、(14分)X.Y.Z是三种短周期元素,且原子序数依次增大。
(1) 若三种元素的原子半径大小顺序为X< Z< Y,且Y能与Z能形成原子个数为
1: 1的离子化合物,A,X与Z能形成原子个数比为1:1的共价化合物B,电解A的水溶液(以石墨做电极)生成化合物C和X. Z的气体单质。
则①元素Z在周期表中的位置 。
②电解A的水溶液反应的离子方程式 。
(2)若三种元素的原子半径为X<Y<Z,且Y与Z能形成原子个数比为1:1的离子化合物D,X与Y能形成原子个数比为1:1的共价化合物E,D与水反应生成气体单质和(1)中的化合物C。
则①X.Y.Z 三种元素在同一周期
甲,可能 乙,不可能 丙,无法判断
②化合物E的电子式 。
③D与二氧化碳反应的化学方程式 ,此反应的用途
是 。
④与Z同周期的某元素单质既能与C溶液反应又能与(1)中的B溶液反应,且都能生成同一气体单质,写出该单质与C溶液反应的化学方程式 。
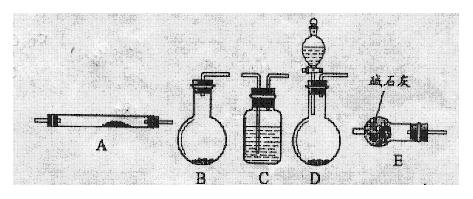
27、(14分)实验室若要制取氮气,有多种方法,通常可将氨气通入灼热的氧化铜粉末,得到氮气和铜。实验时可供选择的实验装置如下图所示(收集装置. 夹持仪器. 石棉网及酒精灯等未列出)。
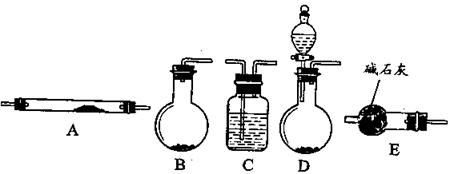
(1)写出氨气与氧化铜反应的化学方程式 。
(2)若实验中的氨气是用氨水与生石灰反应得到,最好选用 (填装置序号)作发
生器,反应的化学方程式 。要制得纯净的氮气,应使
用上述装置中 (填装置序号,并按气流方向从左到右的顺
序列出)。装置C中应当装入的试剂是 。
(3)若用此方法制氨气的过程中,发现氨气产生很缓慢,就此猜测可能的两个原因
是 。
28、(16分)将中学化学中三种常见的金属阳离子的硝酸盐溶于水得到溶液A。用A溶液进行如下实验:
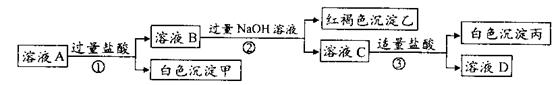
回答下列问题;
(1)根据实验现象,就可以判断三种硝酸盐中一定有的两种阳离子是 , 。
(2)根据实验现象, (“能”或“不能”)确定三种硝酸盐中的第三金属
阳离子,理由是 。
(3)若实验中未发生氧化还原反应,请写出②中反应的离子方程式
,若沉淀甲. 乙. 丙的质量分别
为14.35g,10.7g,7.8g,反应①加入200ml的1mol・L-1的稀盐酸,反应②加入500ml的2moL・L-1的烧碱溶液,则使丙的沉淀的质量达到最大值7.8g,反应③中加入1moL・L-1的盐酸的体积为 ml。
29、 (16分)已知a-氨基酸在一定的条件下能与亚硝酸HNO2反应得到a-羟基酸:
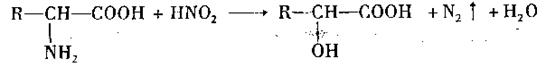
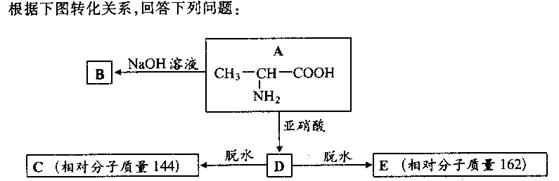
(1)物质B的结构简式 。指出D→C的反应类型 ;
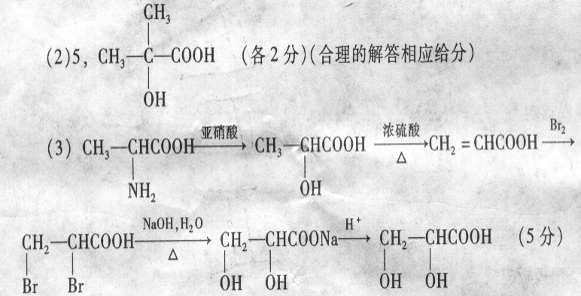
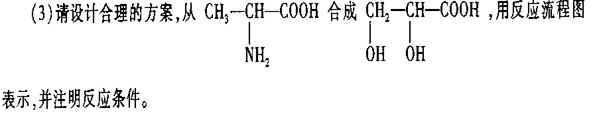
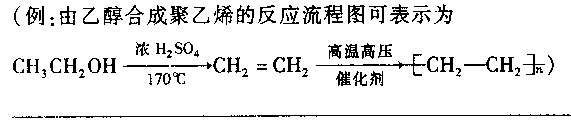
(2)F是分子中碳原子数比D分子碳原子数多1且与D含有相同的官能团的有机物,符合条件的F的同分异构体共有中 种,请写出其中任意一种的结构简式 。
参考答案:
| 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| D | A | C | D | C | D | B | C |