08届高三理科综合考试试题
命题人:李玉义 马勇 俞学良
本卷分第Ⅰ卷和Ⅱ卷两部分。满分240分。考试时间150分钟
第Ⅰ卷(必做 共88分)
一、选择题(本题包括15小题。每小题4分,共60分 。每小题共有一个选项符合题意)
1.在下列生理过程中,细胞内自由水与结合水比值增加的是( )
A. 细胞衰老 B.作物越冬 C.种子萌发 D.细胞质壁分离
2.下列有关细胞器的叙述,不正确的是( )
A. 中心体与动物细胞有丝分裂过程中纺锤体的形成有关
B.唾液腺细胞中有较多的内质网和高尔基体
C.洋葱根尖分生区细胞没有大液泡,不能进行水的吸收
D.肝脏细胞中,核糖体和中心体没有膜结构
3.引起生物可遗传变异的原因有3种,即基因重组、基因突变和染色体变异。以下几种生物性状的产生,来源于同一种变异类型的是( )
①青霉素高产菌株 ②豌豆的黄色皱粒、绿色圆粒 ③八倍体小黑麦 ④人类的色盲 ⑤侏儒症 ⑥果蝇的白眼
A. ①②③ B.④⑤⑥ C.①④⑥ D.②③⑤
 4.右图表示绿色植物体内某些代谢过程中物质的变化,a、b、c分别表示不同的代谢过程。以下表述正确的是( )
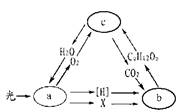
4.右图表示绿色植物体内某些代谢过程中物质的变化,a、b、c分别表示不同的代谢过程。以下表述正确的是( )
A. 水参与c中第二阶段的反应
B.b在叶绿体囊状结构上进行
C.a中产生的O2,参与c的第二阶段
D.X代表的物质从叶绿体的基质移向叶绿体的囊状结构
5.某患儿胸腺先天性缺失,与正常儿童相比,该患儿( )
A.仍有部分细胞免疫功能
B.仍有部分体液免疫功能
C.体内的B淋巴细胞数目显著减少
D.体内的T淋巴细胞数目增加
 6.肺炎双球菌转化实验中,将加热杀死的S型细菌与R型活细菌混合后,注射到小鼠体内,小鼠体内S型和R型细菌含量变化如右图所示。下列有关叙述错误的是( )
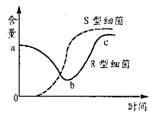
6.肺炎双球菌转化实验中,将加热杀死的S型细菌与R型活细菌混合后,注射到小鼠体内,小鼠体内S型和R型细菌含量变化如右图所示。下列有关叙述错误的是( )
A.小鼠死亡后,体内存在着S型和R型两种细菌
B.曲线ab段下降是因为R型细菌被小鼠免疫系统消灭
C. 曲线bc段上升,与S型细菌在小鼠体内增殖导致小鼠免疫力降低有关
D.S型细菌的出现是由于R型细菌突变的结果
 7.右图为反射弧结构,若刺激a可引起b处产生冲动,效应器做出反应,而刺激b也可以引起效应器做出反应,但不能引起a处产生冲动。以下说法正确的是
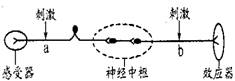
7.右图为反射弧结构,若刺激a可引起b处产生冲动,效应器做出反应,而刺激b也可以引起效应器做出反应,但不能引起a处产生冲动。以下说法正确的是
A. 兴奋在感觉神经元上传导是单向的
B.在神经中枢内突触传递兴奋的方向是单向的
C.兴奋在运动神经元上传导是单向的
D.刺激a使突触传递兴奋,刺激b使突触传递抑制
8.下表中A-F表示六类不同地带的生态系统,据表分析可知
| A | B | C | D | E | F | |
| 年枯叶输入量(t・hm―2) | 1.50 | 70.50 | 11.50 | 7.5 | 9.5 | 50.0 |
| 枯叶现存量(t・hm―2) | 44.00 | 35.00 | 15.00 | 5.0 | 3.0 | 5.0 |
A. 土壤有机物积累量A<B<C<D<E<F
B.F最可能是热带雨林生态系统
C.枯叶分解速率与环境温度和湿度都没有关系
D.分解者作用的强弱依次是A>B>C>D>E>F
9.目前,人类已经发现的非金属元素除稀有气体元素外有16种,下列对这16种非金属元素的判断不正确的是 ( )
①都是主族元素,原子的最外层电子数都大于3 ②单质在反应中都只能作氧化剂
③对应的含氧酸都是强酸 ④氢化物常温下都是气态,所以又叫气态氢化物
⑤气态氧化物与水反应都不会再生成气体
A.全部 B.只有①② C.只有①②③④ D.只有①②④⑤
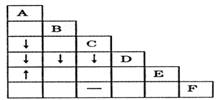 10.有A、B、C、D、E、F六瓶不同物质的溶液, 它们分别是NH3・H2O、Na2CO3、MgSO4、NaHCO3、HNO3和BaCl2溶液中的一种。为了鉴别它们,各取少量溶液进行两两混合,实验结果如表所示,表中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示观察不到明显现象,空格表示实验未做。试推断其中F是( )
10.有A、B、C、D、E、F六瓶不同物质的溶液, 它们分别是NH3・H2O、Na2CO3、MgSO4、NaHCO3、HNO3和BaCl2溶液中的一种。为了鉴别它们,各取少量溶液进行两两混合,实验结果如表所示,表中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示观察不到明显现象,空格表示实验未做。试推断其中F是( )
A.NaHCO3溶液 B.BaCl2溶液
C.MgSO4溶液 D.Na2CO3溶液
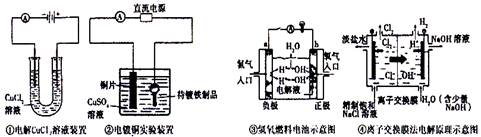
11关于下列电化学装置图的说法,正确的是( )
|
A.①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B.②装置中待镀铁制品应与电源正极相连 C.③装置中电子由b极流向 a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
12.某酸的酸式盐NaHY的水溶液显碱性,下列有关叙述正确是 ( )
![]() A.H2Y在电离时为:H2Y 2H+ +
Y2-
A.H2Y在电离时为:H2Y 2H+ +
Y2-
B.在该盐的溶液里,离子浓度为:c(Na+) > c(Y2-)> c(HY-) > c(OH-) > c(H+)
C.在该盐的溶液里,离子浓度为:c(Na+) > c(HY-)>c(H+) > c(Y2-)
![]() D.HY-水解的化学方程式为:HY- + H2O H3O+
+Y2-
D.HY-水解的化学方程式为:HY- + H2O H3O+
+Y2-
13.下列各组离子,在指定环境中一定能大量共存的是 ( )
A.能使pH试纸变深蓝色的溶液中:S2-、SO2-3、SO2-4
B.加入铝粉能放出氢气的溶液中:CO2-3、AlO-2、I-、NO-3
C.pH=7的溶液中:Al3+、K+、SO2-4、HCO-3
D.由水电离出的[OH-] = 10-13mol・L-1的溶液中:Fe3+、NH+4、ClO-、Cl-
![]() 14.已知以应mX(g)
+nY(g)
qZ(g)的△H <0,m+n>q,在恒容器闭容器中反应达到平衡时,下列说法正确的是( )
14.已知以应mX(g)
+nY(g)
qZ(g)的△H <0,m+n>q,在恒容器闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀气有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速度的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时,X、Y的转化率相等,说明反应开始时,X、Y的物质的量之比为n:m
15.下列说法中正确的是( )
(A)石油裂解可以得到氯乙烯
(B)油脂水解可得到氨基酸和甘油
(C)所有烷烃和蛋白质中都存在碳碳单键
(D)淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖
二、选择题(本题包含7小题,每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得4分,选对但不全的得2分,有选错的得0分)
16、许多科学家在物理学发展过程中做出了重要贡献,下列表述正确的是( )
A.卡文迪许测出引力常数
B.法拉第发现电磁感应现象
C.安培提出了磁场对运动电荷的作用力公式
D.库仑总结并确认了真空中两个静止点电荷之间的相互作用规律
17、据报道,最近在太阳系外发现了首颗“宜居”行星,其质量约为地球质量的6.4倍,一个在地球表面重量为600 N的人在这个行星表面的重量将变为960 N,由此可推知该行星的半径与地球半径之比约为( )
A.0.5 B.2.
C.3.2 D.4
 18、a、b、c、d是匀强电场中的四个点,它们正好是一个矩形的四个顶点.电场线与矩形所在平面平行。已知a点的电势为20 V,b点的电势为24 V,d点的电势为4 V,如图,由此可知c点的电势为 ( )
18、a、b、c、d是匀强电场中的四个点,它们正好是一个矩形的四个顶点.电场线与矩形所在平面平行。已知a点的电势为20 V,b点的电势为24 V,d点的电势为4 V,如图,由此可知c点的电势为 ( )
A.4 V B.8 V
 C.12 V D.24 V
C.12 V D.24 V
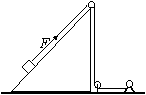
19如图,卷扬机的绳索通过定滑轮用力F 拉位于粗糙斜面上的木箱,使之沿斜面加速向上 移动。在移动过程中,下列说法正确的是( )
A.F对木箱做的功等于木箱增加的动能与木箱克服摩擦力所做的功之和
B.F对木箱做的功等于木箱克服摩擦力和克服重力所做的功之和
C.木箱克服重力做的功等于木箱增加的重力势能
DF对木箱做的功等于木箱增加的机械能与木箱克服摩擦力做的功之 和
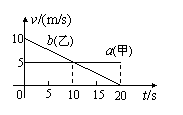 20、甲乙两辆汽车在平直的公路上沿同一方向作直线运动,t=0时刻同时经过公路旁的同一个路标。在描述两车运动的v-t图中(如图),直线a、b分别描述了甲乙两车在0-20 s的运动情况。关于两车之间的位置关系,下列说法正确的是( )
20、甲乙两辆汽车在平直的公路上沿同一方向作直线运动,t=0时刻同时经过公路旁的同一个路标。在描述两车运动的v-t图中(如图),直线a、b分别描述了甲乙两车在0-20 s的运动情况。关于两车之间的位置关系,下列说法正确的是( )
A.在0-10 s内两车逐渐靠近
B.在10-20 s内两车逐渐远离
C.在5-15 s内两车的位移相等
D.在t=10 s时两车在公路上相遇
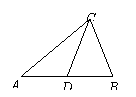 21、匀强电场中的三点A、B、C是一个三角形的三个顶点,AB的长度为1 m,D为AB的中点,如图所示。已知电场线的方向平行于ΔABC所在平面,A、B、C三点的电势分别为14 V、6 V和2 V。设场强大小为E,一电量为1×10-6 C的正电荷从D点移到C点电场力所做的功为W,则 (
)
21、匀强电场中的三点A、B、C是一个三角形的三个顶点,AB的长度为1 m,D为AB的中点,如图所示。已知电场线的方向平行于ΔABC所在平面,A、B、C三点的电势分别为14 V、6 V和2 V。设场强大小为E,一电量为1×10-6 C的正电荷从D点移到C点电场力所做的功为W,则 (
)
A.W=8×10-6 J,E>8 V/m
B.W=6×10-6 J,E>6 V/m
C.W=8×10-6 J,E≤8 V/m
|
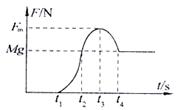
22、利用传感器和计算机可以研究快速变化的力的大小,
实验时让某消防队员从一平台上跌落,自由下落2m
后双脚触地,接着他用双腿弯曲的方法缓冲,使自身
重心又下降了0.5m,最后停止,用这种方法获得消防
队员受到地面冲击力随时间变化图线如图所示,根据图
线所提供的信息以下判断正确的是 ( )
A.t1时刻消防员的速度最大 B.t2时刻消防员的速度最大
C.t3时刻消防员的动能最小 D.t4时刻消防员的动能最小
第Ⅱ卷
(必做120分+选做32分,共152分)
【必做部分】
23.(1)(3分)用如图8所示的器材,研究钨丝灯泡消耗的功率P与通过它的电流I之间的关系。已知灯泡的规格为“12V、5W”,电源的电动势为15V,内阻忽略,滑动变阻器的规格为“20Ω、12A”。功率的测量需要用到电流表、电压表。请将图中的器材连成实验电路。要求实验中灯泡两端的电压变化范围为0―12V。
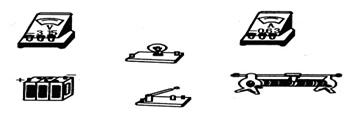
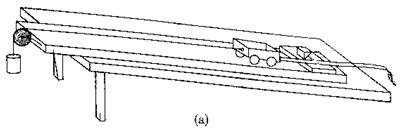
(2)(8分)如图11(a)所示,小车放在斜面上,车前端栓有不可伸长的细线,跨过固定在斜面边缘的小滑轮与重物相连,小车后面与打点计时器的纸带相连。起初小车停在靠近打点计时器的位置,重物到地面的距离小于小车到滑轮的的距离。启动打点计时器,释放重物,小车在重物的牵引下,由静止开始沿斜面向上运动,重物落地后,小车会继续向上运动一段距离。打点计时器使用的交流电频率为50 Hz。图11(b)中a、b、c是小车运动纸带上的三段,纸带运动方向如箭头所示。
|
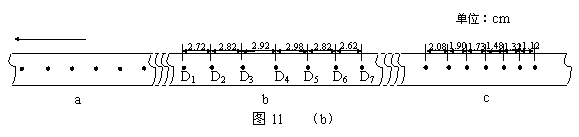
①根据所提供纸带上的数据,计算打c段纸带时小车的加速度大小为_________m/s2。(结果保留两位有效数字)
②打a段纸带时,小车的加速度是2.5 m/s2。请根据加速度的情况,判断小车运动的最大速度可能出现在b段纸带中的_________。
③如果取重力加速度10 m/s2,由纸带数据可推算出重物与小车的质量比为_________。
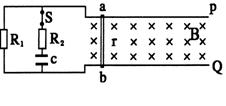 24.(16分)如图所示,P、Q为两根相距为L且互相平行的长直光滑的金属导轨,其左端与电容为C的电容器和阻值分别为R1、R2的电阻连成图示电路,质量为m的金属棒ab与导轨垂直放置,且接触良好,其电阻为r(导轨电阻不计),整个装置放在磁感应强度为B、方向垂直导轨平面向里的匀强磁场中。现闭合开关S,用大小为F的水平力拉棒ab,使它水平向右运动。求:
24.(16分)如图所示,P、Q为两根相距为L且互相平行的长直光滑的金属导轨,其左端与电容为C的电容器和阻值分别为R1、R2的电阻连成图示电路,质量为m的金属棒ab与导轨垂直放置,且接触良好,其电阻为r(导轨电阻不计),整个装置放在磁感应强度为B、方向垂直导轨平面向里的匀强磁场中。现闭合开关S,用大小为F的水平力拉棒ab,使它水平向右运动。求:
(1)棒ab的最大速度;
(2)棒ab达最大速度时电容器的带电量;
(3)在棒ab达最大速度后,断开开关S、并同
时撤去水平拉力F,此后电阻R1产生的热量多大?
|
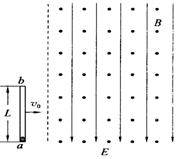
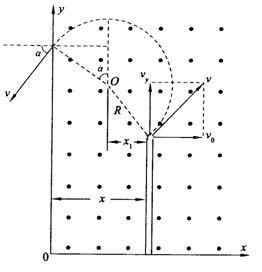
(1)小球从玻璃管b端滑出时速度的大小。
(2)从玻璃管进入磁场至小球从b端滑出的过程中,
外力F随时间t变化的关系。
(3)通过计算画出小球离开玻璃管后的运动轨迹。
26. (14分)在某一片小麦田中,长有许多杂草,还有食草昆虫、青蛙、蛇等动物活动。某研究小组对该农田生态系统进行研究,根据所学知识回答相关问题:
(1)研究小组要估算该农田中荠菜的种群密度,应采用 法;在取样时,关键要做到 。
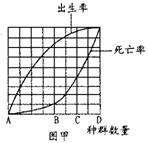
(2)此农田中新迁入了一种食草昆虫,下图甲是与这种昆虫种群数量相关的出生率和死亡率的变化曲线。请说出种群在B点后死亡率明显增加的原因:
(答两点)。
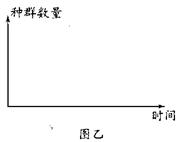
(3)请根据图甲在图乙坐标系中画出种群数量的变化曲线(将A、D标在纵坐标的合适位置上)。
(4)农田如果弃耕,农作物会被杂草取代,这一过程叫做 。
27.(19分)阅读资料结合图示回答有关问题:
乙酰胆碱酯酶能催化神经递质――乙酰胆碱的水解,使神经递质在完成神经兴奋的传递任务之后,尽快消失。有机磷杀虫剂能专门抑制动物乙酰胆碱酯酶的活性,使乙酰胆碱不能很快消失,肌肉细胞就会处于持续兴奋之中,表现为震颤不已,直到死亡。
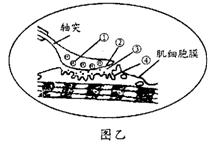
(1)图乙① 中的物质释放到③中的方式是 ,它将与突触后膜上的 结合,从而使突触后膜产生 (据图回答)
(2)由图乙看出,突触后膜的面积相对较大,其意义是 .
(3)请将下列实验步骤及结果补充完整。
实验目的:验证有机磷杀虫剂对乙酰胆碱酯酶的活性具有抑制作用。
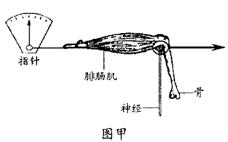
材料用具:两个相同的甲图装置、适宜的放电装置、有机磷杀虫剂、生理盐水、培养皿等。
实验步骤:
第一步:将两个装置编号1、2,并分别将装置中青蛙的“神经――腓肠肌”标本放人盛有等量生理盐水的两个培养皿中。
第二步:同时用电极分别刺激两个“神经――腓肠肌”标本的神经,指针都向左偏转,然后恢复。
第三步:
第四步:
实验结果:
28(14分)短周期中的六种元素A、B、C、X、Y、Z,原子序数依次减小,其中X、Y、Z
原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物;C与X处于同周期,B+与C2―的核外电子排布相同,A与B处于同周期,且形成BA型化合物。请回答:
(1)Y元素的名称是 ;
(2)XZ3的化合物的电子式是 ;
(3)A、B、C的离子半径由大到小的顺序为 (用元素离子符号表示)
(4)化合物XZ4A中所含的化学键类型为 ,该化合物水溶液可用于金属除锈,其原因是: (用离子方程式表示)
(5)元素组成的化合XZ5YC3和足量的化合物BCZ反应的离子方程式为
。
(6)在火箭推进器中装有液态N2H4和液态H2O2,已知0.4mol.液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量。试写出该反应的热化学方程式: 。
|
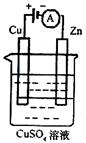
右图是一个电化学过程示意图。
1)锌片上发生的电极反应式为 。
2)假设使用肼一空气燃料电池作为本过程中的电
源,铜片的质量变化为128g,则肼一空气燃料
电池理论上消耗标准状况下的空气 L
(假设空所中氧气体积含量为20%)。
|
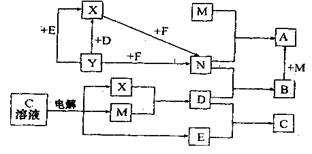
(1)向沸腾的蒸馏水中滴加A的饱和溶液,可以得到红褐色液体。A的化学式是
。
(2)将NaOH溶液注入新B溶液中,观察到的现象是 。(选填序号)。
①生成白色沉淀②生成血红色沉淀③生成红褐色沉淀④生成蓝色沉淀
⑤生成白色沉淀后,迅速变成灰绿色沉淀,最后变成红褐色沉淀
(3)C溶液电解的离子方程式是 。
(4)化合物F中含有组成单质N的元素,且该元素质量分数为70%。化合物F和单质Y反应的化学方程式是 。
(5)W(组成为单质N的元素和碳元素)合金易生锈。某学生在A、B、C、D四个小烧瓶中分别
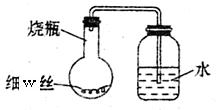 放入干燥的细W丝、浸过食盐水的细W丝、浸过清
放入干燥的细W丝、浸过食盐水的细W丝、浸过清
水的细W丝、食盐水及细W丝(并使W丝完全浸没
有食盐水中)。然后分别装配成如右图所示的装置,
每隔一段时间测量导管中水面上升的高度,结果如
下表所示(表中所列数据为导管中水面上升的高
度/cm),回答下列问题:
| 时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶(盛干燥W丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶(盛浸了食盐水的W丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶(盛浸了清水的W丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶(盛完全浸没在食盐水中的W丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
①为什么有的导管中的水面会上升? 。
②上述实验中,W生锈的速度由大到小的排列顺序为 (填小烧瓶的字母编号)。 。
③影响W生锈的因素除氧气外还有 。
④通过上面的研究,你认为在日常生活中应该如何保护W制品? 。
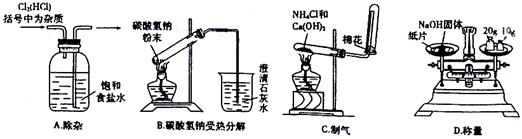
30.(14分)Ⅰ.化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。(1)下列关于实验的叙述正确的是 。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.在两支试管里分别加热NH4Cl和NH4HCO3,现象完全相同
C.在铝热反应的实验中,用滤纸做的漏斗必须干燥
D.用滴有酚酞的水做氨的喷泉实验,只验证了氨的溶解性
E.验证CO2中混有SO2时,可将混合气体通过品红溶液
(2)下列实验装置没有错误的一项是 。
|
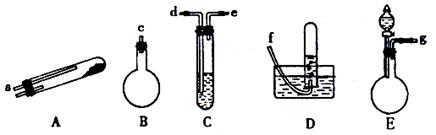
Ⅱ.实验室可以通过三条途径按不同要求来制取氮:
①加热条件下用NH3还原CuO制得纯净的N2和活性铜粉;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热NaNO2(一种致癌物质,有剧毒)与NH4Cl的混合浓溶液制取N2。
|
(1)按途径①制取N2时所需的氨气要用浓氨水与生石灰作原料制取,最好要用上述仪器中的 (填仪器代码,下同)作为氨气发生装置,该反应的化学方程式为 。要制取并收集纯净的N2(允许含少量的水蒸气),还应使用到上述仪器中的 (按气流从左到右的顺序列出)。
(2)按途径②制取N2,原料气空气是通过向 (填上述仪器代码)中加入 而送入反应器的,反应器内发生的现象是 。
(3)上述三种制取N2的途径,①和②两条途径常常被协同使用而越来越受到人们的关注,这种方法与途径③相比其优越性在于 。
【选做部分】
共8题,考生必须从中选择2个物理题,1个化学题和1个生物题作答。
31(8分)[化学与技术]
32(8分)[物质结构与性质]
33(8分)[有机化学基础]
肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中。工业上可通过下列反应制备:
![]() +CH3CHO
+CH3CHO![]()
![]() +H2O
+H2O
(1)请推测B侧链上可能发生反应的类型: 。(任填两种)
(2)请写出两分子乙醛在上述条件下反应的化学方程式:_______ 。
(3)请写出同时满足括号内条件下B的所有同分异构体的结构简式:(①分子中不含羰基和羟基;②是苯的对二取代物;③除苯环外,不含其他环状结构。)______________________。
34.(8分)(选修---生物技术实践)
35.(8分)(选修---现代生物科技专题)
已知SARS是由一种RNA病毒感染所引起的疾病。SARS病毒表面的S蛋白是主要的病毒抗原,在SARS病人康复后的血清中有抗S蛋白的特异性抗体。某研究小组为了研制预防SARS病毒的疫苗,开展了前期研究工作。其简要的操作流程如下:
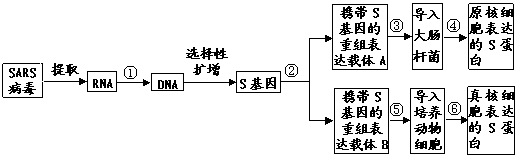 |
(1)实验步骤①所代表的反应过程是 。
(2)步骤②构建重组表达载体A和重组表达载体B必须使用限制性内切酶和 酶。
(3)如果省略步骤②而将大量扩增的S基因直接导入大肠杆菌,一般情况下,不能得到表达的S蛋白,其原因是S基因在大肠杆菌中不能 ,也不能 。
(4)为了检验步骤④所表达的S蛋白是否与病毒S蛋白有相同的免疫反应特性,可用 与 进行抗原―抗体特异性反应实验,从而得出结论。
(5)步骤④和⑥的结果相比,原核细胞表达的S蛋白与真核细胞表达的S蛋白的氨基酸序列 (相同,不同),根本原因是 。
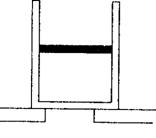 36. (8分)【物理――选修3-3】 如图所示,气缸放置在水平平台上,活塞质量为10 kg,横截面积50 cm2,厚度1 cm,气缸全长 21 cm,气缸质量20kg大气压强为l×105 Pa,当温度为7℃时,活塞封闭的气柱长10 cm,若将气缸倒过来放置时,活塞下方的空气能通过平台上的缺口与大气相通.g取10 m/s2求:
36. (8分)【物理――选修3-3】 如图所示,气缸放置在水平平台上,活塞质量为10 kg,横截面积50 cm2,厚度1 cm,气缸全长 21 cm,气缸质量20kg大气压强为l×105 Pa,当温度为7℃时,活塞封闭的气柱长10 cm,若将气缸倒过来放置时,活塞下方的空气能通过平台上的缺口与大气相通.g取10 m/s2求:
(1)气柱多长?
(2)当温度多高时,活塞刚好接触平台?
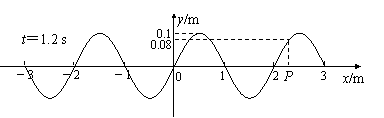
37.(8分)【物理――选修3-4】图为沿x轴向右传播的简谐横波在t=1.2 s时的波形,位于坐标原点处的观察者测到在4 s内有10个完整的波经过该点。
⑴求该波的波幅、频率、周期和波速。
⑵画出平衡位置在x轴上P点处的质点在0-0.6 s内的振动图象。
 |
2008年滕州市第一中学高三理科综合考试试题答案
1C2.C3.C4.A5.B6.D7.B8.B9.A
|
|
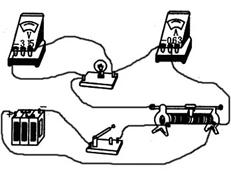 23 (1) (3分)分压电路,选0-0.6A和0-15V量程,内外接法均可。线路有一处错误均的零分。
23 (1) (3分)分压电路,选0-0.6A和0-15V量程,内外接法均可。线路有一处错误均的零分。
(2)①5.0 m/s2(结果是4.8 m/s2的得1分)(2分)
②D4D5区间内(3分)
③1:1 (3分)
24(16分)、解:(1)棒ab在外力F作用下向右运时产生感应电流,从而使棒ab产生向左的安培力作用,当![]() 时棒ab有最大速度
时棒ab有最大速度![]()
由题设条件有![]() (1’)
(1’)
此时棒ab产生的感应电动势为![]() (1’)
(1’)
回路中的总电流为 ![]() (2’)
(2’)
联立上述三式解得 ![]() (2’)
(2’)
(2)设电容器带电量为Q,棒ab达到最大速度时有
![]() (1’)
(1’)
而![]() (1’)
(1’)
联立上述两式![]() (2’)
(2’)
(3)当断开开关S后,电路由![]() 和
和![]() 串联组成,由能量转化与守恒定律有
串联组成,由能量转化与守恒定律有
回路产生的总热量为![]() (2’)
(2’)
![]() 上产生的热量为
上产生的热量为![]() (2’)
(2’)
联立以上二式解得![]() (2’)
(2’)
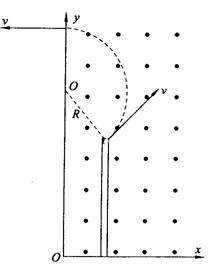
25.(18分)
(1)由![]() ,即重力与电场力平衡 …………………………… 1分
,即重力与电场力平衡 …………………………… 1分
|
![]() ……………………2分
……………………2分
设小球运动至b端时的y方向速度分量为vy,
则:![]() ……………………2分
……………………2分
所以小球运动至b端时速度大小为
![]() ………………1分
………………1分
(2)由平衡条件可知,玻璃管受到的水平外力为:
![]() ……………………2分
……………………2分
![]() …………………2分
…………………2分
解得外力随时间变化关系为:![]() …………………………………………1分
…………………………………………1分
(3)设小球在管中运动时间为t,小球在磁场中做圆周运动的半径为R,轨迹如图所示,
t时间内玻璃管的运动距离![]() ……………………………………………………1分
……………………………………………………1分
由牛顿第二定律得:![]() ……1分
……1分
|
![]()
所以![]() ……1分
……1分
可得![]() …………………………………1分
…………………………………1分
故![]() ,即小球飞离磁场时速度方向垂直于磁
,即小球飞离磁场时速度方向垂直于磁
场边界向左。
小球运动轨迹如图所示………………………2分
26.(14分)
(1)样方(2分) 随机取样(2分)
(2)生活资源和空间有限 天敌增多(其它合理答案亦可)(4分)
(3)要求:画成“S”型曲线(2分);纵坐标上A点对应起点(1分),D点对应
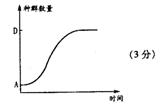 K值(1分)。
K值(1分)。
(4)群落的次生演替(2分)
27.(19分)
(1)突触小泡 (1分) 胞吐(或外排)(2分)特异性受体(2分)兴奋(2分)
(2)有利于接受递质(2分)
(3)第三步:在装置1的培养皿中滴加一定量的有机磷杀虫剂,在装置2的培养
皿中滴加等量的生理盐水。(4分)
第四步:一段时间后,同时用电极刺激两个“神经―腓肠肌”标本中的神经,观察现象。(2分)
实验结果:装置1的指针持续向左偏转,装置2的指针向左偏转后恢复。(4分)
28.(14分)(1)碳(1分) (2)![]() (1分)
(1分)
(3)Cl―>O2―>Na+
![]() (4)离子键和极性共价键 (1分) NH4++H2O NH3・H2O+H+(1分)
(4)离子键和极性共价键 (1分) NH4++H2O NH3・H2O+H+(1分)
(5)NH4++HCO3―+2OH―=NH3・H2O+CO32―+H2O(2分)
(6)①N2H4(l)+2H2O2(l)=N2(g)+4H2O(g);△H=-641.5kJ・mol―1(2分)
②O2+2H2O+4e―
4OH―(1分) N2H4+4OH―-4e― 4H2O+N2↑(1分)
Cu2++2e―
Cu(1分) 112(2分) (其它每空1分)
29 (14分) (1)FeC13 (1分)
|
|
(4)2A1+Fe2O3 2Fe+A12O3
(5)①氧气消耗后,烧瓶内气体减少,导致烧瓶内压强减小,因此导管中水面上升。
②B>C>A=D
③电解质溶液
④洗净、擦干、涂油等
30.(14分) Ⅰ(1)AE (2分) (2)C(2分)
Ⅱ(1)E(1分) CaO+NH3・H2O Ca(OH)2+NH3↑(2分)
A、C、D(2分)
(2)E(1分) 蒸馏水(1分),红色固体逐渐变黑(1分)
(3)Cu和CuO可以循环使用,避免了使用有毒物质。(2分)
33
(1)加成反应、氧化反应、还原反应、聚合反应。
(2)CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O。
CH3CH=CHCHO+H2O。
(3)![]() ,
,![]() 。
。
35.(8分,每空1分)
(1)逆转录(2)DNA连接酶 (3)复制 合成S基因的mRNA
(4)大肠杆菌中表达的S蛋白 SARS康复病人血清
(5)相同 表达蛋白质所用的基因相同
36 (8分)解析 (1)设气缸倒置前后被封闭气体的压强分别为P1和P2,气柱长度分别为L1和L2.
![]() (1分)
(1分)
![]() (1分)
(1分)
倒置过程为等温变化,由玻意耳定律可得
![]() (1分)
(1分)![]() (1分)
(1分)
(2)设倒置后升温前后封闭气柱温度分别为
T2和T3,升温后气柱长度为L3.
T2和Tl=(273+7)K=280 K (1分)
L2=15 cm,L3=20 cm (1分)
升温过程为等压变化,由盖一吕萨克定律可得

![]()
37(8分)解:⑴A=0.1 m (1分)![]() (1分)
(1分)
![]() (1分)
(1分)![]() (1分)
(1分)
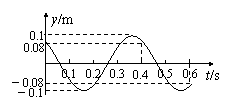 ⑵
⑵
(4分)