可能用到的相对原子质量:H―1,C―12,N―14,O―16,Na―23,Mg―24,Al―27,
S―32,Cl―35.5,K―39,Fe―56, Cu―64,Zn--65
6、在标准状况下,称量一个充满Cl2的容器质量为80.6g,若改充N2,其质量为72g,则容
器的容积为: ( )
A.11.2L B.5.6L C.4.48L D.2.24L
7、一定量的无水乙醇完全燃烧时放出的热量为Q,它所生成的CO2恰好被2mol的烧碱溶液吸收并生成一种正盐,则完全燃烧1mol无水乙醇时放出的热量是:( )
A.0.5Q B.Q C.2Q D.4Q
8、取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是: ( )
A.H2 B.CO C.C6H12O6 D.C12H22O11
9、下列各组离子,在指定的环境中一定能大量共存的是 ( )
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3―、Na+
B.由水电离出的c(H+)=1×10-12mol・L-1的溶液中:K+、Cl-、NO3―、Na+
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42―、Cl―、
D.在能使pH试纸变红色的溶液中:Na+、S2―、NO3―、CO32―
10、我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如右图所示,有关该物质的说法正确的是: ( )
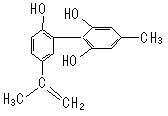 A.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
A.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
B.滴入酸性KMnO4溶液,观察紫色褪去,能证明结构
中存在碳碳双键
C.1mol该物质分别与浓溴水和H2反应时最多消耗Br2
和H2分别为4mol、7mol
D.该分子中的所有碳原子有可能共平面
11、在硫酸铁溶液中,加入a g铜完全溶解后再加入b g铁,充分反应后得到cg残余固体,
且a>c,则下列说法中正确的是: ( )
A.残余固体可能为铁和铜的混合物 B.最后得到的溶液可能含有Fe3+
C.残余固体是铁,溶液中一定不含Cu2+ D.残余固体全部是铜
12、2005年1月美国科学家在《Science》上发表论文,宣布发现了铝的“超级原子”结构―Al13和Al14 。A113、A114的性质很象现行周期表中的某主族元素,且Al13和Al14超级原子结构都是具有40个价电子时最稳定。下列说法中,正确的是 : ( )
A.Al13、Al14互为同位素 B.Al13超原子中Al原子间通过离子键结合
C.Al14最外层电子数之和为42,与ⅡA族元素原子的性质相似,A113与卤素性质相似
D.Al13和Al14都具有较强的还原性,容易失去电子生成阳离子
13、在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是: ( )
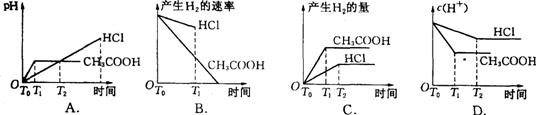
26、(7分)同周期中A、B、C、D、E、F为原子序数依次增大的短周期元素。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。请回答下列问题:
(1)根据以上条件一定能判断出的元素有几种,请填写出相对应的元素符号:
A_______ B_______ C_______ D_______ E_______ F_______。
(2)已知D单质在F单质中燃烧可能生成两种化合物,其中有一种化合物中的所有原子均满足最外层8电子稳定结构,请写出生成该化合物的化学方程式:______________ _____。
(3)若1 mol F的最高价氧化物的水化物与C的最高价氧化物的水化物恰好完全反应,则等物质的量的C的最高价氧化物的水化物与A的最高价氧化物的水化物反应消耗_____mol A的最高价氧化物的水化物。
27、(20分)下列框图中每个字母代表一种物质,其中A是金属单质,B、F是气态非金属单质,其余均为化合物。已知D为淡黄色固体粉末,C为无色无味的液体,G是空气中含量较少的气体,当空气中G的含量增多时会造成“温室效应”。A、D、E、H、M、N中含有同一种金属元素。回答下列问题:
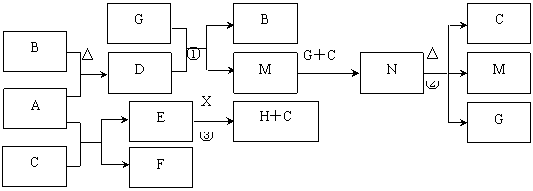
⑴ 写出:A离子的结构示意图 ,G分子的电子式 ,D物质所含有的化学键类型 ;
⑵ 写出下列反应的化学方程式:
① ,
② ;
⑶ X可以是多种类型的物质,H是由三种元素组成的盐。请列举出X可以代表的四种不同类别物质,写出相应的反应③的离子方程式:
当X为 , ,
当X为 , 。
当X为 , ,
当X为 , ,
28、(15分)芳香化合物A、B互为同分异构体,B的结构简式是
O O
|
CH3CO COCH2CH3
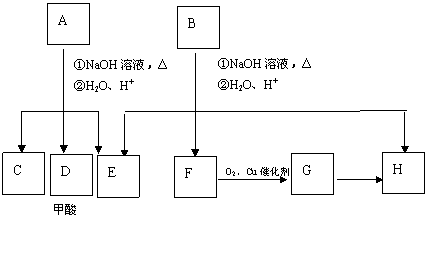
A经①、②两步反应得C、D和E. B经①、②两步反应得E、F和H. 上述反应过程、产物性质及相互关系如图所示.
 |
|
|
|
|
(2)A可能的结构有 种,写出其中任意一种的结构简式 .
(3)在B、C、D、F、G化合物中,互为同系物的是 (填代码).
(4)写出F→G的化学方程式:
(5)B与氢氧化钠溶液共热的化学方程式: ,
反应类型是 .
29、(19分)下图所示装置进行有关实验,将A逐滴加入B中
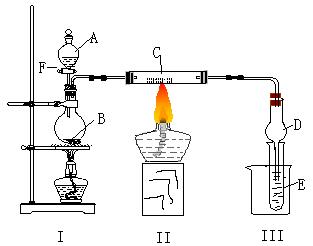
⑴若A是实验室的一种常用燃料,B是生石灰,实验中观察到C中黑色固体逐渐变红,当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜,则A是 ,C是 ,请写出反应管C中所发生的反应方程式: 。 试管E中所发生反应的离子方程式: 。
⑵若I处酒精灯不加热, B、C仍是实验(1)中原物质,实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是 ,E中是 与葡萄糖的混合液(写化学式)。请写出反应管C中所发生反应的方程式: 。仪器D在此实验中的作用是 。
⑶若B为浓硫酸,E为苯酚钠溶液,C仍旧不变,A是只含一个碳的一种有机物也能发生银镜反应,实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管中溶液变浑浊,则A可能是 ,然后往烧杯中加入沸水,可观察到试管中的现象是 ,此实验中浓硫酸的作用是 。写出(1)中A和(3)中A二种物质在浓硫酸存在时所发生的反应方程式:
,此反应中浓硫酸的作用是 。
6―13题答案: CCDBCDCC
26、(6分)(1)A Na B Mg C Al D E F Cl (2分)
(2) 2P+3Cl2==2PCl3 (2分)
(3)1/3 (2分)
27、(20分)⑴![]() (1分) O∷C∷O (1分) 离子键、非极性(共价)键(2分)
(1分) O∷C∷O (1分) 离子键、非极性(共价)键(2分)
![]() ⑵ ① 2Na2O2+2CO2=2Na2CO3+O2 (各2分)
⑵ ① 2Na2O2+2CO2=2Na2CO3+O2 (各2分)
②
⑶ Al2O3:Al2O3+2OH-=2AlO2-+H2O Al(OH)3:Al(OH)3+OH-=AlO2-+2H2O
H2SO4:H++OH-=H2O NaHCO3:HCO3-+OH-=CO32-+H2O
|
|
|
HCOO― ―COOCH2CH2CH3 HCOO― ―COOCH(CH3)2 (4分)
(3)C和F (2分)
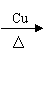
(4)2CH3CH2OH+O2 2CH3CHO+2H2O↑ (2分)
(5)
O O
|
|
CH3CO COCH2CH3 +3NaOH→CH3COONa+ NaO COONa + C2H5OH
+H2O (3分)
水解或取代 (2分)
29、 (19分)(1)乙醇 CuO (各1分)CuO+CH3CH2OH → CH3CHO+Cu+H2O(2分)
CH3CHO + 2[Ag(NH3)2]+ + 2OH - →CH3COO- + NH4+ + 2Ag↓+ 3NH3 + H2O (2分)
(2)浓氨水 AgNO3(各1分) 3CuO+2NH3→N2+3Cu+3H2O(2分)防止倒吸。(2分)
(3)HCOOH 变澄清 脱水性(各1分) HCOOH+C2H5OH → HCOOC2H5+H2O(2分)
催化剂和吸水剂(2分)