高三化学氮族元素单元测试题
时间:60分钟 分值:108分
拟题:易超 审题:裴年喜 2007-10-04
一、选择题(本题包括12小题,每小题4分,共48分,每小题只有一个选项符合题意)
1、汽车排放的尾气中因含有氮的氧化物而污染大气,造成产生氮的氧化物的主要原因是
A.燃烧含氮化合物燃料引起的 B.燃烧含铅汽油引起的
C.是由于燃烧不充分引起的 D.是在气缸中N2被氧化生成的
2、引起下列环境污染的原因不正确的是
A.重金属、农药和难分解有机物等会造成水体污染
B.装饰材料中的甲醛、芳香烃及氡等会造成居室污染
C.SO2、NO2或CO2都会导致酸雨的形成
D.CO2和氟氯烃等物质的大量排放会造成温室效应的加剧
3、下列有关试剂的保存方法,错误的是
A、浓硝酸保存在无色玻璃试剂瓶中 B、少量的钠保存在煤油中
C、氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中
D、新制的氯水通常保存在棕色玻璃试剂瓶中
4、用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。下列不易区别其真伪的方法是
 A.测定密度
B.放入硝酸中 C.放入盐酸中
D.观察外观
A.测定密度
B.放入硝酸中 C.放入盐酸中
D.观察外观
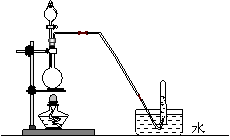
5、下列气体的制备可采用右图装置的是
A.铜与浓硝酸反应制NO2
B.铜与稀硝酸反应制NO
C.乙醇与浓硫酸反应制乙烯
D.氯化钠与浓硫酸反应制HCl
6、已知元素砷(As)的原子序数为33,下列叙述正确的是
A.砷元素的最高化合价为+3 B.砷元素是第四周期的主族元素
C.砷原子的第3电子层含有8个电子 D.砷的氧化物的水溶液呈弱碱性
7、将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
A.稀硝酸 B.稀盐酸 C.硝酸铜 D.氢氧化钠
![]() 8、将a
L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是
8、将a
L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是
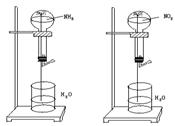 9、同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3②NO2,进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度:
9、同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3②NO2,进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度:
A.①>② B.①<②
C.①=② D.不能确定
10、等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
A.、6 mol・L-1 KOH溶液 B、18 mol・L-1 H2SO4溶液
C、2 mol・L-1 H2SO4溶液 D、3 mol・L-1 HNO3溶液
11、在一定条件下,将m体积NO和n体积O2同时通入倒立于水中且盛满水的容器中内,充分反应后,容器内残留m/2体积的气体,该气体与空气接触后变为红棕色。则m的n比值为
A 3∶2 B 2∶3 C 8∶3 D 3∶8
12、有混合气体x,它是由NO、H2、CO2组成,通入足量的Na2O2层后,变成混合气体y,将y用电火花引燃使其充分反应,只得到浓度为70%的HNO3溶液,无其他任何气体,则x中NO、H2、CO2的体积之比为:
A、 1∶1∶1 B、1∶2∶7 C、3∶2∶2 D、2∶4∶7
二、填空题(本题包括4小题,共60分,)
13、(19分,每空2分)资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
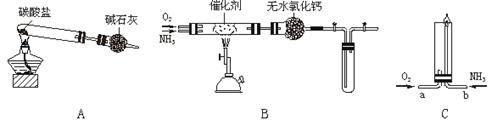
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________________;碱石灰的作用是_______________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是_________________________________________;(3分)试管内气体变为红棕色,该反应的化学方程式是_____________________________。(3分)
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因_________________________________________
_____________________________________________________________________________
____________________________________________________________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是_________________________________________________,其理由是_____________________________________________________________________
____________________________________________________________________________。
②氨气燃烧的化学方程式是_____________________________________________(3分)
14、(14分,每空2分)已知X、Y、Z都是短周期的元素,它们的原子序数依次递增。X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的三倍,Y和Z可以形成两种以上气态化合物,则
(1)X是 ,Y是 ,Z是 。(填元素名称)
(2)由Y和Z组成,且Y和Z的质量比为7∶20的化合物的化学式(分子式)是 。
(3)由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子是
和 。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,该盐的化学式(分子式)是 。
15、(15分,每空3分)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。(b)反应①、②是化工生产中的重要反应。(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。(e)化合物J由两种元素组成,其相对分子质量为32。
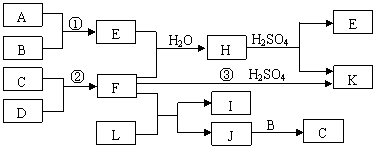 |
请按要求填空:
(1)反应③的化学方程式 。
(2)C的结构式 ;H的化学式 。
(3)L的溶液与化合物E反应的离子方程式 。
(4)化合物J的化学式 。
16、(12分)将9.6 g 铜加入50 mL 12 mol・L-1HNO3溶液中,待铜全部溶解后剩余溶液的pH=0(忽略溶液体积的变化),产生的气体(NO、NO2、N2O4中的一种或几种)折算成标准状况下的体积为4.48 L,则所得气体的成分及各成分的物质的量为:
| 气体的成分 | 各成分的物质的量 |