高三化学反应速率与化学平衡专题
【例题】
1、在恒温、恒容的密闭容器中进行反应A(g)![]() B(g)+C(g),若A的浓度从2.0mol/L降低到1.5mol/L时需要20s,那么A浓度有1.5mol/L降低到1.0mol/L时所需的时间为:( )
B(g)+C(g),若A的浓度从2.0mol/L降低到1.5mol/L时需要20s,那么A浓度有1.5mol/L降低到1.0mol/L时所需的时间为:( )
A、20s B、大于20s C、小于20s D、无法判断
2、在一定条件下,将1 mol CO和1 mol水蒸气混合后发生如下变化:CO(g)+H2O(g) ![]() CO2(g)+H2(g)若反应达平衡时测得CO转化率为21.75%,则平衡混合气体的密度为相同条件下H2 密度的:( )
CO2(g)+H2(g)若反应达平衡时测得CO转化率为21.75%,则平衡混合气体的密度为相同条件下H2 密度的:( )
A、5.75倍 B、11.5倍 C、30.67倍 D、46倍
3、将1
mol CO和1 mol H2O(g)充入某固定容积的反应器中,在某条件下达到平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g),此时有CO转化为CO2。在相同条件下,若将1 mol CO2、1mol H2和1 mol H2O(g)充入同一反应器中,当反应达到平衡后,混合气体中CO2的体积分数可能为: ( )
CO2(g)+H2(g),此时有CO转化为CO2。在相同条件下,若将1 mol CO2、1mol H2和1 mol H2O(g)充入同一反应器中,当反应达到平衡后,混合气体中CO2的体积分数可能为: ( )
A、22.2% B、27.5% C、33.3% D、36.8%
4、在一定条件下,测得2CO2![]() 2CO+O2平衡体系的平均相对分子质量为M 。在此条件下,CO2的分解率是:( )
2CO+O2平衡体系的平均相对分子质量为M 。在此条件下,CO2的分解率是:( )
A、 B、 C、 D、
5、在一个密闭容器中,可逆反应aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则:( )
bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则:( )
A、平衡向正反应方向移动了 B、物质A的转化率减小了
C、物质B的质量分数增加了 D、a>b
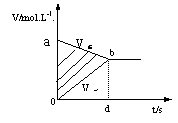 6、在容积固定的4L密闭容器中进行可逆反应X(g)+2Y(g)
6、在容积固定的4L密闭容器中进行可逆反应X(g)+2Y(g)![]() 2Z(g),并达到平衡,在此过程中以Y的浓度改变表示的反应速率V(正)、V(逆)与时间t的关系如下图。图中阴影部分的面积表示:( )
2Z(g),并达到平衡,在此过程中以Y的浓度改变表示的反应速率V(正)、V(逆)与时间t的关系如下图。图中阴影部分的面积表示:( )
A、X的浓度的减少 B、Y的物质的量的减少
C、Z的浓度的增加 D、X的物质的量的减少
7、 在5L的密闭容器中充入2molA气体和1molB气体,在一定条件下发生反应:2A(g)+B(g) ![]() 2C(g),达到平衡时,在相同温度下测得容器内混合气体的压强是反应前的5/6,则A的转化率为:( )
2C(g),达到平衡时,在相同温度下测得容器内混合气体的压强是反应前的5/6,则A的转化率为:( )
A、67% B、50% C、25% D、5%
8、1 mol A气体与1 mol B气体在密闭容器中反应:
A(g)+nB(g) ![]() mC(g),反应进行一段时间后,测得A的转化率为50%。同温同压下,还测得反应前混合气体的密度是反应后混合气体密度的3/4,则n和m的数值可能是:( )
mC(g),反应进行一段时间后,测得A的转化率为50%。同温同压下,还测得反应前混合气体的密度是反应后混合气体密度的3/4,则n和m的数值可能是:( )
A、n=4,m=4 B、n=3,m=3 C、n=2,m=2 D、n=1,m=1
9、16mL由NO与NH3组成的混合气体在催化剂作用下于400℃左右发生反应: 6NO + 4 NH3 ![]() 5N2+6H2O(g),达平衡后在相同条件下混合气体的体积变为17mL。原混合气体中NO与NH3的物质的量之比可能是①3:1②3:2③3:4④3:5 :( )
5N2+6H2O(g),达平衡后在相同条件下混合气体的体积变为17mL。原混合气体中NO与NH3的物质的量之比可能是①3:1②3:2③3:4④3:5 :( )
A、①② B、①④ C、②③ D、③④
10、在一密闭容器中进行以下反应:C(s)+H2O(g)![]() CO(g)+H2(g) 达到平衡后当温度不变,增大压强,混合气的平均相对分子质量的变化趋势是:( )
CO(g)+H2(g) 达到平衡后当温度不变,增大压强,混合气的平均相对分子质量的变化趋势是:( )
A、增大 B、减小 C、不变 D、无法确定
【练习题】
1、在恒温恒容的密闭容器中进行吸热反应:H2![]() 2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为 :( )
2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为 :( )
A、等于18s B、大于18s C、等于12s D、小于18s
2、在一定温度下,将2molSO3(气)放入某定容的密闭容器中,当反应达到平衡时2SO3(g) ![]() 2SO2(g)+O2(g),容器内有1.2molSO2,其平衡混合物的密度在相同条件下H2密度的倍数是 :( )
2SO2(g)+O2(g),容器内有1.2molSO2,其平衡混合物的密度在相同条件下H2密度的倍数是 :( )
A、30.8 B、61.5 C、80 D、40
3、将1mol CO和1mol H2O (g) 充入某固定容积的反容器中,在一定条件下CO(g)+H2O(g) ![]() CO2(g)+H2(g)达到平衡,有1/2的CO转化为CO2在条件相同时,1mlCO和3molH2O(g)充入同一反应容器中,当反应达到平衡后,混合气体中CO2的体积分数可能为 :( )
CO2(g)+H2(g)达到平衡,有1/2的CO转化为CO2在条件相同时,1mlCO和3molH2O(g)充入同一反应容器中,当反应达到平衡后,混合气体中CO2的体积分数可能为 :( )
A、10% B、15% C、25% D、50%
4、反应2A(g) ![]() x B(g)+2C(g),在一定条件下达到平衡时,密闭容器内的压强增大了30%,此时A的转化率为20%,则x的值为:( )
x B(g)+2C(g),在一定条件下达到平衡时,密闭容器内的压强增大了30%,此时A的转化率为20%,则x的值为:( )
A、5 B、4 C、3 D、2
5、在一密闭容器中,反应mA(g)+nB(s) ![]() 3C(g)达到平衡时,测得c(A)为0.5
mol/L在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.3
mol/L,则下列判断不正确的是:( )
3C(g)达到平衡时,测得c(A)为0.5
mol/L在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.3
mol/L,则下列判断不正确的是:( )
A、混合气体密度一定减小 B、平衡一定向逆反应方向移动
C、化学计量数:m+n>3 D、物质C的体积分数增加了
6、在容积固定为2L密闭容器中,充入X、Y各2mol发生可逆反应:X(g)+2Y(g)![]() 2Zg达到平衡,以Y的浓度改变表示的化学反应速率
2Zg达到平衡,以Y的浓度改变表示的化学反应速率![]() 、
、![]() 与时间的关系如图,则Y的平衡浓度的表达式正确的是(式中S指对应区域的面积)( )
与时间的关系如图,则Y的平衡浓度的表达式正确的是(式中S指对应区域的面积)( )
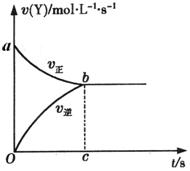
A、2―Saob B、1―Saob C、2―Sabdo D、1―Sbod
7、在合成氨反应过程中,某一时刻混合气体中各成分的体积比为V(N2):V(H2):V(NH3)=6:18:1,反应一段时间后,混合气体中体积比变为V(N2):V(H2):V(NH3)= 9:27:8,则这一段时间内H2转化率为(气体体积在相同条件下测定):( )
A、67% B、50% C、25% D、5%
8、1 mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)
![]() bZ(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是:( )
bZ(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是:( )
A、a=1,b=1 B、a=2,b=1 C、a=2,b=2 D、a=3,b=2
9、容积不变的反应容器中,要求通过调节体系温度使A(g)+2B(g)![]() 2C(g)达平衡时保持气体总物质的量为12mol,现向反应容器中通入6.5molA、xmolB和2molC,欲使起始反应向逆反应方向移动,x的取值范围为
2C(g)达平衡时保持气体总物质的量为12mol,现向反应容器中通入6.5molA、xmolB和2molC,欲使起始反应向逆反应方向移动,x的取值范围为
10、一定温度下C(s)和水蒸气在密闭容器中发生反应,建立化学平衡:C(s)+H2O(g)![]() CO(g)+H2(g);∆H>0。
CO(g)+H2(g);∆H>0。
(1)平衡混合气的平均相对分子质量Mr(平)的取值范围为______>Mr(平)>________。(2)若使用CO和H2从逆反应方向在相同温度下建立平衡,则平衡混合气的平均相对分子质量Mr(平)的取值范围为___________>Mr(平)____________。此时若加压,平衡将_____________(向左、向右、不)移动,设原平衡时混合气中气体的物质的量共a mol,加压、重新达到平衡后气体比原来平衡减少b mol,则新平衡时混合气平均相对分子质量Mr'(平)和Mr(平)的关系为Mr'(平)=____________________(用Mr(平),a、b的数字表示。)
(3)在(2)建立的平衡中,①当Mr'(平)=Mr(平)时,Mr(平)=________,此反应开始时,所用CO、H2的物质的量之比__________。②当Mr(平)<_______________时,Mr'(平)<Mr(平),当Mr(平)>__________________时,Mr'(平)>Mr(平)。
(4)由(3)得出结论:从逆反应方向建立平衡时,Mr'(平)与Mr(平)的相对大小主要取决于__________________________________。
11、在反应2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)达到平衡后,再增大压强,则:
CO(NH2)2(s)+H2O(g)达到平衡后,再增大压强,则:
(1)如果反应物的平均相对分子质量小于30,则平衡混合气体平均相对分子质量将_____________________。(填“减小”、“增大”或“不变”,下同)
(2)如果反应物的平均相对分子质量大于30,则平衡混合气体平均相对分子质量将_____________________。
(3)如果反应物的平均相对分子质量等于30,则平衡混合气体平均相对分子质量将_____________________。
12、下列事实不能用勒夏特列原理解释的是:_______________________
⑴工业生产硫酸的过程中使用过量氧气,以提高SO2的转化率
⑵合成氨工厂通常采用20MPa-50MPa压强,以提高原料的利用率
⑶实验室用排饱和食盐水的方法收集氯气
⑷经粉碎的黄铁矿在沸腾炉中燃烧得较快,较完全
⑸配制FeSO4溶液时加铁粉可防止氧化变质
⑹硫磺在纯氧中燃烧比在空气中剧烈
⑺温度控制在500℃有利于合成氨反应
⑻打开碳酸饮料会有大量气泡冒出
⑼工业制取金属钾 Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
⑽将混合气中的氨气液化,有利于合成氨的反应
⑾开启啤酒瓶后,瓶中马上泛起大量泡沫
⑿由H2(g)+I2(g)![]() 2HI(g)组成的平衡体系,加压后颜色加深
2HI(g)组成的平衡体系,加压后颜色加深
⒀溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
⒁反应CO+NO2![]() CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动。
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动。
⒂加入催化剂有利于氨的氧化反应
⒃在硫化氢水溶液中加入碱有利于S2―的生成
⒄加热可以提高纯碱溶液的去污能力
⒅钢铁在潮湿的空气中容易生锈
参考答案:
例题:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | B | B | B | AC | C | B | D | C | D |
练习题:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | B | A | B | C | D | B | C | AD |
9、2.5<x<3.5
10、(1)18>Mr(平)>15 (2)28> Mr(平)>2 向左 M'r(平)=
(3) ①M'r(平)=12 5:8 ②12 ,12 (4)起始时,CO和H2的物质的量之比
11、(1)减小;(2)增大;(3)不变
12、⑷ ⑸ ⑹⑺ ⑿ ⒂ ⒅