高三化学反应速率平衡单元测试
班级__________学号_________姓名______________
一、选择题
( )1、在恒温恒容条件下,将4molA和2molB放入一密闭容器中发生反应:2A(g)+B(g)![]() 2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是:
2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是:
A.4mol、2mol、0mol、2mol B.2mol、1mol、2mol、2mol
C.2mol、1mol、2mol、1mol D.2mol、1mol、0mol、1mol
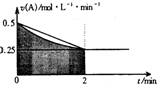 ( )2、某溶液中发生反应:A=2B+C,A的反应速率v(A)与时间t的图象如图所示。若溶液的体积为2L,且起始时只加入A物质,下列说法错误的是:
( )2、某溶液中发生反应:A=2B+C,A的反应速率v(A)与时间t的图象如图所示。若溶液的体积为2L,且起始时只加入A物质,下列说法错误的是:
A.图中阴影部分的面积表示0―2min内A的物质的量浓度的减小值
B.反应开始的前2min,A的平均反应速率小于0.375mol・L-1・min-1
C.至2min时,A的物质的量减小值介于0.5mol至1mol之间
D.至2min时,c(B)介于1mol・L-1 至1.5mol・L-1 之间
( )3、已建立化学平衡的某可逆反应,当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的质量分数一定增加 ②生成物产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速度一定大于逆反应速度 ⑥一定使用催化剂
A.①②⑤ B.③④⑤ C.②⑤ D.④⑥
 ( )4、反应
( )4、反应![]()
![]() 2AB;△H=Q,在不同温度和压强改变
2AB;△H=Q,在不同温度和压强改变
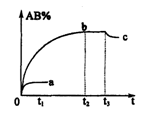
的条件下,产物AB的质量分数AB%生成情况如下图:a为500℃
时的情况;b为300℃时的情况;c为反应在300℃时从时间![]() 开
开
始向容器中加压的情况.则下列叙述正确的是
A.![]() 、
、![]() 及AB均为气体,Q>0
及AB均为气体,Q>0
B.AB为气体,![]() 、
、![]() 中至少有一种为非气体,Q<0
中至少有一种为非气体,Q<0
C.AB为气体,![]() 、
、![]() 中有一种为非气体,Q<0
中有一种为非气体,Q<0
D.AB为固体,![]() 、
、![]() 中有一种为非气体,Q>0
中有一种为非气体,Q>0
( )5、在恒温恒压下,将3molA和1molB放入一密闭容器中发生反应:2A(g)+B(g)![]() 2C(g),
2C(g),
达到化学平衡(Ⅰ)。在同样条件下,3molA和2molB发生同样的反应,达到化学平衡(Ⅱ)。现
将平衡(Ⅱ)的混合气全部压入平衡(Ⅰ)的容器中,在同样条件下达到化学平衡(Ⅲ)。下面关于平
衡(Ⅰ)、(Ⅱ)、(Ⅲ)的说法错误的是:
A.平衡(Ⅲ)中A的转化率等于B的转化率 B.平衡(Ⅰ)中A的转化率小于B的转化率
C.n(C)/n(A)的比值,平衡(Ⅲ)比平衡(Ⅰ)小 D.n(A)/n(B)的比值,平衡(Ⅲ)比平衡(Ⅱ)小
( )6、甲、乙两容器都发生反应 2A(g)+ B(g ) ![]() xC(g),两容器温度和初始压强都相同。甲容器中充入 2 molA 和 1 molB,达平衡后,C 在平衡混合气中的体积分数为φ、物质的量为 n1;乙容器中充入 1.4
molA,0.7 molB 和 0.6 molC,达平衡后 C 在平衡混合气中的体积分数为φ、物质的量为 n2。下列说法中正确的是
xC(g),两容器温度和初始压强都相同。甲容器中充入 2 molA 和 1 molB,达平衡后,C 在平衡混合气中的体积分数为φ、物质的量为 n1;乙容器中充入 1.4
molA,0.7 molB 和 0.6 molC,达平衡后 C 在平衡混合气中的体积分数为φ、物质的量为 n2。下列说法中正确的是
A.若甲、乙两容器均为恒容容器,则 x必等于 2
B.若甲、乙两容器均为恒压容器,则 x必等于 3
C.若甲为恒压容器、乙为恒容容器,且 x≠3,则 n1必大于 n2
D.若甲为恒容容器、乙为恒压容器,且 x= 3,则 n1必大于 n2
( )7、下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O ![]() HBr+ HBrO,当加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO,当加入 AgNO3溶液后,溶液颜色变浅
B.对CO + NO2 ![]() CO2+ NO,平衡体系增大压强可使颜色变深
CO2+ NO,平衡体系增大压强可使颜色变深
C.在电解含有酚酞的硫酸钠溶液时,阴极附近溶液的颜色变红
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
( )8、在一条件下,可逆反应2A(气)+B(气)![]() nC(固)+D(气)达平衡。若维持温度不变,增大压强,测得混合气体的平均相对分子质量不变,则下列判断正确的是
nC(固)+D(气)达平衡。若维持温度不变,增大压强,测得混合气体的平均相对分子质量不变,则下列判断正确的是
(A)其它条件不变,增大压强,平衡不发生移动
(B)其它条件不变,增大压强,混合气体的总质量不变
![]() (C)该反应式中n值一定为2
(C)该反应式中n值一定为2
(D)原混合气中A与B的物质的量之比为2:1,且
( )9、对于平衡体系:aA(g)+bB(g)![]() cC(g)+dD(g);正反应放热,有下列判断,其中正确的是:
cC(g)+dD(g);正反应放热,有下列判断,其中正确的是:
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a+b大于c+d
B.若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为a:b
C.若平衡体系中共有气体M mol,再向其中充入bmolB,达到平衡时气体总物质的量为M+bmol,则a+b=c+d
D.若a+b=c+d ,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变。
( )10、有如下反应2SO2(g)+ O2(g)
![]() 2SO3(g),△H=―197KJ/mol,同温下,往体积相同
2SO3(g),△H=―197KJ/mol,同温下,往体积相同
的密闭容器A、B中分别充入2molSO2、1mol O2和1mol SO2、0.5mol O2、1mol2SO3,当它们
分别达到平衡时放出的热量为Q1KJ和Q2 KJ,则下列比较正确的是
A. Q1=2Q2=197KJ B. Q1=2Q2〈197KJ C.2Q2〈Q1〈197KJ D.Q1〈2Q2〈197KJ
二、填空题
11.反应aA(g) +bB(g) ![]() cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为a∶b。则
cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为a∶b。则
(1)平衡时A与B的转化率之比是_______________。
(2)若同等倍数地增大A、B的物质的量浓度,要使A与B的转化率同时增大,(a+b)与(c+d)所满足的关系是(a+b) (c+d) (填“>”“=”“<”或“没关系”)。
(3)设定a=2 ,b=1,c=3,d=2,在甲、乙、丙、丁4个容器中A的物质的量依次是2 mol、1 mol、2 mol、1 mol,B的物质的量依次是1 mol、1 mol、2 mol、2 mol,C和D的物质的量均为0。则在相同温度下达到平衡时,A的转化率最大的容器是 ,B的转化率由大到小的顺序是 (填容器序号)。
12.在一个密闭容器中,有一个左右可滑动隔板,两边分别进行可逆反应,各物质的量如下:M、N、P为2.5mol、3.0mol、1.0mol。A、C、D各为0.50mol,B的物质的量为x,当x的物质的量在一定范围内变化,均可以通过调节反应器的温度,使两侧反应均达到平衡,且隔板在反应器的正中位置。达到平衡后,测得M的转化率为75%,填写空白:
(1)达到平衡后,反应器左室气体总的物质的量为 mol。
(2)若要使右室反应开始时V正>V逆,x的取值范围 。
(3)若要使右室反应开始时V正<V逆,x的取值范围 。
13.密闭容器中,保持一定温度,进行如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
已知加入1 mol N2和3 mol H2,在恒压条件下,达到平衡时生成a mol NH3[见下表中编号(1)
的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,
达到平衡时混合物中各组分的百分含量不变,请填空:
| 项目 条件 | 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量 (mol) | |||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒 压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 0 | |||
| (3) | 0.2 | 0.5a | |||
| x、y、z取值必须满足的一般条件:____________________________________________。 | |||||
| 恒 容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | b | ||
| (6) | 2.25 | b | |||
| x、y、z取值必须满足一般条件(一个只含x、z,另一个只含y、z): ; 。 | |||||
| a与b的关系是:a b(填>、<、=) | |||||
14.一定条件下,某容积为1L的密闭容器中发生如下反应:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
(Ⅰ)(1)维持温度不变,向该容器中充入2 mol C(s)和2 mol H2O(g),达到平衡后混合气体的平均相对分子质量为Mr,则Mr的范围为 。
(2)在(1)中若充入的是2.5 mol CO(g)和4 mol H2(g),达到平衡后混合气体的平均相对分子质量为 ;若要求达到平衡后混合气体的平均相对分子质量始终大于该值,则充入的CO、H2混合气体的总质量m和总物质的量n必须满足的关系为 。
(Ⅱ)维持温度不变,若在(1)中同时充入1
mol Br2(g),发生如下反应:H2(g)+Br2(g)![]() 2HBr(g)(忽略其他反应)
2HBr(g)(忽略其他反应)
(3)当上述体系达到平衡后,测得容器中c(H2O)平=0.4 mol・L-1,c(Br2)平=0.6 mol・L-1,则平衡时c(H2)平=_______mol・L-1。
(4)当上述体系达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不可能同时是: 和 ,或 和 (填化学式)。
15.在恒温时,向某密闭容器中通入2 mol X和l mol y气体,发生如下反应:2X(g)+Y(g)![]() 2Z(g),压强一定时,测得在平衡时
Z的体积分数为 0.4。
2Z(g),压强一定时,测得在平衡时
Z的体积分数为 0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4 mol X(g)和 2 mol Y(g).达到平衡,则Z的体积分数为_________;平衡时,气体的总物质的量是__________。
(2)与上述平衡保持同温、同压,若向密闭容器中通入X(g)和Y(g)的物质的量分别记为n(X)、n(Y),并满足平衡时Z的体积分数为0.4,则n(x)/n(y)的取值范围为_____________________。
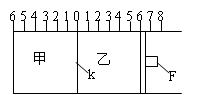 16.(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)
16.(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)![]() 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
(1)可根据 现象来判断甲、乙都已达到平衡。
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是 。
(3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为 mol,
乙中C的转化率 50%(填:>、<、=),此时,乙中可移动活塞F最终停留在右侧
刻度 处(填下列序号:① <6 ② >6 ③ =6)
(4)若达到平衡时,隔板K最终停留在左侧刻度靠近0处,则乙中可移动活塞F最终停留在右侧的刻度不大于 ;若K最终停留在左侧刻度靠近2处,则乙中F最终停留在右侧的刻度不小于 。
(Ⅱ)若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(1)甲、乙中C的物质的量是 (填:“甲>乙”或“甲<乙”或“甲=乙” );
(2)测得甲中A的转化率为b,则乙中C的转化率为 ;
(3)假设乙、甲两容器中的压强比用d表示,则d的取值范围是 。
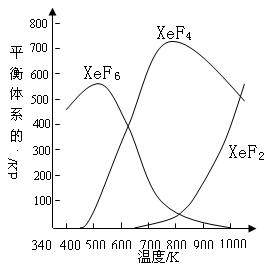 17、在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如右图所示(己知气体的分压之比等于物质的量之比)。
17、在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如右图所示(己知气体的分压之比等于物质的量之比)。
(1)420K时,发生反应的化学方程式为:
____________________________ ;
若反应中消耗l mol Xe,则转移电子_______mol。
(2)600~800K时,会发生反应:
XeF6(g)![]() XeF4(g)+ F2(g),
XeF4(g)+ F2(g),
其反应热△H _______0(填“>”“=”或“<”)。
理由是____________________________________。
(3)900K时,容器中存在的组分有________________
 18.在一定条件下,二氧化碳和氧气发生如下反应:
18.在一定条件下,二氧化碳和氧气发生如下反应:
![]() 2SO2(g)+ O2
(g) 2SO3(g)
+ Q (△H〈0)
2SO2(g)+ O2
(g) 2SO3(g)
+ Q (△H〈0)
(1) 在化工生产中常用化学平衡常数K来表示化学反应
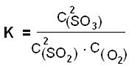 进行的程度,
进行的程度,
则降低温度,该反应K值 ,二氧化硫转化率 ,
化学反应速度 (以上均填增大、减小或不变)
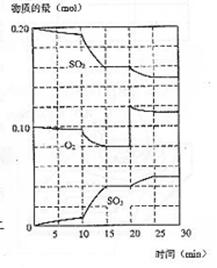
(2)600℃时,在一密闭容器中,将二氧化硫和氧气混
合,反应过程中SO2、O2、SO3物质的量变化如图,
反应处于平衡状态的时间是 。
(3)据图判断,反应进行至20min时,曲线发生变化的原因是
(用文字表达)
10min到15min的曲线变化的原因可能是 (填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量
《化学反应速率 化学平衡》参 考 答 案
一、选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | C | C | B | D | D | B | D | BC | C |
二、填空题
11、(1)1:1(2)〉(3)丁(4)甲〉乙〉丙〉丁
12、(1)3.5mol (2)2.0<x<3.0 (3)1.5<x<2.0
13、
| 恒 压 | (2) | 9 | 3a | ||
| (3) | 0.4 | 1.2 | |||
| x、y、z取值必须满足的一般条件:y=3x(x≥0);z≥0 (x、y、z不同时为0)。 | |||||
| 恒 容 | (5) | 2 | |||
| (6) | 0.75 | 0.5 | |||
| x、y、z取值必须满足一般条件(一个只含x、z,另一个只含y、z): 2x+z=2;2y+3z=6 。 | |||||
| a与b的关系是:(1分)a > b(填>、<、=) | |||||
14、(1)15<Mr<18 (2)12; m>12n (3)1.2 (4)H2O和CO或Br2和HBr
15、⑴ 0.4; 5.0 mol (2)0.5<n(X)/n(Y)<5
16、Ⅰ(1)K、F不再移动(2)0<a<2 (3)1mol、〉、② (4)8、4
Ⅱ(1)甲=乙(2)1-b(3)4/3<a<3/2
![]() 17、(1)Xe+3F2 XeF6、6(2)>(3)Xe、F2、XeF2、XeF4、XeF6
17、(1)Xe+3F2 XeF6、6(2)>(3)Xe、F2、XeF2、XeF4、XeF6
18、(1)增大、增大、减小
(2)15-20min、25-30min
(3)增大O2的浓度、ab