高三化学第一学期11月月考试题
化学
一、选择题:(每题3分,共48分)
1.查阅资料发现,金属钠不仅能跟氧气和水反应.还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同点, 下列的研究方法中没有用到的是
A.实验法 B.观察法 C.分类法 D.比较法
2.我国神舟六号飞船发射时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ•mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534 kJ•mol-1。关于肼和二氧化氮反应的热化学方程式中正确的是
A.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)△H=-1135.7kJ•mol-1
B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7kJ•mol-1
C.N2H4(g)+NO2(g)=3/2N2(g)+2H2O(g)△H=-1135.7kJ•mol-1
D.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=+1135.7kJ•mol-1
3.分析下图所示的四个原电池装置,其中结论正确的是
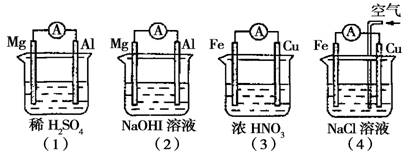 |
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为:6H2O+6e-→6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为:Fe→Fe2++2e-
D.(4)中Cu作正极,电极反应式为:2H++2e-→H2↑
4. 100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①烧瓶内气体的颜色不再加深,②N2O4 的消耗速率与NO2的生成速率之比为1∶2,③NO2的生成速率与NO2消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体的平均相对分子质量不再变化
A.②⑤⑦ B.①③④⑥⑧ C.只有③ D.只有⑤
5.X、Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是 ( )
A.X的金属性比Y的金属性强
B.常温下,X和Y都不能从水中置换出氢
C.Y元素的最高价氢氧化物碱性比X元素最高价氢氧化物碱性强
D.Y元素的最高化合价比X元素的最高化合价高
6.下列关于晶体的说法一定正确的是
 A.第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同
A.第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同
B.晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子
C.离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键
D.C60晶体(其结构模型如上图)中每个C60分子周围与它距离最近且等距离的C60分子有12个
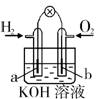 7.燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如右图所示,a、b均为惰性电极。下列叙述不正确的是
7.燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如右图所示,a、b均为惰性电极。下列叙述不正确的是
A.a极是负极,该电极上发生氧化反应
B.b极反应是O![]() +4OH
+4OH![]() -4e
-4e![]() =2H
=2H![]() O
O
C.总反应方程式为2H![]() +O
+O![]() =2H
=2H![]() O
O
D.氢氧燃料电池是一种具有应用前景的绿色电源
8.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去):
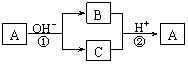 |
下列判断正确的是( )
A.X元素可能为Al B.X元素一定为非金属元素
C.反应①和②互为可逆反应 D.反应①、②不一定为氧化还原反应
9. 某温度下,在一容积可变的容器中,反应2A(g)+B(g) ![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半 B.均加倍
C.均增加1 mol D.均减少1 mol
10.将质量分数为0.052(5.2%)的NaOH溶液1升(密度为1.06克/毫升)用铂电极电解,当溶液中的NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中应符合的关系是
| NaOH的质量分数 | 阳极析出物的质量(克) | 阴极析出物的质量(克) | |
| A | 0.062(6.2%) | 19 | 152 |
| B | 0.062(6.2%) | 152 | 19 |
| C | 0.042(4.2%) | 1.2 | 9.4 |
| D | 0.042(4.2%) | 9.4 | 1.2 |
11.下列叙述不正确的是
A.原子晶体中原子间平均距离越小,熔、沸点越高
B.在水溶液中能电离出自由移动的离子的晶体不一定是离子晶体
C.SnH4 、GeH4、SiH4、CH4四种物质的熔点依次降低
D.水加热到很高的温度都难以分解,是因为水分子之间存在着氢键
![]() 12.电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为
12.电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为
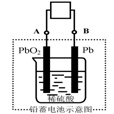 Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,
Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,
则下列说法正确的是
A.放电时:电流方向由B到A
B.放电时:正极反应是Pb-2e-+SO42-![]() PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是PbSO4-2e-+2H2O![]() PbO2+SO42-+4H+
PbO2+SO42-+4H+
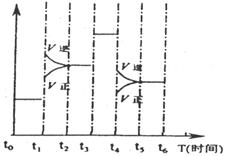 13.右图表示反应N2(g)+3H2(g) ⇌2NH3(g);△H<0在某一时间段中反应速率与反应过程的曲线关系图,则氨的百分含量最低的一段时间是.
13.右图表示反应N2(g)+3H2(g) ⇌2NH3(g);△H<0在某一时间段中反应速率与反应过程的曲线关系图,则氨的百分含量最低的一段时间是.
A. to-t1 B. t2-t3
C. t3-t4 D. t5-t6
14、在一定条件下化学反应:2SO2(g)
+ O2(g) ![]() 2SO3(g);△H=-197kJ・mol-1。现有容器固定且相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和该反应放出的热量(Q)如下表所列:
2SO3(g);△H=-197kJ・mol-1。现有容器固定且相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和该反应放出的热量(Q)如下表所列:
| 容器 | SO2(mol) | O2(mol) | He(mol) | Q (kJ) |
| 甲 | 2 | 1 | 0 | Q 1 |
| 乙 | 1 | 0.5 | 0 | Q 2 |
| 丙 | 1 | 0.5 | 1 | Q 3 |
根据以上数据,下列叙述不正确的是
A、 Q1<197 B、Q2 = Q3 C、Q1 = 2Q2 D、Q1 >2Q2
15.500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是
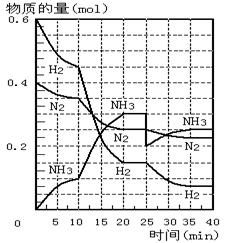 A.反应开始到第一次平衡时,N2的平均反应速率为0.005mol/(L・min)
A.反应开始到第一次平衡时,N2的平均反应速率为0.005mol/(L・min)
B.从曲线变化可以看出,反应进行到10min至
20min钟时可能是使用了催化剂
C.从曲线变化可以看出,反应进行至25min钟 时,分离出0.1mol的氨气
D.在25min钟时平衡正向移动但达到新平衡后
NH3的体积分数比原平衡小
16.已知五种短周期元素的原子半径及主要化合价(最高正价、最低负价)如下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列叙述正确的是
A.T的原子叙述最小
B.相同条件下,L、M的单质分别与稀盐酸反应速率:M>L
C.T、Q的氢化物常温常压下均为无色气体
D.M的最高价氧化物可用作耐火材料
二、非选择题:(52分)
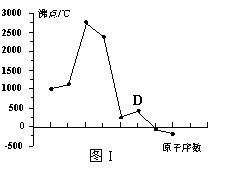 17.(8分) 原子序数依次增大的A、B、C、D四种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多,D所在周期的各元素单质沸点变化如图I(原子序数按递增顺序连续排列)。B、C、D三种元素均能与A形成等电子的三种分子,且化合物中各原子的个数比为:
17.(8分) 原子序数依次增大的A、B、C、D四种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多,D所在周期的各元素单质沸点变化如图I(原子序数按递增顺序连续排列)。B、C、D三种元素均能与A形成等电子的三种分子,且化合物中各原子的个数比为:
| 化合物 | 甲 | 乙 | 丙 |
| 原子个数比 | B∶A=1∶3 | C∶A=1∶2 | D∶A=1∶2 |
⑴元素D在元素周期中的位置 。
⑵B、C形成的一种化合物X是一种原子晶体,晶体中B、C原子均达到稳定结构,则X的化学式为 ;X的熔点 金刚石(填“大于”、“等于”或“小于”)。
⑶写出图I中沸点最高的单质与NaOH溶液反应的离子式 。
17.⑴第三周期第VIA族(2分)
⑵C3N4(2分) 大于(1分)
⑶2Al+2OH-+2H2O=2AlO2-+3H2↑(3分)
18.(10分).下表列出了前20号元素中的某些元素性质的有关数据:
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
试回答下列问题:
(1)以上10种元素形成的单质中,与水反应最剧烈的金属是 (填写编号)。
 (2)上述⑤、⑥、⑦三种元素中的两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质的化学式为 、 。
(2)上述⑤、⑥、⑦三种元素中的两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质的化学式为 、 。
(3)某元素R的原子半径为1.02×10-10m,该元素是 ;化合物Na2R2的电子式为_____________________。
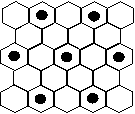
(4)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为 。
18.(10分)(每空2分)
(1)②
![]() (2)PCl3、CCl4
(2)PCl3、CCl4
(3)S (或硫)
(4)KC8
19.(12分)实验是化学的最高法庭。以镁条、铝片为电极,以稀NaOH溶液为电解质溶液构成的原电池,人们普遍认为铝是负极。某研究性学习小组为探究该原电池究竟谁是负极,发生怎样的电极反应,进行了如下实验:
如图,剪取约8cm的镁条及大小相近的铝片,用砂纸去膜,使镁条与铝片分别与量程为500μA的教学演示电表的“-”、“+”端相连接,迅速将两电极插入盛有1mol/LNaOH 溶液的烧杯中。开始,电表指针向右偏移约500μA,铝片表面有许多气泡,很快电流逐渐减小至0;随后,指针向左偏移,且电流逐渐增大至约400μA,此时,铝片表面气泡有所减少,但镁条表面只有极少量的气泡产生。根据以上实验现象,回答下列问题:
溶液的烧杯中。开始,电表指针向右偏移约500μA,铝片表面有许多气泡,很快电流逐渐减小至0;随后,指针向左偏移,且电流逐渐增大至约400μA,此时,铝片表面气泡有所减少,但镁条表面只有极少量的气泡产生。根据以上实验现象,回答下列问题:
(1)开始阶段,原电池的正极是_______(填“Mg”或“Al”)片;铝片表面产生的气泡是__________;负极发生的反应是 。
(2)随后阶段,铝片发生的电极反应式是______________________________;镁条表面只有极少量的气泡产生,其原因之一是:2H2O+2e-=H2↑+2OH-(极少),试判断此电极发生的主要反应是:_________________________________________________________;铝片表面气泡有所减少,但未消失,产生这一现象的可能原因是 。
19.(12分)
(1)Al (2分) H2 (2分)
Mg+2OH--2e-=Mg(OH)2(2分)若写成:Mg-2e-=Mg2+ 得1分
(2)Al+4OH--3e-=AlO2-+2H2O (2分) O2+2H2O+4e-=4OH- (2分) 铝片中含有杂质,构成原电池。(2分)
11.(6分).在室温下,将表面积相同、纯度相同、体积也相同的同种锌片分别投入等体积0.1mol/L的稀硫酸和0.2mol/L的稀盐酸中,仔细观察后发现,两者反应速率有明显差异,投入到稀硫酸中的锌表面产生的气泡没有投入到稀盐酸的快,运用你所学过的知识分析产生这一现象的原因可能是什么,并设计实验来证明你的推论是正确的。
答案:两者反应的本质都是锌与溶液中的氢离子发生的氧化还原反应,氯离子可能是这一反应的正催化剂或硫酸根离子是这一反应的负催化剂。
实验设计:向锌和硫酸反应的试管中滴加氯化锌溶液(其他溶液不可),若反应速率加快了,则说明氯离子是反应的正催化剂。或向锌与盐酸反应的试管中滴加硫酸锌(其他溶液不可),若反应率减慢了,说明硫酸根离子是该反应的负催化剂。
 19.(8分)20世纪80年代日本科学家应用电子计算机模拟出结构类似于C60(分子结构如右图所示)的物质N60,计算机模拟结果显示,N60与C60有相似的结构但稳定性较差。科学家预测,将N2进行冷冻或加压,然后运用高强度激光照射能转变为N60分子团,该分子团具有极强的挥发性,在受热情况下瞬间分解为N2并释放出大量的能量。
19.(8分)20世纪80年代日本科学家应用电子计算机模拟出结构类似于C60(分子结构如右图所示)的物质N60,计算机模拟结果显示,N60与C60有相似的结构但稳定性较差。科学家预测,将N2进行冷冻或加压,然后运用高强度激光照射能转变为N60分子团,该分子团具有极强的挥发性,在受热情况下瞬间分解为N2并释放出大量的能量。
已知E(N-N)=167kJ・mol-1,E(N=N)=418kJ・mol-1,E(N≡N)=942kJ・mol-1。(E表示键能,即打开1mol气态化学键所需要的能量)
回答下列问题:
⑴ N60分子中每个N原子最外层有 个电子;
⑵ N60稳定性较差的原因可能是 ;
⑶ 1molN60受热分解为N2时放出的热量为 ;
⑷ N60潜在的商业用途可能是 。
19.(8分)⑴ 8 ⑵ N-N的键能较小 ⑶ 13 230kJ ⑷ 用作高能量的炸药或火箭燃料
25.
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,
K值大小与温度的关系是:温度升高,K值______________(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) ![]() CO2(g)十H2 (g) △H<0
CO2(g)十H2 (g) △H<0
CO和H2O浓度变化如下图,则 0―4min的平均反应速率v(CO)=______ mol/(L・min)
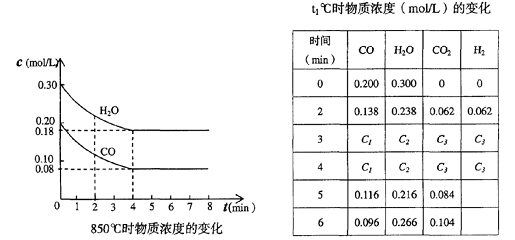
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min―4min之间反应处于_________状态;
C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min―5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min―6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
25.(本题共8分)
(1) 可逆反应的进行程度越大 可能增大也可能减小
(2) 0.03
(3) ①平衡 > ②d a