高三化学12月份月考试题
命题: 张燕 审核: 王国培 总分150分
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 K 39 Cr 52 Fe 56 Cu 64 I 127
第Ⅰ卷(选择题 共64分)
一、单项选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1.历史表明:没有新材料的出现,就没有科技和生产发展的突破。信息高速公路的建立在于寻找新的信息材料。下列材料可作信息材料的是
A.铜线 B.化纤 C.橡胶 D.光导纤维
2.亚硝酸盐中毒,又名乌嘴病、紫绀病、肠源性青紫病。亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法不正确的是
A.在中毒过程中血红蛋白被氧化 B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性 D.解毒时血红蛋白被还原
3.简单原子的原子结构可用下图形象地表示:
![]()
其中![]() 表示质子或电子,
表示质子或电子,![]() 表示中子,则下列有关①②③的叙述正确的是
表示中子,则下列有关①②③的叙述正确的是
A.①②③互为同位素 B.①②③为同素异形体
C.①②③是三种化学性质不同的粒子 D.①②③具有相同的质量数
4.被誉为“太空金属”的钛,在室温下,不与水、稀硫酸、稀盐酸和稀硝酸作用,但易溶于氢氟酸,其原因可能是
A.氢氟酸的酸性比其它酸强 B.氢氟酸的氧化性比其它酸强
C.氢氟酸的还原性比其它酸强
D.钛离子易与氟离子形成可溶性难电离物质
5.组成为![]() 的烷烃有九种,其中仅能由一种单烯烃加氢而制得的有
的烷烃有九种,其中仅能由一种单烯烃加氢而制得的有
A.1种 B.2种 C.3种 D.4种
6.某无色气体可能含有H2S、SO2、CO2、HI、HCl气体中的一种或几种。将气体通入氯水后得无色溶液,向该溶液中滴加氯化钡溶液产生白色沉淀。则下列叙述正确的是
A.该气体中肯定含有SO2 B.该气体中肯定含有H2S和SO2
C.该气体中肯定含有CO2和SO2 D.该气体中肯定含有H2S、CO2和HI
7.下列褪色过程不是因为氧化还原反应而褪色的是
A.SO2气体通入到溴水中使溴水褪色。
B.氯水使滴有酚酞的NaOH溶液褪色,加入NaOH后不变红。
C.将SO2气体通入到滴有酚酞的NaOH溶液中,溶液褪色。
D.在含有碘单质的淀粉溶液中,加入KOH溶液后蓝色褪去。-
8.将a g Fe2O3、Al2O3样品溶解在过量的200 mL pH=1的硫酸溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+ 刚好完全沉淀,用去NaOH溶液100 mL,则NaOH溶液的浓度为
A.0.1 mol·L-1 B.0.2 mol·L-1 C.0.4 mol·L-1 D.0.8 mol·L-1
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
![]() 9.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS)。已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是
9.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS)。已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是
A.羰基硫属于非极性分子 B.羰基硫的电子式为:
C.羰基硫沸点比CO2低 D.羰基硫分子中三个原子处于同一直线上
10.下列实验不能达到预期目的的是
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | 测定同浓度Na2CO3、Na2SO4两溶液的pH | 比较碳、硫的非金属性强弱 |
| D | 用同一电路测定等浓度的盐酸、醋酸两溶液的导电性 | 比较盐酸、醋酸的酸性强弱 |
11.下列离子方程式书写正确的是
A.将6molCl2通入含有5molFeI2的溶液中:
6Cl2+2Fe2++10I-= 12Cl-+5I2+2Fe3+
B.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl溶液等体积混合均匀:
4AlO2-+ 7H+ + H2O = 3Al(OH)3↓+ Al3+
C.向次氯酸钙溶液中通入少量二氧化硫:
Ca2++2ClO-+SO2+H2O = CaSO3↓+2HClO
D.电解饱和MgCl2溶液:2Cl‑+2H2O = 2OH-+H2↑+Cl2↑
12.关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入NaOH溶液并微热,生成使湿润的蓝色石蕊试纸变红的气体,可确定有NH4+存在
B.加入Ba(NO3)2溶液生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42‑存在
C.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32-
13.A、B、C、D为原子序数依次增大的同周期的短周期元素。已知A、C、D三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。下列判断正确的是
A.A、C、D三种元素最高价氧化物对应水化物有两种是强碱、一种是强酸,或两种是强酸、一种是强碱
B.A、C、D三种元素有两种是金属、一种是非金属
C.D元素在第三周期第ⅥA族
D.A、B、C三种元素的单质熔、沸点依次降低
14.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是
A.物质HClO4的氧化性大于HClO3
B.变蓝的淀粉碘化钾试纸褪色可能发生的反应:
5C12+I2+6H2O=12H++10Cl—+2IO3—
C.若化学计量数a=8,b=3,则该反应转移电子数为20e—
D.氯酸分解所得O2和C12的物质的量之比是确定不变的
15.两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42-,若将2.83 g X中的Cr3+全部氧化为Cr2O72-后,溶液中的
Cr2O72-可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为:
Cr2O72-+6I-+14H+=2 Cr3++3I2+7H2O 。若向溶有2.83 gX的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀.由此可推断出X的化学式为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
16.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
|
| 2.24L | 3.36L | 3.36L |
A.盐酸的物质的量浓度为3.0 mol·L-1
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量 D.15.7g混合物恰好与盐酸完全反应
第二卷(非选择题 共86分)
三、(本题包括2小题,共18分)
17.(6分)下列实验操作或对实验事实的描述不正确的是____________ (填序号,错选一个倒扣2分,不出现负分)
A.用分液漏斗进行分液操作,将甘油和水的混合物分离;
B.从溴的四氯化碳溶液中提取溴,可用苯进行萃取;
C.用热的浓HCl洗涤附着有MnO2的试管;
D.在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高 ;
E.用碱式滴定管量得KMnO4溶液20.50mL ;
F.实验室快速制备少量H2、O2、NH3、HCl可以用同一种气体发生装置;
G.只用水一种试剂就能将CuSO4、Na2CO3、CaC2三种固体粉末鉴别;
H.用NaOH溶液和FeSO4溶液制备Fe(OH)2时,吸有NaOH溶液的胶头滴管末端应插入FeSO4溶液液面之下;
18.(12分)某研究性学习小组研究HNO3的氧化性,设计了如下实验:
在盛有新制FeSO4溶液的试管中滴入2滴KSCN溶液,观察现象,然后再滴入几滴浓HNO3,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色快速变为蓝色,并产生红棕色气体,这一奇特现象激起了同学的好奇心与求知欲望,对此现象设计了探究性实验。
⑴甲同学认为是溶液中的Fe2+的干扰造成的,大家经过理性分析,认为可以排除Fe2+的干扰,理由是________________________。
⑵乙同学认为红色消失,说明Fe(SCN)3被破坏,红棕色NO2说明了某些离子与HNO3发生了氧化还原反应,推测可能是KSCN与HNO3作用。KSCN溶液是一种无色液体,根据C、S、N的原子结构和共价键的相关知识推测SCN-的结构式为____________。
⑶根据乙同学的观点,设计了实验方案1,往浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色,突然剧烈反应产生大量气泡,放出红棕色气体,而溶液红色消失变为浅绿色,溶液温度升高;继续滴入KSCN,溶液变为浅蓝色,最后变成无色。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种非极性气体;向反应后的溶液中加入BaCl2溶液产生白色沉淀,写出向浓HNO3中滴入KSCN的离子方程式______________________。
⑷丙同学认为SCN-的性质还可进一步探究,设计了方案2,向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均消失变为黄色,而加入碘水时溶液的颜色基本不变。丙同学的设计意图是____________________________。
⑸通过本次探究,可以得出以下结论,a、用SCN-间接检验Fe2+时应注意________;b、与SCN-反应使溶液变红的_______是Fe3+。(填“一定”或“不一定”)
四、(本题包括2小题,共24分)
19.(12分)A、B、C、D、E分别属于周期表中前20号元素,其原子序数依次递增,并且其中只有一种金属元素。A是元素周期表所有元素中原子半径最小的;B和C都只有两个电子层,B中一层电子数是另一层的两倍;C中两层电子数之和是两层电子数之差的两倍;D中一层电子数是另两层电子数之和;E的正二价阳离子电子层结构与氩原子相同。
请按要求回答下列问题:
⑴画出E原子的原子结构示意图 ,写出由A和C组成的含有非极性键的化合物的电子式 。
⑵由上述元素组成的化合物中属于极性键构成的非极性分子是
(只要求写出两种,用化学式表示)。
⑶由C与E形成的化合物高温时与单质B反应生成两种化合物,请写出该反应的化学方程式 。
⑷写出上述元素形成的化合物或者单质中:①一种可溶性的正盐与另一种强酸反应的离子方程式 ;②上述元素形成的化合物中通常能污染空气的是 (至少写出两种)。③某一种可污染空气的化合物与强氧化性单质常温下反应生成两种化合物,该反应的化学方程式为 。
20.(12分)物质之间的转化关系如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,X的水溶液为一种常见的医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见氮肥,且反应⑦中L与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素。
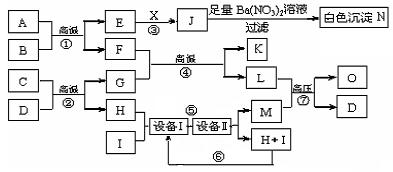
回答下列问题:
⑴X的化学式为 ,O的结构简式为 。
⑵考虑到综合经济效益,工业生产M时,可采取的措施有 (填序号)。
a.使用催化剂 b.适当降低温度 c.选择合适的温度 d.适度增大压强 e.及时分离出产物 f.对原料进行循环利用 g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 j.工厂地址可选择在盛产天然气的地区
工业生产中为了节约资源、降低成本和保护环境,常常对某些物质进行循环利用。上述转化关系中能达到该目的的是 (填序号)。
⑶反应②化学反应方程式为 。
⑷现有1molA参加反应,假设各步均完全反应,生成N的质量为1165g,生成K的质量为224g,则反应①化学反应方程式为 。
五、(本题包括3小题,共26分)
21.(6分)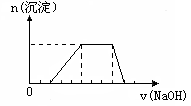 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_________(由少到多排列),且各离子的物质的量之比为_______;肯定不含的阳离子是_______________。
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_________(由少到多排列),且各离子的物质的量之比为_______;肯定不含的阳离子是_______________。
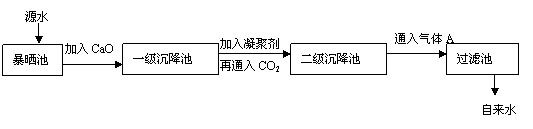 22.(10分)某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:
22.(10分)某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:
⑴源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成Ca(OH)2,进而发生若干复分解反应,试写出其中的一个离子方程式 。
⑵加入凝聚剂可以除去其中的悬浮固体颗粒,其过程是 。(填写下列各项的序号)①只有物理过程,无化学过程 ②只有化学过程,无物理过程
③既有化学过程又有物理过程;
FeSO4·7H2O是常用的凝聚剂,加入后,最终生成红褐色胶状沉淀,则这种红褐色胶状沉淀是 。用化学反应方程式表示实验室制备该胶体的方法: 。
⑶通入二氧化碳的目的是 和 。
⑷气体A的作用是 。
⑸下列物质中, 可以作为气体A的代替品。(填写下列各项的序号)
①ClO2 ②浓氨水 ③SO2 ④浓硫酸
23.(10分)已知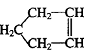 可简写为
可简写为
降冰片烯的分子结构可表示为: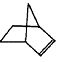
⑴降冰片烯属于__________。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
⑵降冰片烯的分子式为__________。其二氯取代物共有 种。
⑶写出降冰片烯的所有含有一个六元环的单环化合物的同分异构体的结构简式 。
⑷降冰片烯不具有的性质__________。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
六、计算题(本题包括2小题,共18分)
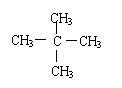
24.(8分)某烃0.1mol与0.7mol氧气混合后,在一密闭容器中充分燃烧。所得产物通过浓硫酸时,浓硫酸增重10.8g,再通过灼热氧化铜粉末,固体质量减轻3.2g,最后通过足量的过氧化钠粉末时,固体质量又增加了14.0g。试通过计算确定该烃的分子式;写出其一氯代物只有一种的结构简式并用系统命名法命名。
25.(10分)铜是人类最早知道的金属之一,实验室可用H2还原CuO制取少量的Cu,工业上主要用火法从黄铜矿中提炼Cu。
Ⅰ、实验表明,CuO被H2还原时也有Cu2O生成。将一定量的H2缓慢通过灼热的CuO粉末,得到固体混合物且混合物中m(Cu) ∶m(O)=8∶a。当a有不同的取值时,固体混合物成份不同。请分析a的取值范围和固体混合物成份的关系并填入下表(不一定填满,表格不够也可自行增加);
| a的取值范围 | 反应后固体的成分(用化学式表示) |
Ⅱ、 黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀释至 2.12 L时测得其pH为0;将稀释后的溶液分为两等份,向其中一份溶液中滴加6.05mol/L的NaOH溶液,向另一份溶液中滴加0.600mol/L Ba(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶液的体积变化如下图所示:
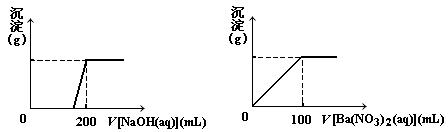
⑴ 请通过计算确定m的值;
⑵ X的摩尔质量为368 g/mol,请确定X的化学式。
高三化学参考答案
一、二、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | D | B | A | D | B | A | C | B |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | BD | B | AB | C | B | BC | C | BD |
17.ABE(6分,选对一个得2分,错选一个倒扣2分,不出现负分)
18.(12分)⑴如果是亚铁离子干扰,不可能变红之后,一段时间之后变成蓝色
⑵![]()
⑶![]()
⑷比较硫氰根离子与氯离子、溴离子、碘离子的还原性强弱
⑸a、加入氧化剂如氯气等必须少量 b、不一定
19.(12分,每空2分) 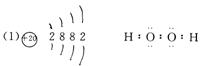 ⑵CH4 、 CO2、CS2
⑵CH4 、 CO2、CS2
⑶CaO+3 C ![]() CaC2+CO↑
CaC2+CO↑
![]()
③H2S+O3=SO2+H2 O
20.(12分)⑴H2O2 ![]() ⑵acdefgj C +2H2O
⑵acdefgj C +2H2O![]() CO +H2 ⑥
CO +H2 ⑥
⑶Fe4S5+8O2![]() 2Fe2O3+5SO2
2Fe2O3+5SO2
21 (6分).Al3+ H+、 NH4+、; 1:2:3 ; Fe3+ 、 Mg2+ (各2分)
22.(共10分,第一空2分,其它每空1分)
⑴只要写出下列4个离子方程式中的任意一个,即可给2分。
![]()
![]() HCO-3+OH- CO2-3+H2O;Ca2++CO32-+OH- CaCO3↓+H2O;
HCO-3+OH- CO2-3+H2O;Ca2++CO32-+OH- CaCO3↓+H2O;
![]() Ca2++2HCO-3+2OH- CaCO3↓+CO32-+2H2O;
Ca2++2HCO-3+2OH- CaCO3↓+CO32-+2H2O;
![]() Mg2++2OH- Mg(OH)2↓
Mg2++2OH- Mg(OH)2↓
⑵③;Fe(OH)3 ⑶除去钙离子;调节溶液酸度
⑷杀菌消毒或氧化性 ⑸①
23.(10分)⑴a、b ⑵C7H10 15 种 ⑶ ![]() 等共5种 ⑷a、d
等共5种 ⑷a、d
 |
|
25.(10分)Ⅰ、
| a的取值范围 | 混合物组成(用化学式表示) |
| 1<a<2 | CuO、Cu2O |
| 0<a<2 | CuO、Cu2O、Cu |
| 0<a<1 | Cu2O、Cu |
Ⅱ、
⑴ 解:依题意,m g X中:n(Cu)∶n(Fe)=1∶1
2n(Cu2+) +3n(Fe3+) =6.05mol·L-1×0.2L×2-1 mol·L-1×2.12L
故:n (Cu) = n (Fe) = 0.06mol
又,n (S) = 0.6mol·L-1×0.1L×2 = 0.12mol
因此,m g = m(Cu) + m(Fe) + m(S)
= 0.06mol×64g·mol-1+0.06mol×56g·mol-1+0.12mol×32g·mol-1
= 11.04g
即m 的值为11.04
⑵ 解:设X的化学式为(CuFeS2)n,则
(64+56+32×2)×n = 368
n = 2 故X的化学式为Cu2Fe2S4