������ѧ12���¿��Ծ�
����ѧ��������
����ʱ��:90���ӡ������� ����:100�֡������������� 2006.12.31
�����õ������ԭ��������H:1 ��C:12�� N:14 ��O:16 Na:23 ��Al��27�� S:32
Cl:35.5��K:39�� Ba:137
�� �ڢ����ѡ���� ��40�֣�
һ��ѡ���⣨���20С�⣬ÿС��2�֣���40�֣�ÿС��ֻ��һ����ȷѡ���
1��������Һ�ܹ����������������ǡ�������
A���Ȼ�����Һ��������B. ������Һ������ C. �ƾ���Һ������D. ���������Һ
2�������й�O3 ��˵�����������ǡ�������
A��O3��O2��Ϊͬ�������塡������������ B. O3 ����ǿ�����ԣ�����������
C����ͬ������O3��O2������ͬ�ķ������� D. ������O3���ߣ��������к�
3����֪25���101kPa�£�1gC6H14�����飩ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�48.41kJ����������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ���ǡ�������������������������������������������������������
������ A��C6H14��1��+![]() O2(g)====6CO2(g)+7H2O(1)�� ��H= ��48.4kJ/mol
O2(g)====6CO2(g)+7H2O(1)�� ��H= ��48.4kJ/mol
������ B��C6H14��1��+![]() O2(g)====6CO2(g)+7H2O(g)�� ��H= + 4163kJ/mol
O2(g)====6CO2(g)+7H2O(g)�� ��H= + 4163kJ/mol
������ C��C6H14��1��+![]() O2(g)====6CO2(g)+7H2O(1)�� ��H= + 48.4kJ/mol
O2(g)====6CO2(g)+7H2O(1)�� ��H= + 48.4kJ/mol
������ D��C6H14��1��+![]() O2(g)====6CO2(g)+7H2O(1)�� ��H=��4163kJ/mol
O2(g)====6CO2(g)+7H2O(1)�� ��H=��4163kJ/mol
4����2CH4(g) + 2NH3(g)
+ 3O2(g) ![]() 2HCN(g) + 6H2O(g)��Ӧ�У�
2HCN(g) + 6H2O(g)��Ӧ�У�
��֪v (HCN) = n mol/(L��min)����v(O2) = m mol/(L��min)
��m��n�Ĺ�ϵ��ȷ���ǡ�������
����A��m =![]() n�������� ��B��m =
n�������� ��B��m =![]() n������������
C��m
=
n������������
C��m
=![]() n������������ D��m = 2n
n������������ D��m = 2n
5�������£���0.1mol��L-1�����0.06mol��L-1����������Һ�������Ϻû����Һ��pH�ǡ�������
�� A��1.7�������� B��12.3�������� C��12������������ D��2
6������ʵ������ᵼ��ʵ����ƫ�ߵ��ǡ�������
A������0.1 mol��L-1NaCl��Һʱ������ʱ���ӿ̶���
B���ⶨ����ͭ����ᾧˮ������ʵ���У����ȷֽ�����Ʒ���ڿ�������Ȼ��ȴ
C����NaOH��Һ�ζ�δ֪Ũ�ȵ�����ʱ����ƿδ�ô�װ��������ϴ
D����pH��ֽ�ⶨ�����pHʱ��������������ˮϴ�Ӻ�δ����
7�����ж�ʵ���ұ����Լ��ķ�����������ȷ���ǡ�������
������ A���ù���Լ�ƿʢ���壬ϸ���Լ�ƿʢҺ��
������ B��Ϊ�˱���������Ӵ��������Ľ����ƺͰ���ͨ����������ú���б���
������ C��Ũ�����Ũ����ḯʴ������ĥɰ������������ô���Ƥ�����Լ�ƿ����
������ D��Ϊ������������ˮ�⣬ʵ���ұ�����Ȼ�����Һ���������ữ
![]() 8��dz��ɫ��Fe(NO3)2��Һ�д�������ƽ�⣺Fe2++2H2O������Fe(OH)2+2H+�������������Һ������Һ����ɫ��������������������
8��dz��ɫ��Fe(NO3)2��Һ�д�������ƽ�⣺Fe2++2H2O������Fe(OH)2+2H+�������������Һ������Һ����ɫ��������������������
������ A����ɫ����������� B����ø�dz������������ C�����ɫ�������������� D������ɫ
9�������ʵ����ʵ���Ũ�Ⱦ�Ϊ0.1 mol �� L �C 1�İ�ˮ������������Һ���ֱ�͵����
pH = 2�����ᷴӦ��������ǡ�ñ���ȫ�к�ʱ�����İ�ˮ������������Һ������ֱ���V1��V2����V1��V2�Ĺ�ϵ��ȷ���ǡ�������
������ A��V1 < V2 �������������� B��V1 = V2����������������������C��V1 > V2 �������������������� D��V1��V2
10����������������ԭ�ӣ�һ�����ڷǽ���Ԫ�ص�ԭ�ӵ��ǡ�������
������ A����������������4�������������������������� B������������Ӧ��ˮ����Ϊ��
������ C���ڻ������п��Ը��ۡ������������� D�����пɱ�Ļ��ϼ�
11����NA ���������ӵ�������ֵ������˵����ȷ���ǡ�������
��������A�����³�ѹ�£�22.4 L��H2������ԭ����ĿΪ2NA
��������B��1.8g NH![]() ��������������ĿΪNA
��������������ĿΪNA
��������C��58.5 g NaCl�������������Ȼ��Ʒ�����ĿΪNA
������ D��1 L 1
mol/L Na2CO3��Һ��������CO![]() ������ĿΪNA
������ĿΪNA
12���������ӷ���ʽ��д��ȷ���ǡ�������������������������
�������� A��������Һ������������Һ��Ӧ��ʹSO42��ǡ����ȫ������
��������Al3++2SO42��+2Ba2++3OH��====2BaSO4��+Al(OH)3��
B����FeBr2��Һ��ͨ�����������
2 Fe2+ + Cl2
![]() 2Fe3+
+ 2Cl��
2Fe3+
+ 2Cl��
�������� C���ò��缫���MgCl2��Һʱ�����ķ�Ӧ��
��������2Cl��+2H2O![]() Cl2��+H2��+2OH��
Cl2��+H2��+2OH��
�������� D�������½��������Һ��KOH��Һ��ϣ� NH4++OH��====NH3��H2O
13����pH=2�Ĵ����pH=12��NaOH��Һ�������ϣ�������Һ������Ũ�ȹ�ϵ��ȷ���ǡ�������
A��c(CH3COO��)��c��Na+����c(H+) ��c(OH��)��
B��c(Na+)��c(CH3COO��)��c(H+)��c(OH��)
C��c(CH3COO��)��c��Na+����c(OH��)��c��H+��
D��c��Na+����c(CH3COO��)��c(OH��)��c(H+)
14��t��ʱ��100g�������Ƶı�����Һ�м���6.2g�����ƣ���ַ�Ӧ��ָ���t��, ����������ȷ���ǡ���������������
A�������������ʵ���������8g���������� B����Һ��pH���
C��������Һ������Ϊ98.2g������������ D����Һ��Na+ Ũ�ȱ��
15��ˮ��Һ�е�Xn+��Ym+��Zn-�������ӣ���֪m>n����X��Y��Z����ԭ�ӵ�M���������Ϊ����������˵���в���ȷ���ǡ�������
A������Ԫ�ص�����������������Ӧˮ����֮����������Ӧ
B��Ym+���ӵİ뾶��С��
C��YԪ��һ���ǽ���Ԫ��
D��ԭ�Ӱ뾶Z>X>Y��
16�����ݻ�������ܱ������д������·�Ӧ��2SO2(g)��O2(g)
![]() 2SO3(g)����H��0
2SO3(g)����H��0
ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ���ǡ�������
A��ͼI�о�����t0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
B��ͼII�о�����t0ʱ�̼��������Է�Ӧ���ʵ�Ӱ��
C��ͼIII�о����Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ�
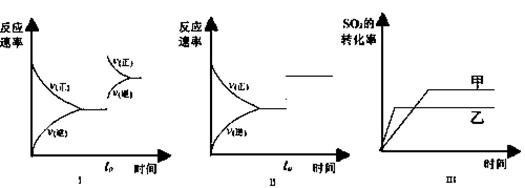 D��ͼIII�о������¶ȶԻ�ѧƽ���Ӱ�죬�Ҽ��¶Ƚϸ�
D��ͼIII�о������¶ȶԻ�ѧƽ���Ӱ�죬�Ҽ��¶Ƚϸ�
17��Ϊ֤��ij������һԪ�ᣨHX�������ᣬͬѧ�����������ʵ�鷽�����������������ǡ�������
A�������£���0.1mol/L HX��Һ��pH ����pH��1��֤��HX������
B�������£���1mol/L NaX��Һ��pH ����pH��7��֤��HX������
C������Ũ�ȡ��������HCl��NaX��Һ��ϣ��������ҺpH��7��֤��HX������
D������ͬ�����£���0.1 mol/L��HCl��0.1mol/L��HX���е�����ʵ�飬��HX��Һ���ݽϰ���֤��HXΪ����
18��������ػ�ѧԭ���������ж���ȷ���ǡ�������
A����X��ԭ�Ӿ��壬Y�Ƿ��Ӿ��壬���۵㣺X��Y
B����A2��2D����2A����D2���������ԣ�D2��A2
C����R2����M+ �ĵ��Ӳ�ṹ��ͬ����ԭ��������R��M
D��������HA������ǿ������HB����ͬŨ��������Һ�ļ��ԣ�NaA��NaB
19��һ������ȼ�ϵ�أ����Զ������Ϊ�缫����KOH��Һ�У�Ȼ��ֱ���������ͨ�������������缫��ӦʽΪ��CH4+10OH����8e��=CO32��+4H2O
����4H2O+2O2+8e��====8OH���йش˵�ص��ƶ���ȷ���� ��������
������ A��ͨ����ĵ缫Ϊ����
������ B����ҺpH������
������ C���ŵ�һ��ʱ���KOH�����ʵ���Ũ�Ȳ���
..... D���μӷ�Ӧ��O2��CH4�����ʵ�����Ϊ4:1
20���ø���ĸ�����ؿ����Ƶü����������������KMnO4��MnO2��K2O��O2��240�棩������˵������ȷ���ǡ�������
A��ÿ����11��2 L����ת����2 mol����
B����ͬ������KMnO4�ֽ⣬��������MnO2�ķ�Ӧ������K2MnO4�ķ�Ӧ�ų���������
C��O2���������MnO2�ǻ�ԭ����
D���ڴ������£�KMnO4��������ǿ��O2
![]()
 ����12���¿�
����12���¿�
�� ѧ �� ��
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� |
|
|
|
|
|
|
|
|
|
|
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� |
|
|
|
|
|
|
|
|
|
|
�ڢ������ѡ���� ��60�֣�
�������������3С�⣬��32�֣�
21����12�֣�������A��B��C��D��E��F��G��H 8��Ԫ�������ڱ���λ�á�
 |
�ݴ˻ش��������⣺
��1����������ǿ���ǣ���Ԫ�ط��ţ����� �������ڹ���Ԫ�ص��ǣ���Ԫ�ط��ţ����� ��
��2��A��C��Ԫ���γɵĻ������к��зǼ��Լ����ǣ�д����ʽ���������� �� ��
D��C��Ԫ�ذ�ԭ�Ӹ����� 1:1 �γɵĻ����������������� �����
�����ʽΪ���������������� ��
��3��������Ԫ����������Ԫ���γɵĻ������У����ڷǼ��Է��ӵ��ǣ�ֻд������������������ ������������ �� ��
��4��A�ֱ���B��C��E��F�γɵ����ֻ�����Ĺ�̬���������� ���� ����д�����Ӿ��塢ԭ�Ӿ������Ӿ��塱�����侧��������������������� ����д����ʽ��
��5����A��C�γɵ�һ�ֻ�������C��E�γɵ�һ�ֻ�������Է���������ԭ��Ӧ������һ��ǿ�ᣬ��д����ѧ��Ӧ����ʽ��
���������������������������������������������������������� ��
���÷�Ӧ����0.5mol��ǿ������ʱ����Ӧ�б���ԭ������������������ g��
22��(12��)�ס��ҡ�����������ֱ���Na2SO4��Ba(NO3)2��HNO3��BaCl2��NaOH������Һ�е�һ�֣�������X��Һ�������ǣ���֪����B���ܶ���ͬ��ͬѹ���������ܶȵ�22�����Ը�����ͼ�е�ת����ϵ�ش����⣺
 |
��1���������ʵĻ�ѧʽ�ֱ�Ϊ��
������ ������������ �� ���������� ������������ ������������ ��X�������� ��
��2����ɫ����A���ҷ�Ӧ�����ӷ���ʽΪ���������������������������������� ��
23��(8��)����ͼ��ʾ��װ�ã�C��D��E��F��X��Y���Ƕ��Ե缫��
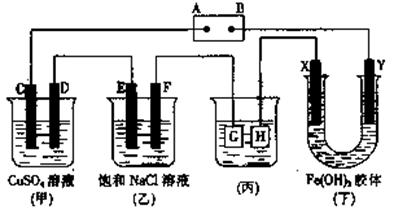 |
����Դ��ͨ�������е����̪Һ����F�������Ժ�ɫ���Իش��������⣺
��1����ԴA����������_______��
��2����װ���е�ⷴӦ���ܷ�Ӧ���ӷ���ʽ�ǣ�____________________________________�������������������������� ��
��3������ռ���װ���в��������壬����������������______________��
��4�����ñ�װ�ø�ͭ��һ������GӦ����_______(�ͭ��������)�����Һ����Ҫ�ɷ���________________(�ѧʽ)��
��5��װ�ö��е�������_________________________________�������� _____��
˵��___________________________________�� ������������
�������������1С�⣬��12�֣�
24����12�֣�ijУ��ѧС��ѧ������ͼ12װ�ý��С����Ĵ��������������֤��ʵ�顣��ͼ�мг�װ������ȥ��
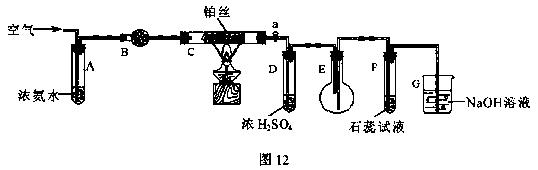
��1��װ��B��ʢ�ŵ��Լ���__________�������ƣ����������ջ�������е�ˮ����
��2����Ӧ��ʼʱ����װ��C�в�˿���ȵ����ȣ���ȥ�ƾ��ƣ���˿�䰵����ʱ�����������˿�ֱ���ȡ�������Ϊ���Ĵ�������_________��Ӧ��
��3��ʵ������У�װ��D�еĵ�������������ɫ�����������Ϊ�˽�������⣬�����ڻ���a������______��ѡ����ţ���
��������ʢ������ˮ��ϴ��ƿ������ʢ��Ũ�����ϴ��ƿ������ʢ�м�ʯ�ҵ�U�ι�
��4����Ӧһ��ʱ���װ��E�е�������ɫӦΪ��������ɫ����ʱ��װ��E�еĺ�����������NH3��NO��NO2��___________���ѧʽ����
��5����Ӧһ��ʱ���װ��F�е���ɫʯ����Һ��죬��ԭ���ǣ�д����ѧ����ʽ��__________________________________________________��
��6��ʵ�����ʱ��Ӧ__________________________����ֹͣ���������
��7����ҵ�Ϻϳɰ��ķ�Ӧ�ǣ�N2(g)+3H2(g)![]() 2NH3(g)����H= -92.2kJ��mol-1��
2NH3(g)����H= -92.2kJ��mol-1��
�� �����������ܹ���߹�ҵ�ϳɰ�ת���ʵ���_________��ѡ����ĸ��
����a������ѹǿ���������������� b�������¶�
������ c��ʹ������ý������������ d�������ɵ�NH3��ʱ�ӻ�������з����ȥ
�� �ڹ�ҵ�ϳɰ�ʱ����500�����ҵ��¶ȣ���Ҫ����Ϊ��
____________________________________________________________�������� ��
�ġ����������2С�⣬��16�֣�
![]() 25����4�֣�
25����4�֣�
��1�������£���1mL pH = 1��H2SO4��Һ��ˮϡ����100mL ��ϡ�ͺ����Һ�С������� =
���� ���������������� ��
![]() ��2�������£�pH=5��H2SO4��Һ����ˮ�������H+Ũ��Ϊc1��pH=5 ��Al2(SO4)3��Һ����ˮ�������H+ Ũ��Ϊc2���� = ������������ ��
��2�������£�pH=5��H2SO4��Һ����ˮ�������H+Ũ��Ϊc1��pH=5 ��Al2(SO4)3��Һ����ˮ�������H+ Ũ��Ϊc2���� = ������������ ��
26����12�֣���һ���¶��½�2molA��2molB������������2L�ܱ������У��������·�Ӧ��
3A��g����B��g��![]() 2C��g����2D��g����2����ĩ��Ӧ�ﵽƽ��״̬��������0.8mol D������д����հס�
2C��g����2D��g����2����ĩ��Ӧ�ﵽƽ��״̬��������0.8mol D������д����հס�
��1��B��ƽ��Ũ��Ϊ���� �������� ��
��2��A��ת����Ϊ�������������� ��
��3����D��ʾ��ƽ����Ӧ����Ϊ���������������� ��
��4�������С�����ݻ����¶Ȳ��䣩����ƽ����ϵ�л��������ܶȡ�ƽ����Է�������__________��__________�������վ���������١����䡱 ��
��5�����������Ӧ����ͬ�����´��淴Ӧ��ʼ���У���ʼ��C��D��4/3 mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ����ȣ���Ӧ�������������� mol B���ʡ�