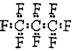高三年级化学第一次月考试题
化 学
一、选择题(每小题只有一个选项符合题意,每小题3分,共60分)
1.以下化学用语正确的是 ( )
|
C.明矾的化湛这式KALSO412H2O D.氯化钠的电子式Na
2.下列不符合当今化学研究方向的是 ( )
A.发现新物质 B.全成新材料
C.研究化学反应的微观过程 D.研究化学反应中原子守恒关系
3.在常温压下呈现气态的化合物,降温使其固化得到晶体属于 ( )
A.分子晶体 B.原子晶体 C.离子晶体 D.何种晶体无法判断
4.碱金属与卤素所形成的化合物大都具有的性质是 ( )
①高沸点;②能溶于水;③水溶液能导电;④低熔点;⑤熔融状态不导电。
A.①②③ B.③④⑤ C.①④⑤ D.②③⑤
5.2004年某一期的《美国化学杂志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成金刚石,具有深远意义。下列说法不正确的是 ( )
A.由二氧化碳合成金刚石是化学变化 B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠 D.金刚石中只含有非极性共价键
6.有关晶体的下列说法中正确的是 ( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
7.下列有关苯和溴苯的廉洁正确的是 ( )
A.它们所形成的晶体都属于分子晶体 B.苯的密度比溴苯的密度大
C.苯的沸点比溴苯的沸点高 D.苯与溴苯的分离可以采用分馏的方法
8.有关晶体的叙述中正确的是 ( )
A.在SiO2金刚石中,由Si、O构成的最小单元环为六元环
B.在12g金刚石中,含C―C共价键键数为4NA
C.干冰晶体熔化只需克服分子间作用力
D.金属晶体中全是由金属原子直接构成的
9.NaF,NaI,MGO均为离子晶体,现有下表所示数据,试判断这三种化合物熔点由高到低的正确顺序为 ( )
| 物质 | ①NaF | ②NaI | ③MgO |
| 离子电荷数 | 1 | 1 | 2 |
| 键长/(10-10m) | 2.31 | 3.18 | 2.10 |
A.①>②>③ B.③>①>② C.③>②>① D.②>①>③
10.根据相关化学原理,下列判断正确的是 ( )
A.若X是原子晶体,Y是分子晶体,则熔点:X<Y
B.若A2+2D-→2A-+D2,则氧化性D2>A2
C.若R2-和M+的电子层结构相同,则原子序数:R>M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB
11.已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序减小,B和E同主族,下列推断不正确的是 ( )
A.A、B、E一定在不同周期 B.D为第二周期
C.A、D可能在同一主族 D.C和D的单质可能化合为离子化合物
12.下面是一些常见分子的比例模型。其1个分子中只含2对共用电子对的是 ( )
|
A. B. C. D.
13.主族金属元素在化学性质上必然是 ( )
A.单质都能跟C12反应生成氯化物 B.氧化物都是碱性氧化物
C.化合态时只能以简单阳离子形式存在 D.单质都不与强碱溶液反应
14.下列分子中,所有原子的最外层均为8电子结构的是 ( )
A.BeCl2 B.H2S C.NCl3 D.SF6
15.下列关于元素周期表和元素周期律的叙述正确的是 ( )
A.元素的性质随着相对原子质量的递增,呈周期性的变化
B.周期表中,原子序数都等于该族元素原子的最外层电子数
C.第三周期,随着核电荷数的递增,元素的离子半径依次减小
D.随核电荷数的递增,ⅦA族元素的单质熔、沸点升高,碱金属元素单质熔、沸点降低
16.由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,C(Al3+)=0.4mol・L-1,c(SO42-) =0.8mol・L-1,则c(K+)为 ( )
A.0.15mol・L-1 B.0.2 mol・L-1 C.0.3 mol・L-1 D.0.4 mol・L-1
17.三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了八个电子的结构。在一个三硫化四磷分子中含有的共价键个数是 ( )
A.7个 B.9个 C.19个 D.不能确定
18.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳效率104倍的“超级温室气体”――全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是 ( )
|
B.全氟冰烷的电子式为:
C.相同压强下全氟丙烷的沸点比丙烷低
D.全氟丙烷分子中既有极性键又有非极性键
19.有关晶体的下列说法中正确的是 ( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
20.下列关于晶体的叙述中,不正确的是 ( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
|
21.有四组同族的物质,它们的沸点(℃,P=1.01×105Pa)如下表所示:
| ① | He -268.8 | Ne -249.5 | Ar (x) | Kr -151.7 |
| ② | F2 -187.0 | Cl2 -33.6 | (a) 58.7 | I2 184.0 |
| ③ | HF (y) | HC1 -84.0 | HBr -67.0 | HI -35.3 |
| ④ | H2O (z) | H2S -60.2 | (b) -42.0 | H2Te -1.8 |
试根据上表回答下列问题:
(1)b的分子式为 。
(2)写出②系列中物质主要化学性质的递变规律(任烈军属一种) ;能够说明该递变规律的化学事实是 (任举一例,用离子方程式表示)。
(3)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是 。
(4)上表中, 两种物质的沸点校同系列其它物质反常,反常的主要原因是
。
22.磷化氢俗称膦,是一种无色有大蒜气味的有毒气体,它由白磷与过量热的氢氧化钾的浓溶液反应产生:P4+3KOH+3H2O=PH3+3KH2PO2。
(1)写出磷化氢的电子式 。
(2)白磷跟氢氧化钾溶液反应时氧化剂是 、还原剂是 。KH2PO2属于 (填“正盐”或“酸式盐”或“碱式盐”)。
(3)白磷分子(P4)结构形状是 ,分子中键角是 ,属于 (填“极性”或“非极性”)分子。
|
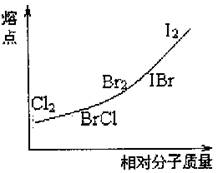
已知,卤素互化物BrCl能发生下列反应
H2O+BrCl=HBrO+HCl KBr+BrCl=KCl+Br2
(1)写出IBr的电子式 。
(2)写出KI与IBr反应的化学方程式
,该反应中的所有反应物和生
成物相比较,熔点最较高的物质是
(写化学式)。
(3)写出苯(C6H6)与BrCl发生取代反应生成一卤代物的化学方程式 。
(4)如图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图。它们的沸点随着相对分子质量的增大而升高,其原因是 。
|
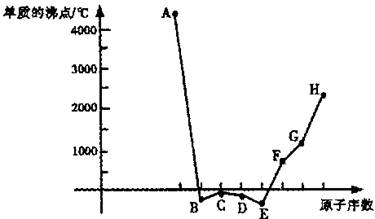
请回答:
(1)A~H八种单质中属于分子晶体的是 ,属于原子晶体有 ,属于金属晶体的有 。(都填化学式,全部写出才给分)
(2)上述元素的最高价氧化物的水化物中,碱性最强的是(写化学式) ;上述元素的气态氢化物中,最稳定的是(写化学式) 。
(3)D、F两元素能化合形成一种化合物,用电子式表示这种化合物的形成过程 。
(4)已知D、F、G三种元素的离子均具有跟Ne相同的电子层结构,则这三种离子的半径由大到小的次序为(用相关元素的离子符号表示) 。
三、共包含2小题(15分)
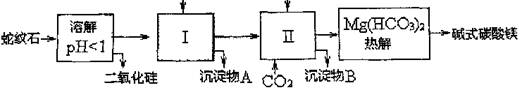
25.(11分)蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验上学骤如下
|
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 。
|
(有关氢氧化物沉淀的pH见右表)
Ca(OH)2不能过量,若Ca(OH)2
过量可能会导致 溶解、 沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料。先向沉淀物A中加入 (填入物质的化学式),然后 (依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以特环使用的物质是 (填写物质化学式)。
(5)现设计一个实验,确定新产品aMgCO3・bMg(OH)2・cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解 ③ ④ ⑤MgO称量
(6)18.2g产品完全分解后,产生6.6gCO2和8.0gMO 由此可知,产品的化学式中:
a= b= c=
26.(4分)称取0.200g硫某赤铁矿样品,矿样溶解后,使其中的铁全部转化成Fe2+(所得溶液中不含其他还原性物质)。另称7.90g硫酸铈铵2(NH4)2SO4・Ce(SO4)2・2H2O(摩尔质量为632g・mol-1),溶解后稀释至250mL。取该溶液30.0mL恰好与上述Fe2+溶液完全反应。反应的离子方程式为:Ce4++Fe2+=Ce3++Fe3+。请计算该矿样中Fe2O3的质量百分含量)(Fe2O3摩尔质量为160g・mol-1)。
参考答案
一、选择题(每小题只有一个选项符合题意,每小题3分,共60分)
1.B 2.D 3.A 4.A 5.B 6.B 7.A 8.C 9.B 10.D
11.B 12.C 13.A 14.C 15.D 16.C 17.B 18.D 19.B 20.B
二、本题共有4小题(每空1分,共25分)
21.(1)H2Se (2)氧化性逐渐减弱 Cl2+2Br-=2Cl-+Br2(其它合理答案也行)
(3)随着相以分子质量增大,沸点逐渐升高
|
22.(1) ;(2)白磷 白磷 正盐;(3)正四面体 60°非极性。
|
|
23.(1) (2)KI+IBr=I2+KBr KBr (3)
(5)分子结构相似,分子间作用力随相对分子质量增大而增大
24.(1)N2、O2、F2、Ne C Na、Mg、Al;
(2)NaOH,HF。
|
(3) (4)F->Na+>Mg2+。
25.(1)Fe3+、Al3+ (2)A1(OH)3、Mg(OH)2 (3)NaOH 过滤、洗涤、灼烧
(4)CO2 (5)③测出CO2的质量 ④测出水蒸气的质量 (6)3、1、3
26.![]()
![]()