高三年级化学第一次阶段性考试试题卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 K-39 Mg-24 Ca-40 Zn-65
第Ⅰ卷 (选择题 共50分)
一、选择题(共50分)(每小题只有1个正确答案,1~10题各2分,共20分;11~20题各3分,共30分)
1.2004年夏季奥运会上,我国运动健儿取得了历史性的突破。2008夏季奥运会将在北京举行,届时要突出“绿色奥运、科技奥运、人文奥运”理念。绿色奥运是指
A.加大反恐力度,并讲求各国运动员的营养搭配,使他们全身心地投入比赛
B.严禁使用兴奋剂,使运动员公平竞争
C.把环境保护作为奥运设施规划和建设的首要条件
D.奥运场馆建设均使用天然材料,不使用合成材料
2.某溶液中大量存在四种离子:![]() 、
、![]() 、H+、M,其物质的量之比为:n(
、H+、M,其物质的量之比为:n(![]() )∶n(
)∶n(![]() )∶ n(H+)∶n(M)=3∶1∶3∶1,则M可能为: ① Fe2+ ② Mg2+ ③ Cl-
)∶ n(H+)∶n(M)=3∶1∶3∶1,则M可能为: ① Fe2+ ② Mg2+ ③ Cl-
④ Ba2+
A.①②④ B.③ C.② D.①②
3.下列叙述中(NA表示阿伏加德罗常数的值),正确的是
A.在同温同压下,两种气体的体积之比等于其摩尔质量的反比
B.气体摩尔体积是指在标准状况下1 mol任何气体所占的体积
C.在25℃时,1 L纯水中含H+的个数为10—7NA
D.在标准状况下,含4n mol HCl的浓盐酸与足量的MnO2反应生成Cl2分子的个数等于nNA
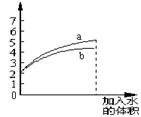 4.常温下,pH为2的两种酸溶液a和b,分别加水稀释1000倍,其pH与所加水的体积变化如图所示,下列结论正确的是
4.常温下,pH为2的两种酸溶液a和b,分别加水稀释1000倍,其pH与所加水的体积变化如图所示,下列结论正确的是
A、酸a的酸性比酸b的酸性强
B、同物质的量浓度时,b的导电能力比a的强
C、a比b难电离
D、pH相同时,酸a的物质的量浓度比酸b的大
5.在二氧化碳溶于水的平衡体系中,存在以下电离:
H2CO3![]() H+ +
H+ + ![]() ,
,![]()
![]() H+ +
H+ + ![]() ,若使溶液pH减小,则
,若使溶液pH减小,则![]() 的物质的量将
的物质的量将
A、增大 B、减小 C、不变 D、可能增大也可能减小
6.下列各离子组中,能在水溶液中大量共存,当滴加稀硫酸后则不能大量共存的是
A.Na+、Mg2+、Cl-、I- B.Fe2+、Ba2+、S2-、Cl-
C.Na+、Al3+、Cl-、![]() D.K+、Fe2+、Cl-、
D.K+、Fe2+、Cl-、![]()
7.在标准状况下,将4.48LSO2、CO2、H2的混合气通入适量的饱和NaHCO3溶液中,充分反应后,若溶液中的溶质只有NaHSO3,并且逸出的4.6g气体中只有CO2和H2,则原有混合气体中SO2、CO2、H2的体积比可能是
A.1︰1︰1 B. 1︰1︰2 C. 1︰2︰4 D. 2︰2︰3
8.常温下已知两种一元弱酸HX和HY,已知向NaX溶液中通入CO2气体只能生成HX和NaHCO3,往NaY溶液中通入CO2可以生成HY和Na2CO3。有关叙述正确的是
A.结合质子的能力:![]()
B.酸性由强至弱:HX >H2CO3>HY
C.溶液碱性:NaX>Na2CO3>NaY>NaHCO3
D.NaX溶液中通入足量CO2后的离子浓度:![]()
9.某氢氧化钠溶液跟醋酸溶液混合后溶液呈酸性,则混合溶液中离子的物质的量浓度之间关系一定正确的是
A.c(Na+)+c(H+)=c(CH3COO-) B.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) D.c(H+)=c(CH3COO-)-c(Na+)+c(OH-)
10.下列离子方程式中正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++ 2 OH-+ 2 H+ + ![]() = BaSO4↓+2
H2O
= BaSO4↓+2
H2O
B.NH4HCO3溶液与过量NaOH溶液反应:![]() + OH-= NH3↑+ H2O
+ OH-= NH3↑+ H2O
C.硫化钠溶于水中:S2- + 2 H2O = H2S↑ + 2 OH-
D.FeBr2溶液中通入过量Cl2:2 Fe2+ + 2 Br- + 2 Cl2 = 2 Fe3+ + Br2 + 4 Cl-
11.对反应:C(s)+H2O(g)![]() CO(g)+H2(g),建立平衡后,如改变条件使平衡向正方向移动,容器内混合气体平均相对分子质量将
CO(g)+H2(g),建立平衡后,如改变条件使平衡向正方向移动,容器内混合气体平均相对分子质量将
A、增大 B、减小 C、不变 D、前三者均有可能
12.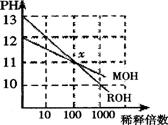 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中不正确的是
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中不正确的是
A.ROH是一种强碱
B.在x点,MOH未完全电离
C.在x点,C(M+)=C(R+)
D.稀释前,C(ROH)=10C(MOH)
13.一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g) ![]() zC(g)达到平衡后,测得A气体的浓度为0.5mol/L,恒温下将容器体积扩大1倍,反应重新达到平衡,测得A在新平衡时的浓度为0.225mol/L,下列叙述中正确的是
zC(g)达到平衡后,测得A气体的浓度为0.5mol/L,恒温下将容器体积扩大1倍,反应重新达到平衡,测得A在新平衡时的浓度为0.225mol/L,下列叙述中正确的是
A、x + y > z B、平衡向左移动
C、B的转化率提高 D、C的体积百分含量降低
14.某温度下,在一容积可变的容器中,反应2A(g)+B(g) ![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
A.均减半 B.均加倍 C.均增加1mol D.均减小1mol
15.反应:E+F=G在温度T1下进行,反应:M+N=K在温度T2下进行,已知T1>T2,且E和F的浓度均大于M和N的浓度(其它条件均相同),则两者的反应速率
A.前者大 B.后者大 C.一样大 D.无法确定
16.已知4NH3 + 5O2 = 4NO + 6H2O,若反应速率分别用V(NH3)、V(O2)、V(NO2)、
V(H2O)表示,则正确的是
A、4V(NH3)=5V(O2) B、5V(O2)=6V(H2O)
C、2V(NH3)=3V(H2O) D、4V(O2)=5V(NO)
17.已知HF的酸性比HCN的酸性强。在相同温度下,现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中的离子数目为n1,后者溶液中的离子数目为n2,下列关系正确的是
A、n1=n2 B、n1>n2 C、 n1<n2 D、c(F-)<c(CN-)
18.40℃时,等质量的两份饱和石灰水,一份冷却至10℃,另一份加少量CaO并保持温度仍为40℃,这两种情况都不改变的是(已知Ca(OH)2的溶解度随温度的升高而降低)
A.Ca(OH)2的物质的量浓度 B.溶液的质量
C.溶质的质量分数 D.溶液中Ca2+数目
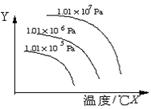 19.下图表示改变条件时,对反应A(g)+2B(g)
19.下图表示改变条件时,对反应A(g)+2B(g)![]() 2C(g);△H<0的影响情况。图中纵坐标Y表示
2C(g);△H<0的影响情况。图中纵坐标Y表示
A.平衡混合气体中C的百分含量
B.平衡混合气体中A的百分含量
C.A的反应速率
D.C的反应速率
 20.反应mA
(s)+nB (g)
20.反应mA
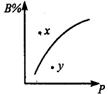
(s)+nB (g) ![]() pC(g);△H<0,在一定温度下B的体积分数(B%)与压强变化的关系如下图所示,下列叙述中正确的是:①m+n>p ②x
点表示该反应的正反应速率大于逆反应速率
pC(g);△H<0,在一定温度下B的体积分数(B%)与压强变化的关系如下图所示,下列叙述中正确的是:①m+n>p ②x
点表示该反应的正反应速率大于逆反应速率
③n>p ④ x 点比y 点的反应速率慢
A. ① B.①③ C. ①③④ D.②④
高三年级第一次阶段性考试化学答题卷
一. 将选择题的答案填入下表中(共50分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
| 题号 | 11 | 15 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
二.非选择题(共29分)
21.(12分)已知N2+3H2 ![]() 2NH3;△H=-akJ·mol-1(a>0)。在一个有催化剂的固定容积的容器中加入1 molN2和3 molH2,在500℃,时充分反应达到平衡后NH3浓度为
2NH3;△H=-akJ·mol-1(a>0)。在一个有催化剂的固定容积的容器中加入1 molN2和3 molH2,在500℃,时充分反应达到平衡后NH3浓度为
n mol·L-1,放出热量为bkJ。
(1)比较a、b大小:a b(填“>”“<”或“=”)
(2)若将反应温度升高到600℃,平衡将向 反应方向移动(填“正”或“逆”)
(3)若在原来的容器中只加入2mol NH3,500℃时充分反应达到平衡时,吸收热量为c kJ,则NH3的浓度为 n mol·L-1(填“>”“<”或“=”),a、b、c三个数值满足何种关系 (用代数式表示)。
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入lmolN2和3molH2,在500℃下达到平衡,放出热量为d kJ,则d b(填“>”“<”或“=”),理由是
。
22、(10分)根据下列各实验要求设计实验。
(1)现有药品和仪器:石蕊试液、酚酞试液、pH试纸、NaOH溶液、酒精灯、半透膜、电泳仪、聚光束仪。就明矾溶于水发生的下列变化,请分别设计最佳化学实验方案,简述实验方法、现象、结论。
①证明明矾发生了水解反应: ,
②证明水解产物呈胶体
。
③证明此水解反应是吸热反应
。
(2)有A、B、C三种溶液,它们是浓度均为0.1mol·L-1的NaOH、H2SO4、NaCl溶液。某同学只有酚酞试液,用下面最简单且滴加液体的次数最少的实验方法,分二步将上述三种溶液鉴别出来。
第一步实验操作和现象如下:取少量A溶液滴入几滴酚酞、无现象,又取少量B溶液
滴入几滴酚酞,又无现象。则C溶液是 ,请写出第二步实验操作,现象和
结论
。
23.(7分)现有A、B、C、D、E五种盐溶液,分别由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同).已知:①A+C→白↓ ②A+D→白↓ ③B+D→白↓④D+C→白↓ ⑤A溶液中c(H+)=c(OH-) ⑥B溶液中c(H+)=1×10-12mol·L-1 ⑦C、D、E三种溶液的pH<7,根据以上实验事实可以推出(用分子式表示)
中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同).已知:①A+C→白↓ ②A+D→白↓ ③B+D→白↓④D+C→白↓ ⑤A溶液中c(H+)=c(OH-) ⑥B溶液中c(H+)=1×10-12mol·L-1 ⑦C、D、E三种溶液的pH<7,根据以上实验事实可以推出(用分子式表示)
A为____ _____;B为___ ____;C为____ _____;
D为__ __;E为___ _ ____。
写出③反应的离子方程式:_ _
三.计算题(共21分)
24.(12分)已知固体混合物A由①NaHCO3、②KHCO3、③MgCO3、④CaCO3四种物质中的两种混合而成,通过计算和推理回答下列问题:
⑴取A与足量的盐酸反应:
a若A的物质的量n(A)为定值,生成气体的量即为定值,则A的组成最多可能有 种。
b若A的质量m(A)为定值,生成气体的量即为定值,则A的组成是 ;
; 。(可以不填满,也可以补充)
⑵若先将A加热,剩余固体再与足量盐酸反应,且先后两次产生的气体分别通过足量的澄清的石灰水生成的沉淀均为10.0g,则A的物质的量n(A)= mol
⑶ 若将wgA高温灼烧至恒重时,固体减轻xg,则x为: 。
25. (9分)现将600 mL稀硫酸等体积分为6份,并向其中5份中分别加入质量不等的Zn粒,并收集生成的氢气,有以下记录结果(H2体积已折算为标准状况)。
| 实验① | 实验② | 实验③ | 实验④ | 实验⑤ | |
| Zn粒质量(g) | 5.0 | 8.0 | 12 | 14 | 16 |
| H2体积(L) | 1.72 | 4.14 | 4.48 | 4.48 |
(1)由实验结果可推知,此稀硫酸的物质的量浓度为 _________________________。实验②收集到H2的体积为 _________________________。
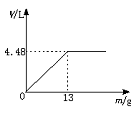
(2)若向第6份稀硫酸中不断加入Zn粒,请在下图中画出H2体积(V)与Zn粒质量(m)的关系图象。
| 答案 | D | D | C | C | D | D | B | C | A | D |
高三年级第一次阶段性考试化学答案及评分标准
21. (共12分)(每空2分) (1)>; (2)逆;(3)= ; a=b+c ; (4)>;
在恒压条件下所达到平衡时容器有体积将比原来小,可看成是在(1)在恒容条件下达平衡的基础上采取了加压使平衡向正向移动达到的一新平衡,而正向为放热反应,所以d>b.
22、(共10分)⑴(各2分)
①用pH试纸(或石蕊试液)检验溶液的酸碱性,若pH<7(或溶液呈红色)则证明明矾发生了水解。
②用聚光束仪对溶液进行丁达尔现象实验,若能观察到溶液中有光亮的通路,证明水解产物呈胶体。
③先用pH试纸测定溶液的pH, 然后给溶液加热到一定温度,再用pH试纸测定溶液的pH,若第二次测得的pH小于第一次测得的pH,证明此水解反应是吸热反应。
⑵NaOH溶液; 向滴有酚酞的A溶液中,滴入几滴C溶液,若溶液呈红色,则A溶液为NaCl溶液,B溶液为H2SO4溶液;若无现象,则A溶液为H2SO4溶液,B溶液为NaCl溶液)
23 (共7分) BaCl2; K2CO3; AgNO3 Al2(SO4)3 NH4Br (各1分)
Al3++3![]() +3H2O=Al(OH)3↓+3
+3H2O=Al(OH)3↓+3![]() (2分)
(2分)
 24.(共12分)⑴(各2分)6; ①③、②④; ⑵0.2(3分);
24.(共12分)⑴(各2分)6; ①③、②④; ⑵0.2(3分);
⑶![]() (3分)
(3分)
25.(9共分)(1)2.0 mol·L-1(3分)
2.76 L(3分)
(2)如右图所示(3分)。