高三年级化学阶段测试试题
化 学 试 题
可能用到的相对原子质量H1 P31 Fe56 Al27 C12 Na23 O16 S32 Mg24 K39 Ba137 Cu64 N14 Zn65
一、选择题(每小题只有一个选项符合题意,每小题3分,本题共78分)
1.一定温度下,有可逆反应:2A(g)+2B(g)![]() C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B
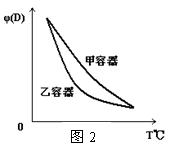 充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。 ( )
充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。 ( )
 |
|
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,但混合气]
体的平均相对分子质量不相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
2.下列各对应反应的离子方程式正确的是 ( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
B.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-=Cl2↑+Mn2++H2O
C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
D.用可溶性铝盐溶液和过量氢氧化钠溶液制取氢氧化铝:Al3++3OH-=Al(OH)3↓
3.下列说法或表示法正确的是 ( )
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石):ΔH = +119 kJ· mol—1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-aq)-===H2O(l);ΔH=-57.3 kJ· mol—1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l);ΔH=-285.8 kJ· mol—1
4.空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民
的支持。下列措施不利于“蓝天工程”建设的是 ( )
| |
B.加大石油、煤炭的开采速度,增加化石燃料的供应量
C.研制开发燃料电池汽车,消除机动车尾气污染
D.实施绿化工程,防治扬尘污染
5.一定能在下列溶液中大量共存的离子组是 ( )
A.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
B.c(H+)=1×10—13mol·L—1的溶液:Na+、Ca2+、SO42-、CO32-
C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
D.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-
6.下列叙述正确的是 ( )
A.室温时10mL 0.02mol·L—1 HCl溶液与10mL 0.02mol·L—1 Ba(OH)2溶液充分混合,
若混合后溶液的体积为20mL,则溶液的pH=12
B.0.1mol·L—1氨水中, c(OH—)<c(NH4+)< 0.1mol
C.在0.1mol·L—1 CH3COONa溶液中,c(OH—)=c(CH3COOH)+c(H+)-C(CH3COO-)
D.0.1mol·L—1某二元弱酸碱性NaHA溶液中,c(Na+)=2c(A2—)+c(HA—)+c(H2A)
7.物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(H+)<c(OH-),
下列关系式正确的是 ( )
A.c(CN-)>c(Na+) B.c(HCN)<c(CN-)
C.c(CN-)+ c(OH-)=0.1mol·L-1 D. c(HCN)+ c(CN-)=0.2mol·L-1
8.硝酸铵在不同条件下分解可以得到不同的产物,下列各组物质中肯定不可能是硝酸铵分
解产物的是 ( )
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
9.用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.4 g重水(D2O)中所含质子数为0.2 NA
B.4.48 L N2与CO的混合物所含分子数为0.2 NA
C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2 NA
D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2 NA
10.向一定浓度的下列物质澄清溶液中通入过量的CO2气体,最后肯定没有沉淀生成的是
( )
①Ca(OH)2 ②Na2CO3 ③CaCl2 ④Ca(ClO)2
A.①③④ B.②③④ C.①②③ D.①②③④
11.A、B、C为三种短周期元素,A、B在同周期, A、C的最低价离子分别为A2-和
C-,B2+和C-具有相同的电子层结构。下列说法中正确的是 ( )
A.原子序数:A>C>B B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
12.下列物质中,均直接由原子构成的是 ( )
①二氧化碳 ②二氧化硅 ③铁蒸气 ④金刚石
⑤单晶硅 ⑥白磷 ⑦硫磺 ⑧氨
⑨钠 ⑩氖晶体
A.②③④⑤ B.②③④⑤⑨⑩ C.②③④⑤⑩ D.②④⑤⑥⑦⑨⑩
13.一定条件下,可逆反应C(s) + CO2(g)![]() 2CO(g);△H>0,达到平衡状态,现进行如下操作:
2CO(g);△H>0,达到平衡状态,现进行如下操作:
①升高反应体系的温度; ②增加反应物C的用量;
③缩小反应体系的体积; ④减少体系中CO的量。
上述措施中一定能使反应的正反应速率显著加快的是 ( )
A.①②③④ B.①③ C.①② D.①③④
14.必须加入氧化剂才能实现的是 ( )
A.Cl2 → NaClO B.Fe2+ → Fe3+
C.H2S → S D.Na2O2 → O2
15.从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4 + 5FeS2 + 12H2O = 7Cu2S + 5FeSO4 + 12H2SO4 ,下列说法正确的是
( )
A.Cu2S既是氧化产物又是还原产物
B.5mol FeS2发生反应,有10mol电子转移
C.产物中的SO42-离子有一部分是氧化产物
D.FeS2只作还原剂
16.R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;X2++Z=X+Z2+;Y+Z2+=Y2++Z。这四种离子被还原成0价时表现的氧化性大小符合( )
A.R2+>X2+>Z2+>Y2+ B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+ D.Z2+>X2+>R2+>Y2+
17.X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为 ( )
A. XY B.XY2 C.XY3 D .X2Y3
18.下列关于硅的说法不正确的是 ( )
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质起反应
| |
19.若1.8g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氢气,
则该金属是 ( )
A.Al B.Mg C.Fe D.Zn
20.用特殊方法把固体物质加工到纳米级(1-100nm)的超细粉末粒子,将这种粉末粒子分散到水中形成的分散系为 ( )
A.溶液 B.悬浊液 C.胶体 D.乳浊液
21.下列关于胶体的叙述不正确的是 ( )
A.布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
B.一束强光透过胶体时,胶体发生丁达尔现象
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳
现象
22.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
A.11.2g B.16.8g C.19.6g D.22.4g
23.根据元素性质递变规律,下列判断均正确的是 ( )
A.酸性:HClO4>HBrO4>HIO4;碱性:NaOH>KOH>RbOH
B.沸点:Cl2<Br2<I2;熔点:Na<K<Rb
 C.可燃性:H2O<NH3<CH4;还原性:HCl<H2S<PH3
C.可燃性:H2O<NH3<CH4;还原性:HCl<H2S<PH3
D.还原性:Na>Mg>Al;氧化性:P>S>Cl2
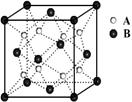
24.某离子晶体的晶体结构中最小重复单元如图
所示:A为阴离子,在正方体内,B为阳离
子,分别在顶点和面心,则该晶体的化学式
为 ( )
A.B2A B.B.BA2 C.B7A4 D.B4A7
25.X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为 ( )
A.X>Z>Y>M B.X>Y>Z>M
C.M>Z>X>Y D.X>Z>M>Y
26.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是 ( )
A .NH4+、NO3-、CO32-、Na+
B.Na+、Ba2+、HCO3-、AlO2-
C.NO3-、Fe2+、K+、Cl-
D.NO3-、K+、AlO2-、OH-
二、填空题
27.(12分)下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是对演示实验改进后的装置(其中a、b、c 为弹簧夹),试回答下列各问:
(1)甲装置中发生反应的离子方程式是 。
(2)和甲装置相比,乙装置的优点是 。
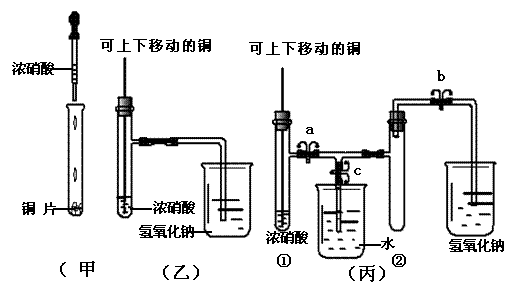
(3)为了进一步验证NO2和水的反应,某同学设计了丙装置。先关闭弹簧夹 (填a、b、c,后同),再打开弹簧夹 ,才能使NO2气体充满②试管。
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操作 。
(5)当②试管中的NO2和水充分反应,所得溶液物质的量浓度的最大值是 。(不考虑NO2与N2O4的转化且该实验条件下气体摩尔体积设为Vm L/mol)
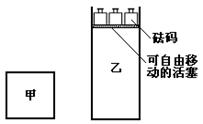
28.(8分)右图是一个体积固定的恒温密闭容
 器,正中间一个可以滑动的隔板将容器隔
器,正中间一个可以滑动的隔板将容器隔
成A、B两室。A室放入H2和O2共5mol,
B室放入H2和N2共5mol,使隔板恰好处
于正中间。
(1)控制一定条件,只使A室气体充分反
应,此时隔板左移,待反应完成且密
闭容器温度恒定(大于120℃)后,A室
气体体积是B室体积的4/5。计算原H2和O2的体积比为 。
(2)再控制一定条件,使H2和N2发生反应(正反应放热)。当密闭容器温度恒定(大
于120℃)且达到平衡时,隔板右移恰好回到正中间,若加入的N2为1mol,则N2的转化率为 ;若加入的N2为x mol,则x的取值范围是
(3)在水为气态的前提下,若改变条件,使隔板继续右移,则改变的条件是
29.(10分)某复盐的组成可表示为:![]() ,R为-2价含氧酸根.为了确定该盐的组成,进行如下实验:
,R为-2价含氧酸根.为了确定该盐的组成,进行如下实验:
(1)准确称取4.02 g样品加热到失去全部结晶水,冷却后称量,质量为2.94 g.
(2)将剩余固体溶于适量水,滴加盐酸,无现象,再滴加足量![]() 溶液,产生白色沉淀.过滤,将沉淀烘干,称质量为4.66 g.向过滤后溶液中加入过量NaOH溶液,产生白色沉淀,过滤,将沉淀烘干,称质量为0.58g,再将固体高温灼烧后冷却,称得剩余固体质量是0.40 g.
溶液,产生白色沉淀.过滤,将沉淀烘干,称质量为4.66 g.向过滤后溶液中加入过量NaOH溶液,产生白色沉淀,过滤,将沉淀烘干,称质量为0.58g,再将固体高温灼烧后冷却,称得剩余固体质量是0.40 g.
试回答下列问题:
(1)R的化学式为_____________ _.
(2)B原子的结构示意图为_______ __.
(3)A元素的名称是____________ _.
(4)要确定某化合物是否含A元素,最简单方法是______________.
(5)该复盐的化学式为______________.
30.(12分)如果取0.1 mol/LHA溶液与0.1mol/LNaOH溶液等体积混合,测得混合溶液室温时的pH=8 。
试回答下列问题:(1)求出混合溶液中下列算式的精确计算结果:
c(Na+)一c(A-)= mol·L-1,c(OH-)一c(HA)= mol·L-1
(2)写出HA的电离式
(3)在含有A-、Na+、H+、OH-四种离子的水溶液中,如果出现下列关系请将它们在溶液中可能对应的溶质化学式分别填在横线上:
①c(Na+)>c(A-)>c(OH-)>c(H+): ②c(A-)>c(Na+)>c(H+)>c(OH-):
③c(Na+)>c(OH-)>c(A-)>c(H+):
31.(10分)
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。
肼—空气燃料电池放电时:
正极的电极反应式是 。
负极的电极反应式是 。
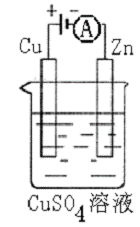
(3)右下图是一个电化学过程示意图。
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变 化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
|
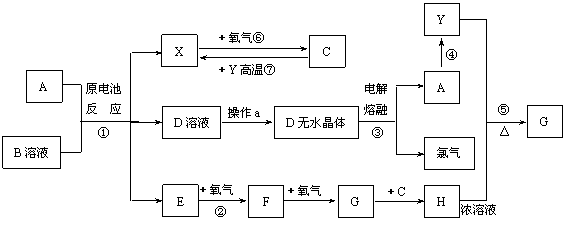
32.(12分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为 。
(2)从D溶液制备D的无水晶体的“操作a”为 。
(3)反应②的化学方程式为 。
(4)反应⑤的化学方程式为 。
(5)原电池反应①中正极的电极反应式为 。
(6)写出③反应的化学方程式
三、计算
33.(8分)将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入pH=0的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
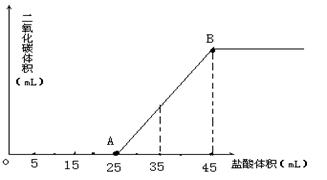
(1)写出OA段所发生反应的离子方程式。
(2)当加入35mL盐酸时,产生二氧化碳的体积 为 _ _____mL(标准状况)。
(3)计算原混合物中Na2CO3的质量分数。
参考答案
1.D 2.C 3.C 4.B 5.D 6.A 7.D 8.D 9.C
10.A 11.C 12.C 13.B 14.B 15.C 16.A 17.A 18.C
19.A 20.C 21.A 22.D 23.C 24.B 25.A 26.D
27.(1)Cu + 4H+ + 2NO3- = Cu2+ + 2 NO2↑+ 2H2O。(2分)
(2)①可以控制反应。(1分)②吸收NO2气体,防止污染环境。(1分)
(3)关闭c(1分);打开a、b(1分)。
(4)先关闭b,再关闭a,然后打开c,(2分)用手捂住(热水、热毛巾、加热)②试管。(2分)
(5)1/Vm mol·L-1(2分)。
28.(每空2分)
(1)2:3或4:1
(2)50% ;0.5﹤x﹤3.5
(3)降温
29.(每空2分)
(1)化学式为![]()
(2)略
(3)A元素的名称是钾
(4)焰色反应
(5)复盐的化学式为![]()
30.(每空2分)
(1)9.9×10-7;1×10-8
(2) HA![]() A-+H+
A-+H+
(3)①NaA或 NaA和NaOH ②HA和NaA③NaA和NaOH
31.(每空2分)
(1)N2H4(1)+O2(g)=N2(g)+2H2O(1);△H=-624kJ/mol
(2)O2+2H2O+4e-=4OH -N2H4+4OH--4e-=4H2O+N2↑
(3)①Cu2++2e-=Cu ②112
32.(每小题2分,共12分)
(1)2Mg+CO2====2MgO+C
(2)将D溶液在HCl气流中蒸干;
|
(3)4NH3+5O2==== 4NO+6H2O;
(4)C+4HNO3====CO2↑+4NO2↑+2H2O
(5)2NH4++2e- = 2NH3↑+H2↑
(6)略
33.(8分)(1)H++OH-=H2O, CO32-+H+=HCO3-3-(各1分)
(1)224(3分)
ω(Na2CO3)=42.4% (3分)
答:原混合物中Na2CO3的质量分数为42.4%。