�����꼶�����ۺ��ײ�����(һ)
���Ծ��֢�ھ�(ѡ����)�͵ڢ��(��ѡ����)�����֡���300�֣�����ʱ��150���ӡ�
�ڢ����ѡ���126�֣�
ע�����
1�� ��ڢ��ǰ��������ؽ��Լ�����������֤�š����Կ�ĿͿд�ڴ���ϡ�
2�� ÿС��ѡ���𰸺���Ǧ�ʰѴ���϶�Ӧ��Ŀ�Ĵ𰸱��Ϳ�ڣ�����Ķ�������Ƥ���ɾ�����ѡͿ�����𰸱�ţ����ܴ���������ϡ�
3�� ���Խ�������˽����Ծ��ʹ��һ���ջء�
�����õ������ԭ��������H��1 C��12 N��14 O��16
һ��ѡ���⣨�������13С�⡣ÿС��ֻ��һ��ѡ��������⣬ÿ��6�֡���
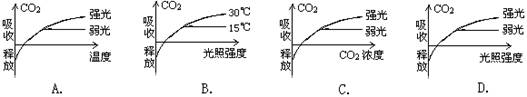
1��ijͬѧ�о�������̬���ضԹ�����õ�Ӱ�죬����ʵ�������Ƴ�������ͼ����ͼ��ʾ����ʦ�Ը�ѧ���������ǡ������û�����ȷ��
�����ﲻ��������������4λͬѧ�Ը�����ͼ�����IJ��䣬����Ϊ��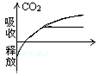
|
��������������
2���±���ʾij��ʳ���е����ְ�����ĺ��������嵰���������ְ������ƽ�����������ʣ������ʳ������ʳ��������ڷ������������������̣�����ʹʳ���е������ְ�����õ���ֺ��������ã���������������������������
| ������ | ������ | ������ | �Ȱ��� | ˿���� |
| ʳ���� | 0.01g/g | 0.10g/g | 0.05g/g | 0.20g/g |
| ���嵰������ | 0.20g/g | 0.01g/g | 0.10g/g | 0.04g/g |
������ A���Ѱ������á�������B���������á�����������C������ת�����á��� D����������
3���ö���������Ϊ�ױ����������������������ϡ������У�����˵����ȷ���ǡ��� ��������
������ A����һ���ֲ���У�Ⱦɫ�������ɴ���2��3��4��5��Ⱦɫ����
������ B���ڶ����ֲ����û��ͬԴȾɫ��
������ C����һ������������Ƥ���ߡ������Ⱦɫ��������ͬ�����ǵ����ӽ��Ľ��
������ D���ڶ����ֲ��������������ĸ�����������ĸ��������ľ����ܾ��ò�������
������ ��������
|
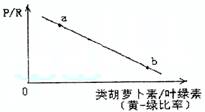
������ A���ڴ�ů��������Ȼˮ�ơ��̱���������
����
������ B����ˮ�����ջڣ�Ⱥ��P/Rֵ������a��
������ C�����������ֲ��Ļơ��̱��ʿ�����b��
������ D���˹��ֵ���ƽ���ơ��̱��ʹ���ʱ��Ӧ����
�ʵ��ɷ�
|
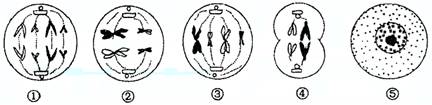
������������йصļ���˵���У�����ȷ���ǡ���������������������������������������������������������������
������ A�����ķ�������ʾ�������������Ҫ����ͼ����ʾ��ʱ�ڽ��е�
������ B�����Ŵ��ı�����Դ֮һ�Ļ�������ķ�����ͼ���йض���ͼ����ֱ�ӹ�ϵ
������ C����ͼ��ʾϸ�����ѷ�ʽ��������ڷ����Ļ���ͻ�䴫�ݸ���һ���Ŀ�����Ҫ��ͼ����ʾ�Ĵ�ö�
������ D�������Զ������ڣ�ͬʱ�߱�����5��ͼ��ʾϸ������ʱ�ڵ�������غ������Ǹ���
6������˵����ȷ���ǣ�������
A��������ˮΪ֮��������ˮ��˵����ͬ������ˮ�ͱ���ˮ��������
B����H2��I2(g)��HI��ɵ�ƽ����ϵ����ѹ����ɫ����������������ԭ������
C���Թ�������������ۣ��ټ���һ����ϡ���ᣬ����3��4���ӣ�Ȼ�����������Һ��Ƭ�̺�ܱ��Ͼͻ��С�����������
D������ʵĵ����Ժͽ�������ĵ����Զ����¶ȵ����߶���ǿ
7������о�֤�������������������������Ч���������ú�����ƫ�����ƺ�ʳ�εĻ����Һ��4���ѪҺ�е��������ɻָ������������Ļ������ж��������ն��˻�÷�ˮ�ס�����������ȷ���ǡ��������� ��������
A����������Ԫ�أ���Ԫ�����ڱ��д��ڵ�������
B������ѪҺ�к����������ǣ�ҽԺע�����õ���Ҳ������
C�������������Һ��ʵ�ʾ��Ǽ�⺬��������
D��V2O5��������������л��ϳɵĴ���
8.A��B�Ƕ����ڢ�A�������Ԫ�أ�Ԫ��A�ķǽ����Ա�Bǿ�������й�A��B��˵������ȷ���ǣ�������
��A��HA��HB�е�ߵ�ԭ����1molHA������H-A������ʱ��Ҫ���յ�������1molHB������H-B������ʱ��Ҫ���յ�������
B������A�ɰ�B��NaB����Һ���û�����
C��NaA��NaB�ľ��嶼�����Ӿ���
D�������£�NaA��NaB��Һ��pH������7
9�����и��ֱ�����ȷ���ǣ�������
A�����⻯�Ƶ�ˮ�⣺HS��+H2O![]() H3O++S2-
H3O++S2-
B��С�մ���Һ�еμӴ�����Һ��HCO3-+CH3COOH==CH3COO-+H2O+CO2��
C���ȼҵĿǰ���õıȽ��Ƚ����豸�������ӽ���Ĥ�����У����������ķ�Ӧ�ǣ�4OH����4e-==O2��+2H2O
D��CH4��ȼ����Ϊ802.3kJ/mol��CH4(g)+2O2(g)==2H2O(g)+CO2(g)����H=��802.3kJ/mol
10�������ӵ�����ԼΪ6.02��1023 mol��1�����������в���ȷ���ǣ�������
A����162.5g FeCl3ת��Ϊ�������������������������������С��6.02��1023
![]() B���ں�196g H2SO4��Ũ������Һ�м���������п��ʹ���ַ�Ӧ����Ӧ����ʱ��ת�Ƶ�����ԼΪ4��6.02��1023
B���ں�196g H2SO4��Ũ������Һ�м���������п��ʹ���ַ�Ӧ����Ӧ����ʱ��ת�Ƶ�����ԼΪ4��6.02��1023
C����ʯī�����У�ƽ��0.3 mol̼̼���ۼ������е�̼ԭ����ԼΪ����6.02��1023
D��1mol C10H22�����й��ۼ�����ԼΪ31��6.02��1023
11��ʼ����ϩ(Pterodactyladiene)����״����һֻչ�������������ʽ����ͼ������R1��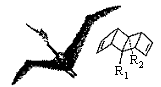 R2Ϊ���������������й�ʼ����ϩ��˵������ȷ���ǣ�����
R2Ϊ���������������й�ʼ����ϩ��˵������ȷ���ǣ�����
��A��ʼ����ϩ����ϩ��Ϊͬϵ��
B����R1=R2= ��CH3�����仯ѧʽΪC12H16
C����R1=R2��һ��������ϩ��˫��̼ԭ���ϵ���Ҳ��ȡ������ʼ����ϩ���ϵĶ��ȴ�����10�֡�
D��ʼ����ϩ����ʹ���Ը��������ɫҲ��ʹ��ˮ��ɫ������ɫԭ����һ����
12���к͵ζ�ʵ���У���NaOH��Һ��Ũ�ȣ�ͨ����H2C2O4��H2OΪ�����ʽ��б궨�������ʱ���߱��������������ʴ���Ҫ�ߣ�����Է��������ϴ������ȶ����粻�ֽ⡢���绯�������⡢���������е�CO2��O2�ȷ�Ӧ��ʵ���ұ궨�����Ũ��ʱ��ѡ��Ļ���������ǣ�������
A��NaOH������B��NaHCO3������C��Na2CO3������D��Na2CO3��10H2O
13��A��һ�ֳ����ĵ��ʣ�B��CΪ��ѧ�����Ļ����A��B��C������Ԫ��X�����������µ�ת����ϵ(���ֲ��P��Ӧ��������ȥ)��
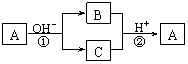 |
�� �����ж���ȷ���ǣ�������
A��XԪ�ؿ���ΪAl������������ B��XԪ��һ��Ϊ�ǽ���Ԫ��
C����Ӧ�ٺ͢ڻ�Ϊ���淴Ӧ������ D����Ӧ�١��ڲ�һ��Ϊ������ԭ��Ӧ
�������¸�ѡ���У�������һ���������⣬�������ѡ������ȫ��ѡ�Ե�6�֣�ѡ��ȫ��3�֣�ѡ����ѡ��0�֣�ÿ��6�֡�
14�����ĵ����Ƚ�ȷ�ز������������ʵ�飬�����и�ͼ��ʾ��ʵ���е���һ����
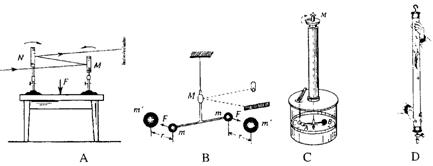
15 ������˵������ȷ����
A������ķ������˶����ܵ��ܺ;������������
B������ͬһ�����壬�¶�Խ�ߣ�����ƽ������һ��Խ��
C��Ҫʹ����ķ���ƽ���������������������崫��
D��һ�����������壬�¶�����ʱ�����Ӽ��ƽ������һ������
16 ������˵����ȷ����
����A��̫�������������Ҫ����̫���ڲ����ѱ䷴Ӧ
����B������¬ɪ���Ħ�����ɢ��ʵ����Թ���ԭ�Ӻ˵Ĵ�С
����C���������������ݦ�����ɢ��ʵ������ó���
D����ԭ�Ӻ�����ӴӰ뾶��С�Ĺ��ԾǨ���뾶�ϴ�Ĺ��ʱ�����ӵĶ��ܼ�С����������������������
17 . �����ṩ�˿Ƽ���չ��������Ϣ�����п϶��������
A�� ���¼��������ش�ͻ�ƣ�1933������Ѵ�0.25K, 1995��ͨ��һϵ������ķ����Ѵﵽ1��10-8K �����ŵ��¼����ķ�չ����ѧ��һ���ܰ�����ѧ�¶Ƚ�������������¡�
B�� ���Ż�������ķ�չ������һ���ܹ��ڵ����������λ�÷���һ��ͬ�����ǡ�
C�� һ�����ʿ���С����������ij��ʹ���е����嶼��������С�Ŵ����������ѧ��ϣ���ڲ��õĽ�����ʹ���˷ɻ���С������ע����ע�䵽�˵�Ѫ���У��Ա�ҽ�����벡������������ơ�
D�� ����̫�������䣬���������¶ȿɴ�30�����ң�����������¶�Ҫ�͵ö࣬��ˮ��600��1000m�ĵط���ˮ��Լ4�棬���������������һ�ֿ���ʴ���Ƚ����������ú�ˮ�²�磬��ȡ���˳ɹ���
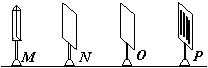 18��Ӣ������ѧ������˹��������ؽ������ɹ�Դ���⣬��һ����ʵ���ҹ۲쵽�˹�ĸ���������ͼΪʵ��װ�ü�ͼ��MΪ��ֱ�߹�Դ(��ֱ��˿�Ƶ�)��N��O��Ϊ��������ڹ�����PΪ�������������ֲ�ͬ����������ڹ�����ʵ��ʱ����ȷѡ����
18��Ӣ������ѧ������˹��������ؽ������ɹ�Դ���⣬��һ����ʵ���ҹ۲쵽�˹�ĸ���������ͼΪʵ��װ�ü�ͼ��MΪ��ֱ�߹�Դ(��ֱ��˿�Ƶ�)��N��O��Ϊ��������ڹ�����PΪ�������������ֲ�ͬ����������ڹ�����ʵ��ʱ����ȷѡ����
A��NӦѡ1��OӦѡ2 ��
B��NӦѡ3��OӦѡ4 ��
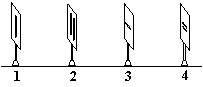 C��NӦѡ1��OӦѡ4 ��
C��NӦѡ1��OӦѡ4 ��
D��NӦѡ3��OӦѡ2 ��
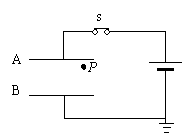 19.��ͼ��ƽ�а������������S�������ӣ�P���̶���һ�������dz�С��������q �����²����У���ʹq�ĵ�����������ǡ�������
19.��ͼ��ƽ�а������������S�������ӣ�P���̶���һ�������dz�С��������q �����²����У���ʹq�ĵ�����������ǡ�������
A��S�պϣ���A������һС�ξ���
B��S�պϣ���B������һС�ξ���
C��S�ȱպϺ�Ͽ���Ȼ��A������һС�ξ���
D��S�ȱպϺ�Ͽ���Ȼ��B������һС�ξ���
20 ��ͼ1�У���ԴS��ƽ��λ��y=0��ʼ���˶�������ֱ����(y���������)��������T=0.01s�������ļ�г���������������������پ�Ϊv=80m/s������һ��ʱ���P��Q���㿪ʼ��,��֪����SP=1.2m��SQ=2.6m������Q�㿪ʼ��ʱ����Ϊ��ʱ����㣬����ͼ2����ͼ���У�����ȷ����P��Q�������������
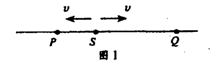 A����ΪQ����ͼ��
A����ΪQ����ͼ��
B����ΪQ����ͼ��
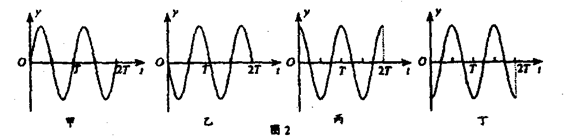 C����ΪP����ͼ��
C����ΪP����ͼ��
D����ΪP����ͼ��
������������������������������������������������������������������������������������
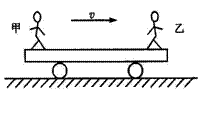 21 .��ͼ��ʾ���⻬ˮƽ������һ������Ϊ2m��С���������������˷ֱ�վ�żס��������ˣ����ǵ���������m����ʼ���˺ͳ�һ�����ٶ�
21 .��ͼ��ʾ���⻬ˮƽ������һ������Ϊ2m��С���������������˷ֱ�վ�żס��������ˣ����ǵ���������m����ʼ���˺ͳ�һ�����ٶ�![]() ���������˶���ijһʱ�̣�վ�ڳ��Ҷ˵�����������ڵ���ˮƽ���ҵ��ٶ�u����С����Ȼ��վ�ڳ���˵ļ�������ڵ���ˮƽ������ٶ�u����С�������˶��뿪С����С�����ٶȽ���
���������˶���ijһʱ�̣�վ�ڳ��Ҷ˵�����������ڵ���ˮƽ���ҵ��ٶ�u����С����Ȼ��վ�ڳ���˵ļ�������ڵ���ˮƽ������ٶ�u����С�������˶��뿪С����С�����ٶȽ���
A.![]() ����
B.2
����
B.2![]() ����
C.����
����
C.����![]() ��2
��2![]() �� D.����2
�� D.����2![]()
�ڢ������ѡ����,��174�֣�
ע�����
1�� �øֱʻ�Բ���ֱ�Ӵ��������У�����Ŀ������涨�⣩��
2�� ���ǰ���ܷ����ڵ���Ŀ��д�����
������ѡ���⣬��10�����⡣
22��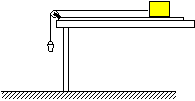 ��17�֣�һλͬѧ������ô���ʱ������ľ���볤ľ���Ķ�Ħ��������ʵ�飬ʵ��װ����ͼ��ʾ����ľ�崦��ˮƽ��װɰ��СͰ��ɰ���ɵ�����ͨ��ϸ���ƹ���������ľ�������ӣ�ϸ�ߵij��ȴ�������ĸ߶ȡ�����ͻȻ�ƶ�ľ���ľ���϶�ֽ����ͼ��δ����ֽ���ʹ���ʱ������ˮƽľ���˶���СͰ�����Ӵ�֮��ľ����ľ���ϼ����˶�һ�ξ����ͣ��(ľ��δ�붨������ײ)����ľ���˶�������Դ���أ�����ʱ����ֽ���ϴ���һϵ�еĵ㡣�ı�СͰ�е�ɰ�����ظ�����ʵ�飬�õ�����ֽ����ѡ�����е�һ��ֽ����ͼ�и�����ֽ����ǰ����������¼�Ĵ���������������ֽ����1��2��3��4��5�������㵽0�ľ������±���ʾ��������ֽ���ṩ�����ݣ���
��17�֣�һλͬѧ������ô���ʱ������ľ���볤ľ���Ķ�Ħ��������ʵ�飬ʵ��װ����ͼ��ʾ����ľ�崦��ˮƽ��װɰ��СͰ��ɰ���ɵ�����ͨ��ϸ���ƹ���������ľ�������ӣ�ϸ�ߵij��ȴ�������ĸ߶ȡ�����ͻȻ�ƶ�ľ���ľ���϶�ֽ����ͼ��δ����ֽ���ʹ���ʱ������ˮƽľ���˶���СͰ�����Ӵ�֮��ľ����ľ���ϼ����˶�һ�ξ����ͣ��(ľ��δ�붨������ײ)����ľ���˶�������Դ���أ�����ʱ����ֽ���ϴ���һϵ�еĵ㡣�ı�СͰ�е�ɰ�����ظ�����ʵ�飬�õ�����ֽ����ѡ�����е�һ��ֽ����ͼ�и�����ֽ����ǰ����������¼�Ĵ���������������ֽ����1��2��3��4��5�������㵽0�ľ������±���ʾ��������ֽ���ṩ�����ݣ���
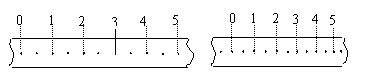 ��
��
�����cm
| 1 | 2 | 3 | 4 | 5 | |
| ǰһ�� | 4.8 | 9.6 | 14.4 | 19.2 | 24.0 |
| ��һ�� | 3.96 | 7.44 | 10.44 | 12.96 | 15.00 |
������ֽ���ṩ�����ݣ���
(1)ľ���볤ľ���Ķ�Ħ��������
(2)��ֽ���ϴӵ�һ���㵽���һ����ľ�����49.2cm����ֽ������������֮��Ӧ�ж��ٸ��㣿
23����16�֣�. ��ͼ�������ϵ�һ��Ͷ����ҵ���е��Ϻ��Ÿ��г�������·��31.5km������ٶȿɴ�430km.h����119.4m/s��������ȫ��ֻ��8min�����ǿ����������ø�����Լ15cm������Ϊ���ɡ������Ľ�ͨ���ߣ����ݳ�������ʾ������ʾ��ʱ�̺��ٶ�ֵ�����������±���ʾ����������;��
 |
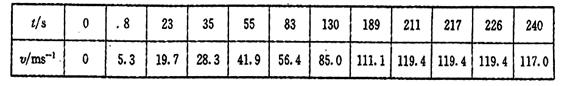 |
 �����г���������Ϊ3��104kg���г��Խϸ��١� ������ʱ���ܿ����������ã��ҿ����������ٶȵ�ƽ�������ȣ���
�����г���������Ϊ3��104kg���г��Խϸ��١� ������ʱ���ܿ����������ã��ҿ����������ٶȵ�ƽ�������ȣ���![]()
��1��ʹ�г�����Ҫ�����ٹ���
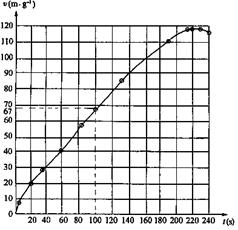
��2�������г���0~240s�ڵ�v-tͼ��
��3�������г�������ٶ�����ʱ��ǣ����
��4������100s ��һʱ�̣��г�ǣ������˲ʱ����
24����18�֣�. ��ͼ��ʾ�����![]() =30�㡢����L=1m���㹻��ΪU��ƽ�й⻬��������̶��ڴŸ�Ӧǿ��B=1T����Χ��ִ����ǿ�ų��У��ų�����ֱ����ƽ��б����.����һƽ�е����ǣ����F��ǣ��һ������m=0.2kg������R=1
=30�㡢����L=1m���㹻��ΪU��ƽ�й⻬��������̶��ڴŸ�Ӧǿ��B=1T����Χ��ִ����ǿ�ų��У��ų�����ֱ����ƽ��б����.����һƽ�е����ǣ����F��ǣ��һ������m=0.2kg������R=1![]() ����ֱ����Ľ�����ab���ɾ�ֹ�ص��������ƶ���ab��ʼ���뵼��Ӵ������Ҵ�ֱ�����Ƶ�����輰һ��Ħ�������ʣ�
����ֱ����Ľ�����ab���ɾ�ֹ�ص��������ƶ���ab��ʼ���뵼��Ӵ������Ҵ�ֱ�����Ƶ�����輰һ��Ħ�������ʣ�
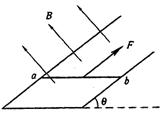 ��1����ǣ����Ϊ��������F=9N����������ﵽ���ȶ��ٶ�v1
��1����ǣ����Ϊ��������F=9N����������ﵽ���ȶ��ٶ�v1
��2����ǣ�������ʺ�Ϊ72W����������ﵽ���ȶ��ٶ�v2
��3����������������������б�浼���ϴﵽijһ�ٶ�ʱ������ ͻȻ�������˺��������ǰ����0.48�� ,��䣬��������
������Ϊ0ʱֹ������������1.12J.������ʱ����v3���
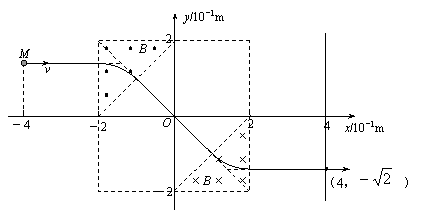
25.��21�֣���ͼ��ʾ����ֱ������ϵ�ĵڢ����͵ڢ������е�ֱ�������������ڣ��ֲ��ŴŸ�Ӧǿ�Ⱦ�ΪB��5.0��10��2T����ǿ�ų�������ֱ�ֱֽ��������������Ϊm��6.64��10��27�K�������Ϊq����3.2��10��19C�Ħ����ӣ����Ʀ��������������ɾ�ֹ��ʼ�����ٵ�ѹΪU��1205V�ĵ糡��ͼ��δ���������ٺ������M����4��![]() ����ƽ����x�������˶������Ⱥ�ͨ����ǿ�ų�����
����ƽ����x�������˶������Ⱥ�ͨ����ǿ�ų�����
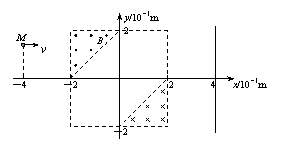 ����������������ڴų��е��˶��뾶��
����������������ڴų��е��˶��뾶��
��������ͼ�л��������Ӵ�ֱ��x����4��ֱ��
x��4֮����˶��켣������ͼ�б����켣��ֱ��
x��4��������ꣻ
������������������ų�����ƫת���õ���ʱ�䡣
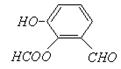
26����16�֣�A��B��D��E�����ڱ���ǰ20��Ԫ�أ����ǵ�ԭ��������������EA2��ˮ��Ӧ������ȼ������Ͱ�ɫ��״���ý�״����ͨ��AB2����ɵ���һ��ɫ�����B��Dͬ���壬D����������E�������Ӿ�����ͬ�ĺ�������Ų�����ش�
��1��д��Ԫ�ط��ţ�A���������� ��B������������ ��
��2����֪AD2��AB2�Ľṹ���ƣ�AD2�ĽṹʽΪ���������������� ���������� ���÷����������������� ������Է��ӡ��Ǽ��Է��ӡ�����
��3��þ����AB2��ȼ�յĻ�ѧ����ʽΪ______________________________________��
��4����D���ʷ���ŨHNO3�м��ȣ����ɺ���ɫ�����һ��ǿ�ᣬ�÷�Ӧ�����ӷ���ʽΪ������������������ �������������������������������������������� ��
��5��A���γɶ�Ԫ����H2A2O4��0.1 molH2A2O4��100 mL 2 mol/L��KOH��Һ��Ӧ����Һ�е�����Ũ���ɴ�С������˳�������������������� �������������� ��
27����15�֣��ҹ��ڶ�������֤���õ��Ǿ�����ɫ�����������ܵ�PETG�²��ϣ�PETG�²��Ͽ��Ի��������ã����Ҷ��ܱ����������κ���Ⱦ��PETG�Ľṹ��ʽ���£�
��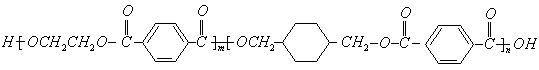
�� ���ֲ��Ͽɲ�������ͼ��ʾ�ĺϳ�·�ߣ�
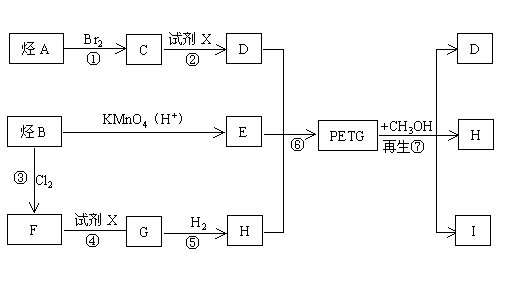
��1��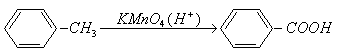
��
��2��![]() �����÷�ӦΪȡ����Ӧ���Իش��������⣺
�����÷�ӦΪȡ����Ӧ���Իش��������⣺
�� ��1���ߵķ�Ӧ������_____________________��
������2��д��I�Ľṹ��ʽ��____________________________��
������3���ϳ�ʱӦ���Ƶĵ�������ʵ�����![]() _______��______��_____����m��n��ʾ����
_______��______��_____����m��n��ʾ����
������4��д����Ӧ�ڵĻ�ѧ����ʽ��____________________________
������5��д��ͬʱ������������Ҫ���E������ͬ���칹��Ľṹ��ʽ��
�����ٸ�ͬ���칹��ı��������ڵ�����̼ԭ���϶�����ȡ������
�����ڸ�ͬ���칹����һ���������ܷ���������Ӧ��ˮ�ⷴӦ������![]() ��Һ����ɫ��
��Һ����ɫ��
����
________________��______________��__________________��
28����15�֣����������ʵ��װ��ͼ����Щ�����ļг�װ��δ�������ش��й����⣺
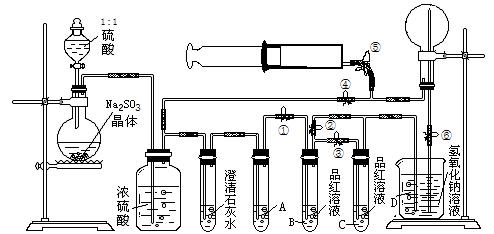
��1�����ȴ�ֹˮ�Тܺ͢ޣ��ر�����ֹˮ�У������ұ���ƿ�¶˵ij�ֱ���ܴ������аγ���Ȼ���Һ©������ʹ���Ỻ��������ƿ����Ӧ�Ļ�ѧ����ʽΪ��____________________�� ____________��
��2��ȷ����ƿ�������Ѿ������ر�ֹˮ�Тܢޣ���Ѹ�ٴ�ֹˮ�Тٺ͢ڣ�Ȼ���¶˵��ܲ��������С�A�Թ��е��Լ���Ϊ�˼�������Ļ�ԭ�ԣ����¿�ѡ�õ��Լ���_______________��
A��˫��ˮ�� B����ˮ���� C�����Ը��������Һ��
D��Ũ���ᡡ E��ϡ���ᡡ��F���μ��˼���KSCN���Ȼ�����Һ
G���μ��˼���KSCN���Ȼ�������Һ
��3����Ӧ�����ر�ֹˮ�Тٺ͢ڣ�����ֹˮ�Тۣ�Ȼ���B�Թܼ��ȣ���B��C���Թ��е�������______________����ԭ���� __________________________��
��4����ֹˮ�Тݺ͢���ע��������ʢ����Ѹ��ע����������ƿ�У���ʱ��ƿ�в�������Ȫ��������ע��������ʢ��һ���������壬��������_____(�ѧʽ)����ע��������ʢ��һ��ǿ����Һ���йط�Ӧ�����ӷ���ʽΪ��_________________����ע��������ʢ����SO2���壬��SO2ע��һ��������ƿ�У��ܷ��������Ȫ������______(��ܡ����ܡ�)����ԭ����___________________________��
29����15�֣���ѧ����Դ����������������ʮ�ֹؼ������á�
���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壬�ҹ��Ϻ������м���ḻ�ġ���ȼ������Դ��
�ٽ�����ȼ�����Ӻ���ȡ��������ȼ�������ڻ����ų��������塣������ѧ�����ʽṹ֪ʶ���Խ��ͣ������������������������������������������������������� ��
��ȡ356g����ʽΪCH4��9H2O�ġ���ȼ�����������ͷŵļ�����ȫȼ������Һ̬ˮ���ɷų�1780.6kJ�����������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ���������� ����������
��������������������������������
����Ƴ�ȼ�ϵ��ʹҺ��ʯ��������ֱ�Ӳ��������������������ս�ԵĿ���֮һ���������������һ��ȼ�ϵ�أ�һ���缫ͨ���������һ�缫ͨ��Һ��ʯ��������C4H10��ʾ����صĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2�����ӡ�
����֪�õ�صĸ�����ӦΪC4H10��13O2�D�D26e�D��4CO2��5H2O����õ�ص�������ӦʽΪ���������������� ����ع���ʱ�������������O2�������� ���ƶ���
��Һ��ʯ����ȼ�ϵ�������ϰ���������Ӧ����ȫ���������������� ����д���ʵ����ƣ������缫������ͨ����
����Դ�Ľ�ȱ�ںܴ�̶�����Լ���ҹ��ľ��÷�չ�������������ҹ���Դ��ȱ��������㽨���������������������������������������������� ��
30����16�֣����мס������ֿ�����һ�����ԵĻ�ѧ���ʣ�ʵ�����о���Ա��ͨ������ϸ�������ķ��������������Ƿ��ж��Բ��Ƚ϶��߶��Ե�ǿ����������һ���о���Ա�����ݲ�������о����������ʵ�鱨�沢�ش��й����⡣
I��ʵ��ԭ����������������������������������������������������������������
�������������������������� ���������ֱ���ϸ��ռȫ������ϸ���İٷ��������³�Qֵ�������жϸû�ѧ���ʵĶ��ԡ�
II��ʵ����ϣ����С������̥��
III��ҩƷ�þߣ��ȵ���øҺ������ϸ������Һ������ϸ���̶�Һ������Ũ�ȵ���������Һ���ιܡ�������������ƿ�������䡢�ز�Ƭ���Dz�Ƭ��������С����������˿���Ѹ�ʱ�ڵĸ߱�����Ƭ��
IV��ʵ�鲽�裺
��1�������� �Ʊ�ϸ������Һ��
�ѻ��С������̥�����������м��飬ת����ƿ�У������ȵ���øҺ������ʹ��̥��֯��ɢ�ɵ���ϸ�����ټ��붯��ϸ������Һ���Ƴ�ϸ������Һ��
��2�������� ����ϸ��������
��ȡA��B��C�����ྻ������ƿ���������������� �������������������� ��
����A��B������ƿ�зֱ��������Ļ�ѧ���ʼס��ң���������ƿҡ�ȡ�
���������������������������������������������� ��
��3�������� ������ʱװƬ��
�ٵ�ϸ����ֳ����Լ8������ʱ��ͬʱ�Ӻ�������ȡ����������ƿ�����ȵ���øҺ������ʹ������ϸ����ƿ�������䣬�ټ��붯��ϸ���̶�Һ��Ѹ��ɱ��ϸ�����̶�ϸ�������ࡣ
�ھ���һ��ʱ��ֱ�Ӹ�����ƿ�ײ���ȡ������ϸ������Һ������������ƿ����ͬ��ŵ��ز�Ƭ�����룬������������������������������������ ��3~5min���ϸDz�Ƭ��
��4�������� �����ͳ�ƣ�
����ʱװƬ���������£����õͱ������ø߱�����Ѱ�Ҵ��������������� �ڵ�ϸ���������������������������������������������������������������� �Ա���ȷ�Ϸ������������ϸ����ͬʱͳ�Ƹ��ڱ����ϸ��ռ����ϸ�������İٷ�����Qֵ����
V�������������ۣ�
���о���Աʵ���֪��A��B��C��������ƿ��Qֵ����Ϊ��QA=1.3%��QB=12.5%��QC=0.1%���ɴ˿�֪��ʵ��Ľ�����������������������������������������������
�������������������������������������������������������������� ��
VI���ش����⣺
��ʵ���У�C����ƿ�����������С����������ϸ����˿���Ѹ�ʱ�ڸ߱�����Ƭ�кβ�ͬ����������������������������������������������������������������������
�������������������������������������������������������������� ��
31����26�֣�ˮ����ȫ������Ҫ����ʳ���ά���������ϰ����˿ڵ����档��������в��ϻش��й����⣺
 �� ��1���ҹ�Ŀǰ�㷺��ֲ���ӽ�ˮ�������з�������ǿ�������Ըߡ������ߵ��ص㡣ˮ������ֳ��ʽ��_______________��������ֳ��ʽ���ص���_________________������ӽ�ˮ�����Ŵ�ѧԭ����________________��
�� ��1���ҹ�Ŀǰ�㷺��ֲ���ӽ�ˮ�������з�������ǿ�������Ըߡ������ߵ��ص㡣ˮ������ֳ��ʽ��_______________��������ֳ��ʽ���ص���_________________������ӽ�ˮ�����Ŵ�ѧԭ����________________��
�� ��2��2001��10�£��ҹ������������������ˮ��������ġ��������ͼ�������ݿ⣬��ͼ��ʾΪˮ������ϸ��Ⱦɫ��ͼ����ˮ��������IJ�������У���Ҫ�ⶨ��ϸ����__________��Ⱦɫ������������Ⱦɫ�塣����ͼ��ʾ����ijһƷ��ˮ������ϸ���е�Ⱦɫ����ɣ���������ֻ��۵�ˮ��ֲ����ͨ��________���ַ�ʽ���������ġ�
�� ��3���±��ǿ�����Ա����������ˮ���ӽ�ʵ���ͳ�����ݣ�D��d��ʾˮ����ߵ��ԡ����Ի���T��t��ʾ���Ե��ԡ����Ի��ݱ��ش��������⣺
| �ױ���� | F1�������ͺ����� | ||||
| ���� | ������ | �߾����� | �߾���Ⱦ�� | �������� | ������Ⱦ�� |
| �� | �߾��������������� | ||||
| �� | �߾�����������Ⱦ�� | ||||
| �� | �߾���Ⱦ������������ | ||||
������ ������������״�У�������״��_____________��
�ڻ�ô��ϰ�������������������ӽ�����У��ױ��Ļ�������________��
�����������ֻ��������е��ױ���Ҫ�����ʱ������������������ˮ����Ӧѡ��______________���ֵķ���������ʱ����Ļ���Ӧ����_________��������ĸ����F1����
��5�������� ��ѧ������Ѹ������Ĺ̵�����ת�Ƶ�С���ϵ�������У���ȡ�������̵��Ļ��������_________���������ع̵�����Ĺ��߿�����_____________________�����γ�����DNA�Ĺ����У���ʹ����DNA����ĩ��֮��ķ�϶����ӵ�������_________�������һ�����ܹ�ʵ�֣������̵������Ƿ������Խ�ת����С���ϵ������������______________�������ϣ��۲����Ƿ��ܹ����档
����𰸣�
1��D��2��C��3��A��4��D��5.B
30����16�֣��𰸺������֣�
�ж����ʼ���ϸ������Һ�������Ķ���ϸ���ᷢ��Ⱦɫ��ṹ����Ŀ�ı��졣
�ֱ���������ϸ������Һ
��3������ƿ����37�棨�������¶ȣ��ĺ�����������
��1~2��������ҺȾɫ
��˿�������ڡ��� С��������ϸ����˿�������ڸ߱�����Ƭ
�ס������ֻ�ѧ���ʾ��ж��ԣ����ҵĶ��ԱȼĶ��Դ�
Cƿ��ΪA��B��ƿ�Ķ����飬��������á�
31����26�֣��𰸺������֣�
�� ��1��������ֳ������߱������ױ����Ŵ���״�����и�����������ͱ����Ի�������
�� ��2��1�����
�� ��3���ٸ߾��Ϳ����� ��DdTt �� ddTt���� �۵����塡 F1
�� ��4����ǹ�����˹��ϳɷ��������� ������
��������������DNA����ø��������
��ѧ�𰸣�
6-13ADCBBCCB
26����15�֣�
�� ��1��C��2�֣���O��2�֣�
|
|
|
|
|
|
[c (HC2O4 )��c (H+ )λ�õߵ����۷�]
27. ��15�֣�
������1��ȡ����Ӧ��2�֣� ��2��![]() ��2�֣�
��2�֣�
������3����������������2�֣�
|
��5��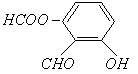
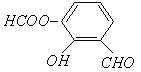 ��������������
��������������
��ÿ��2�֣���6�֣�
28����1��H2SO4��Na2SO3��Na2SO4��SO2����H2O�������������������� ��2�֣�
��2��B��D��F�������������������������������������������������������� ��3�֣�
��3��B�ָܻ�Ϊ��ɫ��C�ܺ�ɫ��dz������Ϊ��ɫ�������������������������� ��2�֣�
SO2��Ʒ�����ɵ���ɫ���ʲ��ȶ��������ֽ⡣���������������������� ��2�֣�
��4��H2S����1�֣���SO2��2OH����SO32-��H2O�����������𰸾��ɣ���2�֣����ܣ���1�֣�
SO2ѹ���������ձ��е�NaOH��Һ�Ӵ���Ѹ�����գ�ʹ��ƿ�ڲ�����ѹ���Ӷ���������Ȫ�������������������������������������� ��2�֣�
19���Ţٸþ����Ƿ��Ӿ��壬�����Ӽ���ڽ����ķ��Ӽ����������ʡ���ȼ�����۷е�ϵͣ�3�֣�
��CH4(g)��2O2(g)��CO2(g)��2H2O(1)����H����890.3kJ/mol��3�֣�
�Ƣ�O2��4e��2 O2�C��2�֣������ƶ� ��2�֣� �ڹ���̼����̿���� ��2�֣�
��Ѱ������Դ�����ȼ�ϵ�ȼ��Ч�ʵȣ�3�֣�
�����𰸣�
���
14��B��15��B��16��BD��17��AC��18��A��19��D 20��AD��21��B
22����1���ɴ��ϵļ������֪��ľ����ǰһ��ʱ����������ֱ���˶����ٶ�Ϊv=![]() =
=![]() =1.2m/s����������3�֣�
=1.2m/s����������3�֣�
��ɰͰ���غ����ȼ���ֱ���˶������ٶ���Ϊa���ɦ�s=aT2���ɵü��ٶ�Ϊ
![]() ��3.0m/s2��������3�֣�
��3.0m/s2��������3�֣�
ɰͰ���غ�ľ���ڳ�ľ����ˮƽ����ֻ�ܻ���Ħ���������ã����ȼ���ֱ���˶����С�����
��mg=ma������
��ö�Ħ�����������̣�0.3��������3�֣�
��2����ľ��ӵ�һ�������㵽���ͣ������ǰһ��������ֱ���˶���ʱ����Ϊt1����һ�����ȼ����˶���ʱ����Ϊt2����λ��
s=vt1+vt2- at22 /2������v=at2����������4�֣�
����s=49.2cm�����t2=0. 40 s ,t1=0.21s������2�֣�
�ӵ�һ�������㵽���ͣ����������ʱ����ĵ���Ϊn=![]() =30.5��
=30.5��
ֽ�ϴӵ�һ���㵽���һ�����ĵ���Ϊ30������2�֣�
23.��1��W=mgh=3��104��100.5J=4.5=104J��������������������������3��
��2������ͼ��ʾ����������������������������������������������������������������������������������
��3������ٶ�����ʱ�ӽ�����ֱ���˶�
F=![]() ��������������������������������3�֣�
��������������������������������3�֣�
��4��100sʱ˲ʱ�ٶ�Ϊ67m/s����ʱͼ�����ֱ�ߣ��г����ȼ��Ӽ����˶���
���ٶ�a=![]() ����������������������������������������
����������������������������������������
 |
��ʱ����λ![]() ��ǣ����ΪF������ţ�ٵڶ����ɣ�F-
��ǣ����ΪF������ţ�ٵڶ����ɣ�F-![]() ��
��
������ F=![]() ����2��
����2��
![]() ����������������������������������
����������������������������������
��������������������������ʱ��
�ƣ��������ȣ��£ɣ�
�����������ȣ����������������ҡ��æ���������������������6��
�������������㹦������������ʱ��
�ƣ��У���������������������������������������������������������������������������������������������������
�������У��������������ȣ�����������������
������������������������������������������������������������������������
�������������賷�������ǰ���е�������Ϊ��,�˹��̷���Q,��
������������������ӣ���ȣ���
����������������������������������������������������������������������������������������������������6�֣�
�������Ŧ������ڵ糡�б����٣��ɶ��ܶ����� ![]() ������������3��
������������3��
�������ڴų���ƫת����ţ�ٵڶ����ɵ�
![]() ��������
3��
��������
3��
�������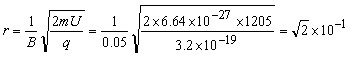 ��m����3��
��m����3��
������ȷ����ͼ��á�����������������6��
 |
�Ǵ��������ڴų��е��˶�����
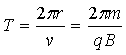 ����������3��
����������3��
�������������ų��зֱ�ƫת�Ļ���Ϊ![]() ���ڴų��е��˶���ʱ��
���ڴų��е��˶���ʱ��
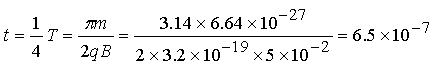 ��s�� 3��
��s�� 3��
��������Դ����(5.17)
��� �������� ���������������� ѧ�� ����������
һ.ѡ����
| ��� | 1 | 2 | 3 | 4 | 5 |
| �� |
��.�����
30��
I������������������������������������������������������������������������������
�������������������������������������������������������������������� ��
IV�������� ��������������������������������������������������������������������
���������������������������������������������������������������������������� ��
��
��3������������������������������������������������������������������������������
��4������������������ ��������������������������������������������������������������
V������ ���������������������������������������������������������������������������� ������������������������������������������������������������������
VI������������������������������������������������������ ��������������������
31����1������ ����������
��
�� ����������������������������������������������������������������������
��
��2���������� ������������������������
��3������������������ �� �������������� ������������������������������ ��
��4���������������������������� �������������������������������� ������������
������������������������������ ��������������������������