高三教学化学上学期阶段性质量检测3
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 K39 Ca 40 Mn 55 Fe 56 I 127 Ba 137
第I卷 (共64分)
一、单项选择题(本题包括8小题,每小题4分共32分。每小题只是一个选项符合题意)
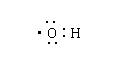 1、下列化学用语表示错误的是 ( )
1、下列化学用语表示错误的是 ( )
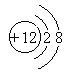
A、镁离子结构示意图 B、羟基电子式
![]()
![]()
C、次氯酸电子式 D、氨分子结构
2、关于反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O的有关叙述中,正确的是 ( )
A、KCl中含有35Cl B、生成物Cl2的相对分子质量为73.3
C、该反应转移的电子数为6e- D、氧化剂和还原剂的物质的量之比为1:6
3、炽热的炉膛内有反应:C(s)+O2(g)==CO2(g);△H = -393.5KJ/mol,往炉膛内通入水蒸气时,有如下反应:C(s) +H2O(g)==H2(g)+CO(g);△H = +131KJ/mol,CO(g)+1/2O2(g)==CO2(g);△H = -283KJ/mol,H2(g)+1/2O2(g)==H2O(g);
△H =-241.8KJ/mol,由以上反应推断往炽热的的炉膛内通入水蒸气时( )
A、不能节省燃料,但能使炉火瞬间更旺B、虽不能使炉火瞬间更旺,但可以节省燃料
C、既能使炉火瞬间更旺,又能节省燃料D、既不能使炉火瞬间更旺,又不能节省燃料
4、科学家最近发现两种粒子:第1种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第2种是由四个氧原子构成的分子。下列有关这两种粒子的说法不正确的是 ( )
A、“四中子”不显电性
B、“四中子”的质量数为4
C、第2种粒子是氧元素的另一种同位素
D、第2种粒子的化学式为O4
5、利用某些有机物的同分异构体间的转化可用来贮存热能,如原降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应:
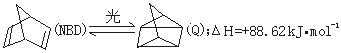
下列说法不正确的是 ( )
A.、NBD、Q、甲苯三者互为同分异构体
B、NBD可开发为贮能材料
C、46克NBD经太阳光照射完全转化成Q时需吸收44.31 kJ热量
D、 NBD、Q、甲苯三者可能是同系物
6、下列实验中,溶液颜色有明显变化的是 ( )
A、少量明矾溶液加入过量NaOH溶液中
B、往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C、少量Na2O2固体加入到过量NaHSO3溶液中
D、往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
7、下列实验能达到预期目的的是 ( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;②用NaOH溶液除去苯中的少量苯酚;
③用饱和NaHCO3溶液除去CO2中的少量SO2;④用加热的方法提取NH4Cl固体中混有的少量碘;⑤用醋和澄清石灰水验证蛋壳中含有碳酸盐;⑥用米汤检验食用加碘盐不含碘;
⑦用碘酒验证汽油中含有不饱和烃;
A、①②⑥⑦ B、①③⑤⑥⑦
C、②③⑤⑦ D、②③④⑤⑦
8、将一定量的钠铝合金置于水后,合金全部溶解,得到20 mL、pH=14的溶液,然后用1 mol・L-1的盐酸滴定到沉淀质量最大时,消耗40 mL的盐酸。原合金中钠的质量为 ( )
A、0.92 g B、0.69 g C、0.46 g D、0.23 g
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
9、下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
A、盐酸、水煤气、醋酸、干冰
B、冰醋酸、福尔马林、硫酸钠、乙醇
C、单甘油酯、混甘油酯、苛性钠、氯气
D、胆矾、漂白粉、氯化钾、氯气
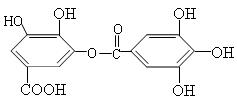 10、某有机物的结构简式如下图所示,对该有机物的下列叙述中不正确的是(
)
10、某有机物的结构简式如下图所示,对该有机物的下列叙述中不正确的是(
)
A、常温下,能与Na2CO3溶液反应放出CO2
B、在发生碱性水解时1mol该有机物能消耗8molNaOH
C、与稀硫酸共热时可生成两种有机物
D、 该有机物的分子式是C14H10O9
11、下列反应的离子方程式正确的是 ( )
A、等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:
Ba2++2OH―+H++NH4++SO42―=BaSO4↓+NH3・H2O+H2O
B、氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O
C、足量的CO2通入饱和碳酸钠溶液中:CO2+CO32―+H2O=2HCO3―
D、向碳酸氢钠溶液中滴入过量澄清石灰水:
Ca2++2OH―+2HCO3―=CaCO3↓+CO32―+2H2O
12、设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A、1mol金刚石晶体中含碳碳键数为4 NA
B、常温常压下,32克的O2和O3混合气体中氧原子数为2NA
C、标准状况下,22.4LSO3中含有的氧原子数约为3 NA
D、1molH2O2与足量SO2反应转移的电子数2NA
13、下列各项实验操作正确的是 ( )
A、实验室规定:所有实验剩余的药品均不应放回原药品瓶内
B、为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
C、在转移固体需使用玻璃棒
D、为了防止容量瓶漏水,可在玻璃塞上涂上凡士林
14、分别配制H3PO4、KOH的乙醇溶液,取10 mL H3PO4乙醇溶液后不断振荡并滴加KOH乙醇溶液,立即产生白色沉淀,并不断增多,继而又逐渐减少至消失,然后又逐渐增多至一定量不再消失。以上事实说明 ( )
A、K2HPO4不溶于无水乙醇 B、KH2PO4、K3PO4不溶于无水乙醇
C、KH2PO4、K2HPO4不溶于无水乙醇 D、K2HPO4溶于无水乙醇
15、下列画有横线的物质在反应中不能完全消耗的是 ( )
A、将含少量CO2的CO气体通入盛有足量的Na2O2的密闭容器中,并不断用电火花引燃
B、将1mol Mg置于10L空气中(标况),使之在高温下反应
C、将1mol Cu置于含2mol H2SO4的98%的浓硫酸中加热
D、在强光持续照射下,向过量的Ca(ClO)2悬浊液中通入少量CO2
16、已知相同温度时,同浓度的HCO![]() 的电离程度大于HS―的电离程度。将0.1
mol・L―1的盐酸缓慢滴入0.1
mol・L―1 的Na2S溶液中,当等体积混合后,溶液中下列粒子浓度的大小关系正确的是
( )
的电离程度大于HS―的电离程度。将0.1
mol・L―1的盐酸缓慢滴入0.1
mol・L―1 的Na2S溶液中,当等体积混合后,溶液中下列粒子浓度的大小关系正确的是
( )
A.c(Cl―)>c(HS―)>c(H+)>c(OH―) B.c(Cl―)>c(H2S)>c(HS―)>c(OH―)
C.c(Cl―)>c(HS―)>c(H2S)>c(S2―) D.c(Cl―)>c(S2―)>c(HS―)>c(H+)
第II卷(86分)
三、填空
17、根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
(1) 有下列仪器,本实验中需要的仪器是(填写字母) ,除上述仪
器外,还需要的仪器是(填仪器名称): ;
A.带砝码的托盘天平 B.研钵 C.试管夹 D.酒精灯 E.蒸发皿
F.玻璃棒 G.坩埚 H.干燥管 I.石棉网 J.三角架
(2)本实验至少需要加热 次,至少需要称量 次;
(3)某学生实验得到以下数据:加热前容器的质量为m1,容器和晶体的总质量为m2,加热后容器和无水CuSO4的总质量为m3。请写出结晶水含量(ω)的计算公式并求出CuSO4・nH2O中n的值(用ml、m2、m3表示):ω= ,n = ;
(4)若ml = 5.4g、m2 = 7.9g、m3 = 6.8g,该生结果 (填“偏高”或“偏低”)?
从下列分析中选出该生实验产生误差的原因可能是(填写字母) 。
A、加热前称量时容器未完全干燥 B、最后两次加热后的质量差大于0.1g
C、加热后容器未放在干燥器中冷却 D、加热过程中有少量晶体溅出
 E、加热后的粉末中有少量黑色固体
E、加热后的粉末中有少量黑色固体
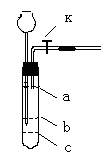
18、现有一套简易的气体发生装置(如右图所示,
其中活塞已打开)。
(1) 甲、乙两同学分别设计了如下实验方案以检验其气密性是否良好。
甲:把导气管插入一盛水的水槽中,双手捂住试管外壁, 过一会儿,
若看到试管末端有气泡冒出,松开手后又看到导管内有一段水柱,
则说明该装置的气密性良好。
乙:往漏斗中注入一定量的水,直到浸没长径漏斗下端。然后关闭活塞K,用手捂住试管
中上部(气体部分),一会儿若看到漏斗液面上升到一定高度,再重新打开活塞让液面回落,
并迅速关闭活塞K,松开手,又看到漏斗中液面低于试管中液面且不再升降。则说明该装
置气密性良好。
①甲、乙的设计方案中不可行的是 (填“甲”、“乙”或“甲和乙”),理由是: 。
②丙同学认为,只要往漏斗中加水,便可检验其气密性是否良好。经检验他的方案是可行的。则他的方案是: 。
(2) 若用该装置制取氢气,反应原理为:Zn + H2SO4 = ZnSO4 + H2↑。
试简述其实验操作步骤:
。
(3)若要将上述装置改成可随时控制反应和停止的气体发生装置,则需在试管里增设一带
小孔隔板,你认为隔板应装在 (填a、b、或c)处。
19、某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 gCuSO4・5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
⑴上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤①、③中研磨固体所用仪器的名称是___________________;
⑵步骤③中洗涤沉淀的操作是______________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
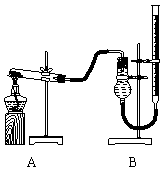 用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2 g | 无其他物质 | |
| ⑤ | 1.2 g | CuO 0.5 g | |
| ⑥ | 1.2 g | MnO2 0.5 g |
回答下列问题:
⑶上述实验中的“待测数据”指_____________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,__________________________________________
___________________________________
_________________;
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a、_______________________________,b、 。
20、有四种同主族物质,它们的沸点(℃,1.01×105pa)如下表所示:
| ① | He -268.8 | Ne -249.5 | Ar (x) | Kr -151.7 |
| ② | F2 -187.0 | Cl2 -33.6 | (a) 58.7 | I2 184.0 |
| ③ | HF (y) | HCl -84.0 | HBr -67.0 | HI -35.3 |
| ④ | H2O (z) | H2S -60.2 | (b) -42.0 | H2Te -1.8 |
试根据上表回答:
⑴a为 色液体;b的分子式是:
⑵写出②系列中物质主要化学性质的递变规律(任定一种): ;能够说明该递变规律的化学事实是: ;(任举一例,用离子方程式表示)
⑶除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是:
⑷上表中,和两种物质的沸点较同系列其他物质反常,反常的主要原因是
21、在现代生活中,人们越来越注意微量元素的摄入。碘元素对人体健康有着至关重要的作用。为预防碘缺乏病,我国卫生部规定每千克食盐中应含有40~50 mg KIO3。回答下列问题:
(1)加碘食盐的包装袋上通常标有如下食用建议:勿长时间炖炒。其包含的原理是
(2)KIO3可用电解的方法制得,原理是:以石墨为阳极,以不锈钢为阴极,在一定温度和电流下电解KI溶液。总反应方程式为KI+3H2O===KIO3+3H2↑,则两极的电极反应式分别为:阴极_____________________,阳极______________________。
(3)为检验某食盐中是否含有KIO3,某同学取食盐样品428 g完全溶解于水中,然后加入用盐酸酸化的淀粉-KI溶液,结果溶液呈蓝色,则反应的离子方程式为__________________。为进一步确证样品是否为合格产品,该同学又用0.030
mol・L-1的Na2S2O3溶液滴定,当用去18.00 mL时蓝色刚好褪去(反应方程式为I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() ),由此可判定该加碘食盐为 ______________(填“合格”或“不合格”)产品。
),由此可判定该加碘食盐为 ______________(填“合格”或“不合格”)产品。
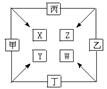 22、甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,转化关系如图所示,又知:
22、甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,转化关系如图所示,又知:
①甲、乙、丙均为前三周期元素的单质,常温下均为气态;丁是日常生活中的一种常见金属。
②常温下,X是无色液体,Y是黑色固体,
③丙在乙中燃烧发出苍白色火焰,丁在乙中燃烧生成棕黄色的烟,W的水溶液呈黄色。
请填空:
(1)丁在甲和X同时存在的条件下,可以被腐蚀,写出电极反应方程式:
负极: 正极: 。
(2)将少量W的浓溶液滴入热的X中,反应的化学方程式为: 。
(3)将Y看成碱性氧化物,Y与Z的溶液发生反应的离子方程式是: 。
(4)若一定条件下丁分别与X、Z发生反应生成等物质的量的气体,则消耗丁的物质的量之比为 。
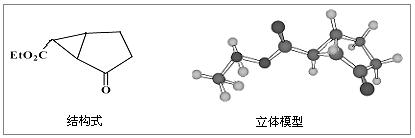
23、下图是某药物中间体的结构示意图:
试回答下列问题:
⑴观察上面的结构式与立体模型,通过对比指出结构式中的“Et”表示 ;该药物中间体分子的化学式为 。
⑵请你根据结构示意图,推测该化合物所能发生的反应及所需反应条件 。
⑶解决有机分子结构问题的最强有力手段是核磁共振氢谱(PMR)。有机化合物分子中有几种化学环境不同的氢原子,在PMR中就有几个不同的吸收峰
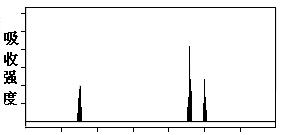
现有一种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如上图所示,试写出该化合物的结构简式: 。
四、计算
24、有一瓶白色固体,取少量置于试管中加热,固体逐渐消失,放出水蒸气和其他两种气体,试管内除管口有少量水珠外,没有任何残留物.取0.350g这种固体跟过量的碱液反应,生成一种能使湿润红色石蕊试纸变蓝的气体,这些气体正好能和30.0mL 0.1mol/L硫酸完全反应;另取0.350g该固体跟足量的盐酸反应,放出一种无色无臭气体,将这些气体通入过量的澄清石灰水,得到0.400g白色沉淀。
(1)计算0.350g该固体中含有的阴离子和阳离子的物质的量。
(2)根据实验及计算结果确定白色固体是什么?写出判断的依据。
25、某课外兴趣小组决定开展研究,寻求可行的方法,鉴别某样品是亚硝酸钠还是氯化钠。为解决这一问题,该小组查阅了大量的资料,对亚硝酸钠的性质做如下归纳:亚硝酸钠,化学式为NaNO2,是亚硝酸(HNO2,一种弱酸)的钠盐;白色粉末,易溶解在水中,有毒,容易潮解。由于亚硝酸钠中的氮元素处于中间价态,既有氧化性(在酸性条件下会氧化KI,得到碘单质),又有还原性(在酸性条件下,会被KMnO4酸性氧化),大量用于防锈、印染……
甲设计方案如下:取少量固体,配成溶液。往溶液中滴加少量KMnO4酸性溶液,观察溶液是否褪色。如果褪去,说明该样品为亚硝酸钠。反应表达式为:
______MnO![]() +______NO
+______NO![]() +______H+====______Mn2+______NO
+______H+====______Mn2+______NO![]() +______H2O。
+______H2O。
(1)配平上述离子方程式。
(2)甲认为他的方案还可测定样品中亚硝酸钠的含量(假设该样品只含有NaNO3和NaNO2)。过程如下:
Ⅰ、称一定量样品,溶于水置于锥形瓶中;Ⅱ、取0.10 mol・L―1 的KMnO4酸性溶液25.00 mL(过量)倒入锥形瓶中,振荡;Ⅲ、用草酸钠溶液滴定过量的KMnO4酸性溶液;Ⅳ、重复上述操作。各次实验数据如下:
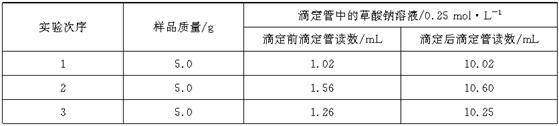 已知:2MnO
已知:2MnO![]() +5C2O
+5C2O![]() +16H+=2Mn2++10CO2↑+8H2O。试计算样品中NaNO2的质量分数(必须列出计算过程,小数点后保留两位数字)。
+16H+=2Mn2++10CO2↑+8H2O。试计算样品中NaNO2的质量分数(必须列出计算过程,小数点后保留两位数字)。
高三教学质量检测
化学试题答题卷 姓名 学号
选择题一、二(共64分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
三、填空(共71分)
17、(1) , ;(2) , ;
(3)ω= ,n = ;(4) ; 。
18、(1)① , 。
② 。
(2)
。
(3)
19、(一)⑴_______________,___________________;
⑵____________________ __________________________
(二)⑶ _________;⑷___________
⑸_________________________________ ___________________________________ ;
⑹_______________________________, 。
20、 (1) ;
(2) _____ ______ __________, ________________ ______
(3) _____________
(4)__________ ___
21、⑴
⑵ 、
⑶ 、
22、(1) ; 。
(2) 。
(3) 。(4) 。
23、(1) ; ⑵ ⑶
四、计算(共15分)
24、
26、
参考答案
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| C | B | A | C | D | B | C | A |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| B | C | AB | BD | C | BD | C | C |
![]() 17、(11分)(1)A、B、D、F、G、J(2分,多一少一不得分);泥三角、坩埚钳、干燥器(2分,多一少一不得分) (2) 2(1分)、4(1分); ;(各1分)
17、(11分)(1)A、B、D、F、G、J(2分,多一少一不得分);泥三角、坩埚钳、干燥器(2分,多一少一不得分) (2) 2(1分)、4(1分); ;(各1分)
(4) 偏高(1分);A、D、E(2分)
18、(11分)(1)①甲(2分);长颈漏斗与外界相通。(2分)
②往长颈漏斗中加水使水浸没长颈漏斗下端,关闭活塞,再加水,直至漏斗中液面高于试管内液面,停止加水。若漏斗和试管的液面差保持不变,则说明气密性良好。(3分)
(2)先往试管中加入锌粒,装好装置,再往长颈漏斗中加入稀硫酸直至浸没漏斗下端。(2分)(3)b(2分)
19、(12分)⑴ ①②③ (3分) 研钵 (1分)
⑵沿玻璃棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次
(2分)
⑶时间 (2分) ⑷碱式 (1分)
⑸取一根带火星的木条,伸入干燥管内,看木条是否复燃 (1分)
⑹CuO的质量有没有改变 (1分) CuO的化学性质有没有改变 (1分)
20、(10分)(1)深红棕色(1分);H2Se(1分)
(2)氧化性逐渐减弱(2分);Cl2+2Br-= Br2+2 Cl-(2分)
(3)随着相对分子质量的增大沸点逐渐升高(2分)
(4)HF,H2O分子间易形成氢键(2分)
21、(9分)(1)KIO3在加热或高温下易分解而变质。(2分)
(2)6H2O+6e-===3H2↑+6OH- I-+3H2O-6e-===IO![]() +6H+(每空2分,共4分)
+6H+(每空2分,共4分)
(3)5I-+IO![]() +6H+===3I2+3H2O(2分) 合格(1分)
+6H+===3I2+3H2O(2分) 合格(1分)
22、(10分)(1)Fe―2e-====Fe2+ O2+2H2O+4e-====4OH-
(2)FeCl3
+3H2O![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(3)Fe3O4+8H+====Fe2++Fe3++4H2O
(4)3∶4(每空2分)
23、(8分)⑴乙基 C9H12O3 ⑵与NaOH溶液在加热条件下反应
⑶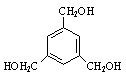 (每空2分,共8分)
(每空2分,共8分)
24、(9分)(1)NH4+:0.006mol、CO32―:0.002 mol 、HCO3―0.002 mol(每个2分)
(2) (NH4)2 CO3、 NH4HCO3(3分)
25、(6分)(1)2 5 6 2 5 3 (2分) (2)5.52%(4分)