高三理综复习化学测试题
6.反应E+F==G在温度T1下进行,反应M+N==K在温度T2下进行,已知T1>T2,且E
和F的浓度均大于M和N的浓度(其他条件均相同),则两者的反应速率
A.前者大
B.后者大
C.一样大
D.无法判断
7.下列操作或试剂中,不可能使溴水变为无色的是
A.CCl4多次萃取
B.镁粉
C.KOH溶液
D.KI溶液
8.t℃时,水的离子积为Kw,该温度下将amol・L-1一元酸HA与bmol・L-1一元碱 BOH等体积混合,要使混合液呈中性,必要的条件是
A.混合液的pH=7
B.混合液中:c(B+)=c(A-)+c(OH-)
C.a=b
D.混合液中:c(H+)=
9.北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的分析正确的是
A.K3C60中既有离子键,又有极性键
B.1mol K3C60中含有的离子数目为63×6.02×1023
C.该晶体在熔融状态下能导电
D.该晶体的熔点比C60低
10.下列说法不正确的是
A.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等
B.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同
C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成
D.将足量Cl2通入NaBr、NaI的混合溶液中,反应后将溶液蒸干并充分灼烧,剩余的固体物质成分为NaCl
11.下列说法不正确的是
①分液漏斗、滴定管、容量瓶在使用前均需检查是否漏水 ②镊子不能用来夹持正在加热或刚加热过的仪器 ③容量瓶上需标明温度、容量、刻度线及浓度 ④用滴定管及量筒分别量取一定量的溶液并俯视读数,结果一定偏高 ⑤用托盘天平(1g以下用游码)称量2.5g药品时,砝码和药品都已放好,发现指针向右偏,应该进行的操作是减少药品
A.①②
B.③④⑤
C.③④
D.④⑤
12.在恒温恒容的密闭容器中,发生反应3A(g)+B(g)![]() xC(g)。
xC(g)。
Ⅰ、将3molA和2molB在一定条件下反应,达平衡时C的体积分数为a;
Ⅱ、若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。
下列说法正确的是
A.当Ⅱ体系起始物质的量满足3 n(C) +8n(A)=12 n(B)时,可确定x≠4
B.若x=2,则Ⅱ体系起始物质的量应满足3n(B) =n(A)+3mol
C.若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大
D.若向Ⅰ平衡体系中再加入3molA和2molB,C的体积分数若大于a,可确定x>4
13.已知t℃时,盐M(不含结晶水,摩尔质量为126g・mol-1)的溶解度为S g。在一定
量的M的水溶液中加入a g M后,恰好为t℃时的饱和溶液,饱和溶液的密度是ρg・mL-1,物质的量浓度是c mol・L-1,质量分数为ω。若用M・7H2O代替M,欲使原溶液在t℃时恰好饱和,则需加入b g M・7H2O,下列等式不正确的是
A.b(100-s)=200a
B.a=b/2
C.126c(100+s)=1000sρ
D.1000ωρ=126c
26.(17分)
Ⅰ.(6分)下列有关化学实验的操作或说法中,正确的是(填写字母代号)_________。
A、配置硫酸铜溶液时应向溶液中加入少量的铜粉
B、进行中和热测定实验时,需要测出反应前盐酸与NaOH溶液的各自温度及反应后溶液的最高温度
C、向某溶液中先通入Cl2再滴加KSCN溶液时溶液变红,证明该溶液一定含有Fe2+
D、制备硫酸亚铁晶体时,向稀硫酸中加入废铁屑至有少量气泡发生时,过滤,然后加热蒸发滤液即可得到硫酸亚铁晶体
E、FeCl3溶液能使淀粉碘化钾试纸变蓝,故能用淀粉碘化钾试纸鉴别黄色的FeCl3溶液和溴水
F、实验室制取肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂
Ⅱ.(11分)今有下列气体:①H![]() ②Cl
②Cl![]() ③CH
③CH![]() ④HCl ⑤NH
④HCl ⑤NH![]() ⑥NO ⑦H
⑥NO ⑦H![]() S ⑧SO
S ⑧SO![]() ,用
,用
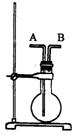 右图所示装置进行实验。
右图所示装置进行实验。
请写下列空白:
(1)当烧瓶干燥时,从B口进气可收集的气体是(填序号)_____________。
(2)当烧瓶干燥时,从A口进气可收集的气体有______种。
(3)若烧瓶充满水,可收集的气体有(填序号)______;此时气体由____口进入。
(4)若烧瓶内装入浓H![]() SO
SO![]() 进行气体干燥,不能用此装置干燥的气体有(填序号)________。
进行气体干燥,不能用此装置干燥的气体有(填序号)________。
27.(12分)
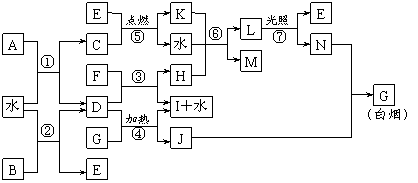
下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
 |
请按要求填空:
⑴G属于_________晶体。
⑵反应⑥的化学方程式是_________________________________________________。
⑶已知C的燃烧热是1300 kJ・mol-1,表示C的燃烧热的热化学方程式是_____________。
⑷根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
28.(19分)
Ⅰ.(10分)下表列出了前20号元素中的某些元素性质的有关数据:
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
试回答下列问题:
(1)以上10种元素形成的单质中,与水反应最剧烈的金属是 (填写编号)。
 (2)上述⑤、⑥、⑦三种元素中的两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质的化学式为
。
(2)上述⑤、⑥、⑦三种元素中的两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质的化学式为
。
(3)某元素R的原子半径为1.02×10-10m,该元素是 ;化合物Na2R2的电子式为_____________________。
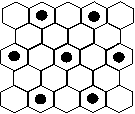
(4)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为 。
Ⅱ.(9分)A、B、C、D均为4种常见的短周期元素,常温下A、B可形成两种常见的液态化
合物,其最简式分别为BA和B2A;B与D可形成分子X,也可形成阳离子Y,X、Y在水溶
液中酸碱性正好相反;C+的焰色反应呈黄色。
⑴液态X类似B2A,也能微弱电离且产生电子数相同的两种离子,则液态X电离方程式为 。
⑵M、N是由A、B、C、D四种元素中任意三种元素组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且M溶液中水的电离程度小于N溶液中水的电离程度。 则M、N分别为(填化学式)___________________;若将0.1mol・L-1M和0.2mol・L-1N两溶液等体积混合所得溶液中离子浓度的大小顺序为____________________________________。
29.(12分)
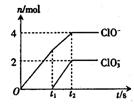 一定量的石灰乳中通入一定量的氯气,两者恰好完全反应,生成
一定量的石灰乳中通入一定量的氯气,两者恰好完全反应,生成
物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线图如图所示。试回答:
(1)t2时Ca(ClO)2与Ca(ClO3)2的物质的量之和为________mol,该
石灰乳中Ca(OH)2的质量是________g。
(2)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通气速率不同,ClO-和ClO3-的比
例也不同,若在原石灰乳中通入氯气速率加快,则反应后n(ClO-)/n(ClO3-)将______(填“>”“<”或“=”)2,若n(ClO-)/n(ClO3-)=a,则n(Cl-)=_________________mol(用a的代数式表示)。
理综化学 参考答案及评分标准
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | D | D | D | C | A | B | B | B |
26.(17分)
Ⅰ.(6分)
B(多答一个扣3分,多答两个得0分)
Ⅱ.(11分)
(1)①③⑤ (答对一种得1分,答对三种得3分,出现错误答案该空得0分,下同)
(2)4 (2分)
(3)①③⑥(3分) B(1分)
(4)⑤⑦(2分)
27.(12分)(每空3分)
⑴离子
⑵Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
⑶CH≡CH(g)+5/2O2(g)→2CO2(g)+H2O(l);ΔH=-1300 kJ・mol-1
⑷CaO2
28.(19分)
Ⅰ.(10分)(每空2分)
(1)②
![]() (2)PCl3、CCl4
(2)PCl3、CCl4
(3)S (或硫)
(4)KC8
Ⅱ. (9分) (每空3分)
⑴2NH3![]() NH4++NH2-
NH4++NH2-
⑵NaOH和NH4NO3
c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)
29.(12分)(每空3分)
(1)3 740
(2)< 10(a+5)/(a+3)
 高三理科综合化学答题卷
高三理科综合化学答题卷
(108分) 2006/11/18
单项选择题(6分×8=48分)
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 |
非选择题(共60分)
 26.(17分)Ⅰ._______。
26.(17分)Ⅰ._______。
Ⅱ.(1)________。 (2)_____。
(3)_________;_____。 (4)________。

27.(12分)(1)_________。
(2)_________________________________________________。
(3)_______________________________________________________。
(4)__________。

28.(19分)Ⅰ.(1)______。 (2)________________。
(3)_______; ________________________。 (4)________。
Ⅱ.(1)________________________。(2)____________________。
(3)____________________________________________。

29.(12分)(1)_______ __________。
(2)________ _____________________。