高三第二次月考理科综合化学部分试题
6.下列说法正确的是
A.新制的干燥氯气能使鲜花褪色
B.SO2只有还原性,没有氧化性
C.NO是棕红色气体,能结合人体血液中的血红蛋白
D.Fe、Mg能在冷的浓硝酸中钝化
7.超临界流体是物质介于气态和液态之间的一种新的状态。目前应用最广的是超临界二氧化碳,在化学工业上可取代氟利昂等溶剂、发泡剂。下列有关超临界二氧化碳的说法中
错误的是 A.超临界二氧化碳是新合成的一种物质
B.超临界二氧化碳由CO2分子构成
C.用超临界二氧化碳溶解物质后,可在常温常压下使二氧化碳挥发除去
D.用超临界二氧化碳代替氟利昂可减轻对臭氧层的破坏
8.下列反应的离子方程式正确的是
A.FeBr2溶液中通入过量Cl2
2Fe2++2Br―+2Cl2=2Fe3++Br2+4Cl―
B.用氨水吸收少量二氧化硫
NH3·H2O+SO2=NH4++HSO3―
C.过量的铁与稀硝酸反应
3Fe+8H++2NO3―=3Fe2++2NO↑+4H2O
D.二氧化硫通入漂白粉溶液
Ca2++2ClO―+SO2+H2O=CaSO3↓+2HClO
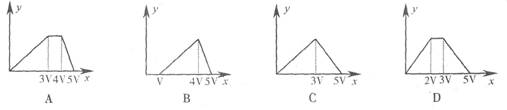 9.将物质的量相等的氯化铝和氯化铵溶于水形成混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液,直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的质量(y)的关系图中正确的是
9.将物质的量相等的氯化铝和氯化铵溶于水形成混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液,直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的质量(y)的关系图中正确的是
10.四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水糟中,发生的现象如下图所示,其中充满Cl2的试管是
|
11.某一无色溶液,若向其中加入足量饱和氯水,溶液呈橙黄色;再向橙黄色溶液中滴加BaCl![]() 溶液,产生白色沉淀;若向原溶液中加入铝粉,有气体放出,该溶液可能大量存在的一组离子是
溶液,产生白色沉淀;若向原溶液中加入铝粉,有气体放出,该溶液可能大量存在的一组离子是
A.K![]() 、H
、H![]() 、NO
、NO![]() 、Na
、Na![]() B.H
B.H![]() 、Br
、Br![]() 、SO
、SO![]() 、Na
、Na![]()
C.SO![]() 、Br
、Br![]() 、OH
、OH![]() 、Fe
、Fe![]() D.H
D.H![]() 、Br
、Br![]() 、SO
、SO![]() 、K
、K![]()
12.2.1g Mg、Al混合物投入足量盐酸中产生2240mLH2(标准状况),然后加入1mol/LNaOH溶液充分反应后,过滤、洗涤、干燥后固体的质量不可能为
A.3.0g B.3.5g C.5.5 D.5.6g
13.某无色溶液可能由Na2CO3、MgCl2、NaHCO3、BaCl2中的一种或几种混合而成,向溶液中加入烧碱溶液出现白色沉淀,加入稀硫酸也出现白色沉淀并放出气体。据此分析,下述组合判断中正确的是
①肯定有BaCl2 ②肯定有MgCl2 ③肯定有NaHCO3 ④肯定有NaHCO3或Na2CO3
⑤肯定没有MgCl2
A.①②③ B.①③ C.②④ D.①③⑤
 26.(16分)材料科学是近年来化学研究的热点之一。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性,它是以中学化学中的常见物质为原料来生产的,如下虚线框外为其生产过程;线框内的其他转化是为探究C的组成而设,G、H均为难溶于水的白色固体;图中C、M、K均含A元素,C物质遇水强烈水解,能生成一种白色胶状物质F和E的酸雾,其余物质均为中学化学常见物质。请回答下列问题:
26.(16分)材料科学是近年来化学研究的热点之一。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性,它是以中学化学中的常见物质为原料来生产的,如下虚线框外为其生产过程;线框内的其他转化是为探究C的组成而设,G、H均为难溶于水的白色固体;图中C、M、K均含A元素,C物质遇水强烈水解,能生成一种白色胶状物质F和E的酸雾,其余物质均为中学化学常见物质。请回答下列问题:
(1)指出K可能所属的晶体类型__________。
(2)写出化学式:单质B________,化合物F__________。
(3)写出上述反应的离子反应方程式:
⑤__________________________________________________________________________
⑥__________________________________________________________________________
(4)写出反应④的化学反应方程式 .
27.(18分)我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉中内外。“侯氏制碱法”的基本做法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱。它的反应原理可用下列化学方程式表示:
|
某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下一套实验装置
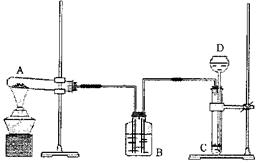
实验室可选药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化铵、氯化钠
(1)选用最合适的试剂的名称A ;D
(2)本实验具体操作过程中,应先通 气体,再通 气体;
原因是
(3)指出该装置的至少两处错误
(4)在改进装置后,该同学进行了实验,实验所用的饱和NaCl溶液中含溶质58.5g,实验最后得到无水碳酸钠26g,则其产率为 ;该同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是
(5)在“侯氏制碱法”的工业生产中,原料的利用率高,大大降低了成本。请问本实验中哪些物质可重复利用?
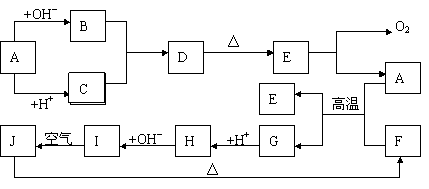 28.(14分)下图中A—J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A—E和F—J中分别含有同一种元素,框图中有的生成物被略去,反应E→A+O2的条件未标出。请填写下列空白:
28.(14分)下图中A—J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A—E和F—J中分别含有同一种元素,框图中有的生成物被略去,反应E→A+O2的条件未标出。请填写下列空白:
(1)化合物H中的阳离子是 ___________;D的化学式是 _________________。
(2)A生成B反应的离子方程式是
__________________________________________。
(3)B和C反应的离子方程式是
____________________________________________。
(4)A和F反应的化学方程式是
____________________________________________。
(5)I→J反应的化学方程式是 _____________________________________,
该反应过程中发生的实验现象是 _________________________________ 。
29.(12分)将Mg粉放入盛有CO2和O2混合气的密闭容器中充分燃烧。
(1)若Mg粉的质量为6.0 g,反应后容器内O2有剩余,则在反应后容器内的固体
物质中一定含有______________,该固体物质的质量为________________;
(2)若Mg的质量为a g,混合气体的体积为b L,反应后容器内O2有剩余,则在b L
混合气中,V (O2)的取值范围是_____________________________________;
(3)若Mg粉的质量仍为a g,燃烧后Mg粉和气体均无剩余,则反应后容器内固体物质的质量的最大值是______________________________________________。
(气体体积均已折算成标准状况下的数据)
答题卷
化 学
第Ⅰ卷
一 选择题(48分)
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 |
二 填空题
26.(16分)
(1)指出K可能所属的晶体类型__________。
(2)写出化学式:单质B ,化合物F 。
(3)写出上述反应的离子反应方程式:
⑤__________________________________________________________________________
⑥__________________________________________________________________________
(4) 。
27.(18分)
(1)A ; D
(2)应先通 气体,再通 气体;
原因是
。
(3)指出该装置的至少两处错误
。
(4)产率为 ;
主要原因是
(5)
28.(14分)(1)H中的阳离子是 ___________;D的化学式是
_________________。
(2)
。
(3)
。
(4)
。
(5)
,
实验现象是 。
29.(12分)
(1)定含有______________,该固体物质的质量为________________;
(2)V (O2)的取值范围是_____________________________________;
(3)最大值是______________________________________________。
参考答案
一、选择题(每小题只有一个选项符合题意,每小题6分,共48分)
6A 7A 8C 9A 10C 11B 12D 13B
26.(16分)
(1)原子晶体(2分) (2)Cl2 、 H2SiO3或者H4SiO4(各2分)
(3)⑤SiO2+2OH-===SiO![]() +H2O( 3分)
+H2O( 3分)
⑥SiO![]() +2H2O+2CO2===H2SiO3+2HCO
+2H2O+2CO2===H2SiO3+2HCO![]() ( 3分)
( 3分)
![]()
![]() (4)3Si(NH2)4 Si3N4+8NH3↑或者Si(NH2)4
SiN+NH3↑(4分)
(4)3Si(NH2)4 Si3N4+8NH3↑或者Si(NH2)4
SiN+NH3↑(4分)
27.(共18分)(1)氯化铵和熟石灰;(2分)稀盐酸 (2分)
(2)NH3,(2分)CO2;(2分)
CO2在水中溶解度小,先通NH3至饱和,有利于NaHCO3析出(2分)
(3)BC之间缺少止水夹;B装置应与大气相通;通NH3的导管不应伸入液面以下(任意两处,2分)
(4)49%;(2分)NaHCO3在水中有较大的溶解度,未能全部沉淀出来(2分)
(5)NH4Cl, CO2 (2分)
28.(14分) (1)Fe2+ (2分)Al(OH)3
(2分)
(2)2Al+2OH-+2H2O=2AlO2-+3H2↑
(2分)
![]() (3)Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)
(4)2Al+Fe2O3
2Fe+Al2O3(2分)
(5)4Fe(OH)2+O2+2H2O=4Fe(OH)3,(2分)
白色絮状沉淀迅速变为灰绿色,最后变为红褐色。(2分)
29.(12分)(1)MgO (2分) 10 g (2分)
(2)![]() <V<b (4分)
<V<b (4分)
(3)![]() +a (4分)
+a (4分)