高三级化学上学期第一次月考试题
命题人:袁妙君 审核人:吴惠芝
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分150分,考试时间120分钟。
第一部分 选择题共70分
一.选择题(本题包括10小题,每小题3分,共30分,每小题只有一个选项符合题意)
1.六氟化硫分子呈正八面体,难以水解,在高电压下仍有良好的绝缘性,在电器行业有着广泛用途,但逸散到空气中会引起强温室效应。下列有关SF6的推测正确的是 :
A.SF6易燃烧生成二氧化硫 B.SF6中各原子均达到八电子稳定结构
C.高温条件下,SF6微弱水解生成H2SO4和HF D.SF6是极性分子
2.下列事实不能用勒夏特列原理解释的是:
A.氨水应密闭保存,放置于低温处
B.在硫酸亚铁溶液中,加入铁粉以防止氧化变质
C.生产硝酸的过程中使用过量空气以提高氨气的利用率
D.实验室常用排饱和食盐水的方法收集氯气
3 下列可用氢键来解释的是:
A.浓的氢氟酸溶液中存在HF2-和H2F3- B.SiH4沸点比CH4高
C.水和乙醇分别与金属钠反应,前者比后者剧烈
D.H2O比H2S稳定,前者1000oC以上才分解,后者300 oC分解
4.下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是:
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
5.下列有关阿伏加德罗常数的叙述正确的是:
A.0.1mol碳酸钠溶于水所得溶液中所含阴离子数小于0.1×6.02×1023个
B.标准状况下,0.5×6.02×1023个甲醛分子所占体积约是11.2L
C.1mol冰醋酸中含有6.02×1023个CH3COO—
D.标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2
6.用98%的浓H2SO4(密度为1.84g/cm3)配制1mol/L的稀H2SO4100mL,配制过程中需用仪器的先后顺序排列是 :①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒 (A)①③⑤⑥⑦ (B)②③⑦⑤⑥ (C)②⑤⑦⑥① (D)④③⑦⑤⑥
7.已知![]() (1) H=-890.3 kJ·
(1) H=-890.3 kJ·![]() ,现有
,现有![]() 和CO的混合气体共0.75 mol,完全燃烧后,生成
和CO的混合气体共0.75 mol,完全燃烧后,生成![]() 气体和18 g液态水,并放出515.9
kJ热量,则CO燃烧的热化学方程式是:
气体和18 g液态水,并放出515.9
kJ热量,则CO燃烧的热化学方程式是:
①![]() H=-566 kJ·
H=-566 kJ·![]()
②![]() H=-283 kJ·
H=-283 kJ·![]()
③![]() H=-374.4 kJ·
H=-374.4 kJ·![]()
④![]() H=+1406.2KJ·
H=+1406.2KJ·![]()
A.①② B.①③ C.②④ D.③④
8.某无水盐在30℃时的溶解度为50g,20℃时的溶解度为20g。若将100g质量分数为30%的该盐溶液从30℃降到20℃,析出无水晶体的质量是:
A、16 g; B、12 g; C、10 g ; D、1 g;
9.下列叙述中正确的是:
①金属钠不能与NaOH溶液反应;②液溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯;③溴化银具有感光性,碘化银不具感光性;④某溶液与淀粉碘化钾溶液反应出现蓝色,则证明该溶液是氯水或溴水;⑤氟气能与氯化钠水溶液反应生成HF和O2;⑥氯气跟水反应时,水既不是氧化剂也不是还原剂。
(A)①③⑤ (B)②④⑥ (C)②⑤⑥ (D)①③④
![]()
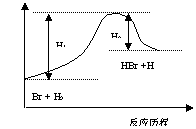 10.参照反应Br + H2 = HBr +H的能量对反应历程的示意图, 下 列 叙述中正确的是
10.参照反应Br + H2 = HBr +H的能量对反应历程的示意图, 下 列 叙述中正确的是
A. 正反应为吸热反应
B. 加入催化剂,该化学反应的反应热变大
C. 正反应为放热反应
D. 加入催化剂可增大正反应速率,降低逆反应速率
二.选择题(本题包括10小题,每小题4分,共40分,每小题有一至两个选项符合题意)
11.在标准状况下,ag气体A与bg气体B的分子数相同,与此有关的以下说法中不正确的是
A.A与B的摩尔质量之比为:a:b
B.相同状况下,同体积的A与B的质量之比为a:b
C.质量相同的A与B的分子数之比为b:a
D.同温同压下,A与B的密度之比为b:a
12. 下列离子方程式书写正确的是:
![]() A.碳酸钠溶液显碱性:CO32-
+ 2H2O H2CO3 +2OH-
A.碳酸钠溶液显碱性:CO32-
+ 2H2O H2CO3 +2OH-
B.氯化铝溶液中加入偏铝酸钠溶液:Al3+ +3AlO2- +6H2O= 4Al(OH)3 ↓
C.氨气通入碳酸氢钠溶液中:NH3 +H+ = NH4+
D.碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2+ +2HCO3- +2OH-= CaCO3↓+2 H2O+CO32-
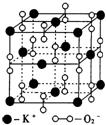 13.高温下,超氧化钾(KO2)晶体结构与NaCl相似,其晶体结构的一个基本重复单元如右图所示,已知晶体中氧的化合价可看作部分为0价,部分为—2价。则下列说法正确的是 :
13.高温下,超氧化钾(KO2)晶体结构与NaCl相似,其晶体结构的一个基本重复单元如右图所示,已知晶体中氧的化合价可看作部分为0价,部分为—2价。则下列说法正确的是 :
A.晶体中与每个K+距离最近的K+有12个
B.晶体中每个K+周围有8个O2—,每个O2—周围有8个K+
C.超氧化钾晶体中阳离子与阴离子的个数比为1:2
D.晶体中,0价氧原子与-2价氧原子的数目比为1:1
14.在加入铝粉能放出H2的溶液中,可能大量共存的是:
A.NH4+、NO3-、CO32-、Na+ B.Na+、Ba2+、Mg2+、HCO3-
C.NO3-、K+、SO42-、Cl- D.NO3-、Na+、Fe2+、K+
15.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羧基硫(COS),已知羧基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法正确的是:
A.羰基硫的电子式为:B.羰基硫属于非极性分子
C.羰基硫沸点比CO2低 D.羰基硫中三个原子处于同一直线上
16.在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量浓度之比为:4:2:1,现加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比为:1:3:9,则投入的铁粉与原溶液中Cu2+的物质的量之比为:
A、5:4 B、4:5 C、3:5 D、5:6
17.已知热化学方程式2SO2(g)+
O2(g)![]() 2
SO3(g) △H= -Q kJ/mol(Q>0),则下列说法正确的是:
2
SO3(g) △H= -Q kJ/mol(Q>0),则下列说法正确的是:
A.2molSO2(g)和1mol O2(g)所具有的内能小于2 molSO3(g)所具有的内能
B.将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QKJ的热量
C.升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小
D.如将一定量SO2(g)和 O2(g)置于某密闭容器中充分反应后放热QKJ,则此过程中有2molSO2(g)被氧化
18.在容积不变的密闭容器中存在如下反应: 2SO2(g)+O2(g)![]() 2SO3(g)
△H<0
2SO3(g)
△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
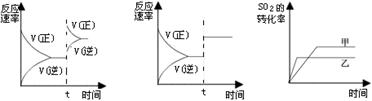
I II III
A.图I研究的是t时刻增大O2的浓度对反应速率的影响
B.图II研究的是t时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且甲的温度较低
19.羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65mL 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4= Fe2(SO4)3+ K2SO4+ MnSO4+ H2O(未配平),则在上述反应中,羟胺的氧化产物是:
A.N2 B.N2O C.NO D.NO2
20.在一定量饱和的澄清石灰水中,加入5.60克CaO后充分搅拌,静置恢复到原来的温度,发现石灰水下部有白色不溶物形成,则下列叙述正确的是:
A.白色不溶物为CaO,其质量为5.60克
B.白色不溶物为Ca(OH)2,其质量为7.40克
C.石灰水的浓度和质量均不会变化
D.石灰水的质量将会减少,石灰水的pH不会发生变化
第二部分 非选择题 共80分
三、(本题包括2小题,共22分)
21.(8分)近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管,常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:
C+ K2Cr2O7
+ H2SO4(稀)![]() CO2↑+ K2SO4 + Cr2 (SO4 ) 3+
.
CO2↑+ K2SO4 + Cr2 (SO4 ) 3+
.
(1)完成并配平上述反应的化学方程式。(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 (填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11g气体物质,则转移电子的数目为 。
22.(14分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。回答下列问题:
⑴上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤①、③中研磨固体所用仪器的名称是___________________;
⑵步骤③中洗涤沉淀的操作是_____________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
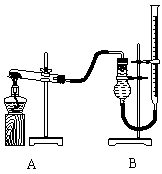 用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2 g | 无其他物质 | |
| ⑤ | 1.2 g | CuO 0.5 g | |
| ⑥ | 1.2 g | MnO2 0.5 g |
回答下列问题:
⑶上述实验中的“待测数据”指_____________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,__________________________________
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a._______________________________;b.CuO的化学性质有没有改变。
四、(本题包括2小题,共21 分)
23. (11分)据著名网站-网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构。
(1)下列有关O4的说法正确的是
A、O4分子内存在极性共价键
B、合成O4的反应可看作核聚变反应,即不属于化学变化
C、O4与O3、O2都是氧的同素异形体
D、O4将来可用作更强有力的火箭推进的氧化剂
 (2)含O
(2)含O![]() 、O
、O![]() 甚至O
甚至O![]() 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
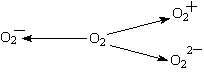
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式: 。
(4)化合物O2[PtF6]中含有O![]() ,则O2[PtF6]属于____________化合物,有一种常见的含有O
,则O2[PtF6]属于____________化合物,有一种常见的含有O![]() 的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
____________________________________________________________
24.(12分)物质A是化合物,B、C、D、K都是单质,反应②~⑤都是常见的工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
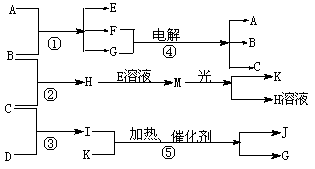
请填写下列空白:
(1)写出下列物质的化学式:B ; C ; D ;
K ;G ;J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。②I溶于G 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为
五.(本题包括2小题,共17分)
25.(9分)汽油不完全燃烧的化学方程式为:2C8H18+23O2![]() 12CO2+4CO+18H2O。人体吸进CO后,CO、O2与人体血红蛋白(Hem)建立如下平衡:CO+HemO2
12CO2+4CO+18H2O。人体吸进CO后,CO、O2与人体血红蛋白(Hem)建立如下平衡:CO+HemO2![]() O2+HemCO,此平衡存在如下关系:
O2+HemCO,此平衡存在如下关系:![]() =210,当HemCO浓度为HemO2浓度的2%时,人的智力将受到严重损伤。
=210,当HemCO浓度为HemO2浓度的2%时,人的智力将受到严重损伤。
某40万人口的中等城市,能有效利用的标准状况下的空气为2.24×106m3(O2约占空气体积的21%),以每辆汽车满负荷行驶,每天约有28.5 g汽油不完全燃烧,此城市如达到中等发达国家水平,平均每10人拥有1辆汽车。
试回答:(1)空气中含氧气_________mol。(2)![]() ≤________时人才能不受严重损伤。
≤________时人才能不受严重损伤。
(3)若该城市上方的未被污染的空气在某一天内没有流动,则该天汽车的最大使用率不得超过________%(要求保留2位有效数字)。
26、(8分)在密闭容器中,通入AmolN2和BmolH2,在一定条件下达到平衡,容器中还剩余CmolN2,
(1)生成NH3的物质的量为 ; (2)平衡时H2的转化率为 ;
(3)若把容器体积减小一半,则正反应速率 ,逆反应速率 ,
N2转化率 。(填“变大”、“变小”、“不变”)
六.(本题包括2小题,共20分)
27.(12分)(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化:
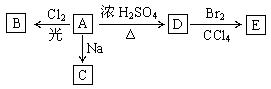 |
① A分子中的官能团名称是 。
② A只有一种一氯取代物B。写出由A转化为B的化学方程式: 。
③ A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。则F的结构简式是 。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(填序号)
① 加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是 。
(3)A和“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。 “TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。“TBHQ”的结构简式是 。
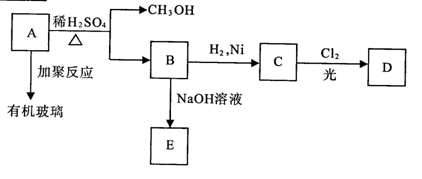 |
28.(8分)有机玻璃是一种重要的塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化:
请回答:
(1)B分子中含有的官能团是_____________, _____________.
(2)由B转化为C的反应属于(选填序号) _____________.
①氧化反应 ②还原反应 ③加成反应 ④取代反应
(3)C的一氯代物D有两种,C的结构简式是_____________.
(4)由A生成B的化学方程式是_____________.
(5)有机玻璃的结构简式是_____________.
高三级第一次月考化学试题答题卡
一、选择题(共30分)
|
二、选择题(共40分)
|
第二部分 非选择题 共80分
三、(本题包括2小题,共22分)
21.(1) C+ K2Cr2O7
+ H2SO4(稀)![]() CO2↑+
K2SO4 +
Cr2 (SO4 )
3+ .
CO2↑+
K2SO4 +
Cr2 (SO4 )
3+ .
(2) , 。
(3) (4) 。
22.(14分)⑴_______________ 、 ___________________;
⑵_____________________________________________
⑶___________; ⑷___________
⑸_________________________________________
⑹a._______________________________;
四、(本题包括2小题,共21 分)
23. (11分)(1)
(2) 、 (3) 。
(4)____________ 、____________________________________________________________
24.(12分)(1) B ; C ; D ;
K ;G ;J 。
(2) ① 。② 。
(3)
五.(本题包括2小题,共17分)
25.(9分)(1)_________mol。(2)________ (3)________%(要求保留2位有效数字)。
26、(8分)(1) ; (2) ;(3) , ,
。
六.(本题包括2小题,共20分)
27.(12分)① 。② 。③ 。
(2) 、 。
(3) 。
28.(8分)(1) _____________, _____________.
(2) _____________. (3) _____________.
(4) _____________. (5) _____________.
高三级第一次月考化学参考答案
一、选择题(共30分)
|
二、选择题(共40分)
|
21、(1)3、2、8![]() 3、2、2、8H2O(3分) (2)K2Cr2O7(1分)、CO2 (1分)
3、2、2、8H2O(3分) (2)K2Cr2O7(1分)、CO2 (1分)
(3)A(1分) (4)6.02×1023 (2分)
22、(14分)⑴ ①②③ 研钵 ⑵沿玻璃棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次 ⑶时间 ⑷碱式 ⑸取一根带火星的木条,伸入干燥管内,看木条是否复燃 ⑹CuO的质量有没有改变(每空2分)
|
(4)离子(1分) 4KO2 + 2CO2 = 2K2CO3+ 3O2 (2分)
24.(12分)(1) B.Cl2 C.H2 D. N2 K. O2 G. H2O J.NO(各1分)
(2) ①H+ +ClO-= HClO、NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH- (各2分)
NH4++OH- (各2分)
(3)2HCl(g)=H2(g)+Cl2(g);△H= +184.6 kJ·mol-1(2分)
25. 分析:(1)n(O2)=(2.24×106m3×103L·m—3×21%)/22.4 L·mol—1=2.1×107mol。
(2)![]() ≤
≤![]() 。
。
(3)该城市每天所有汽车满负荷行驶不完全燃烧的汽油的总物质的量为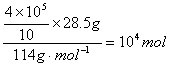
设汽车利用率为ω,根据关系式:
2C8H18~4CO可得
耗O2物质的量为![]() mol,生成CO物质的量为2×104ωmol,则有:
mol,生成CO物质的量为2×104ωmol,则有:
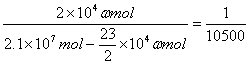 ,
,
解得:ω=10%。
答案:(1)2.1×107 (2)![]() (3)10%
(3)10%
26.(1)2(A-C)mol (2)3(A-C)/B (3)变大 变大 变大
27.(1)①羟基(2分) ② (2分)
③ (2分)
(2)①② (2分) (3) (2分)
![]() 28. (1)碳碳双键、羧基 (或 -COOH )
28. (1)碳碳双键、羧基 (或 -COOH )
(2)②③
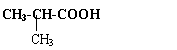 (3)
(3)
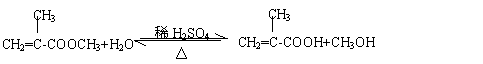 |
(4)
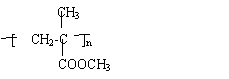 |
(5)