高三年级化学上学期第三次联考试题
化学试题
本试卷分为第Ⅰ卷和第Ⅱ卷两部分,满分100分,考试时间100分钟
相对原子量:H:1 O:16 C:12 N:14 Al:27 S:32 Cl:35.5 K:39 Fe:56 Ba:137
第Ⅰ卷(选择题,共51分)
一.选择题(本题包括17小题,每小题3分,共51分。每小题只有1个选项符合题意)
1. 下列各项中的“黄色”,不属于因化学反应而产生的现象的是( )
A.无色试剂瓶中的浓硝酸呈黄色
B.用玻璃片靠近在玻璃导管口燃着的硫化氢的火焰,玻璃片上附有的固体呈现黄色
C.久置的碘化钾溶液呈黄色
D.食盐在无色的火焰上灼烧时,火焰呈黄色
2.Na3N是离子化合物,它能与水反应生成氨气。以下关于Na3N的说法中正确的是( )
A.Na3N与盐酸反应时生成两种盐
B.在Na3N与水反应中Na3N是还原剂
C.Na3N分子中Na+的半径比N3-的半径大
D.Na+ 与 N3-的电子层都与氩原子的结构相同
3.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2 → H2O IO3- → I2 MnO4- → Mn2+ HNO3 → NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. IO3- C. MnO4- D. HNO3
4. 关于NaHCO3性质的说法正确的是( )
A.只能与酸反应,不能与碱反应
B.医疗可用于冶疗胃酸过多
C.与足量的酸反应时放出的CO2比等质量的Na2CO3要少
D.相同温度时,碳酸氢钠的溶解度大于碳酸钠的溶解度
5.已知:①向KMnO4固体滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取实验②生成的溶液滴在淀粉KI试纸变蓝
下列判断正确的是( )
A.上述实验证明氧化性:MnO4- > Cl2 > Fe3+ > I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
6.将5.4g Al 投入到200.0mL 2.0mol・L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为( )
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
7.设NA代表阿伏加德罗常数,下列说法正确的是( )
A.5.6 g铁与足量盐酸反应转移的电子数为0.3NA
B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA
C.标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA
D.20 g重水(D2O)中含有的电子数为10NA
8.在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
A.两种气体的压强相等 B.O2比O3的质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
9.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
由于浓度不同而发生不同氧化还原反应的是( )
A.①③ B.③④ C.①② D.①③④
10.下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2OFe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:HCO3-+H+===CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu===Fe2++Cu2+
11.下列实验中,溶液颜色有明显变化的是( )
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHSO3溶液中
D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
12.下列物质能通过化合反应直接制得的是( )
①FeS ②H2SO4 ③NH4NO3 ④HCl
A.只有①②③ B.只有②③
C. 只有①③④ D.全部
13.某非金属单质A和氧气发生化合反应生成B(B为气体)。其体积是反应掉氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
14.下列条件下,两瓶气体所含原子数一定相等的是( )
A.同质量、不同密度的N2和CO2 B.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H6 D.同压强、同体积的N2O和CO2
15.有一在空气中暴露过的KOH固体,经分析知其内含水7.62%、K2CO3 2.38%,KOH 90%,若将样品1g加入到1mol・L-1盐酸46mL里,过量的酸再用1.07mol・L-1 KOH溶液中和,蒸发中和后的溶液可得固体质量为( )
A.3.43g B.4.00g C.4.50g D.无法计算
16.将一定量的钠、铝合金置于水中,合金全部溶解,得到20ml、pH=14的溶液,然后用1mol/L的盐酸滴定至沉淀量最大时,消耗盐酸40ml。原合金中钠的质量为( )
A.0.23g B. 0.64g C.0.69g D. 0.92g
17. 天平的两个托盘上放两个等质量的烧杯,分别加入3.65 g的盐酸,再分别加入x g的NaHCO3与y g的KHCO3, 反应后天平仍平衡,则x,y的正确关系是( )
A. x>y≥8.4 g B. y>x≥10 g C. x=y≥8.4 g D. x=y≥10 g
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | |||||||||
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | |
| 答案 |
第Ⅱ卷(非选择题,共49分)
二、填空题(本题包括2小题,共24分)
18.(8分) 碱金属能形成离子型氢化物。如氢化钠的化学式为NaH,氢化钠具有较强的还原性。
(1)氢化钠的电子式为____________,氢化钠中氢元素是______价。
(2)NaH能与水剧烈反应生成对应的碱和氢气,写出反应的化学方程式并标明电子转移的方向和数目_______ ____。该反应中氧化产物与还原产物的质量比为______________。
19.(16分)中学化学中几种常见物质的转化关系如下:
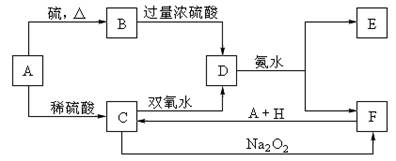
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体E粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)①H2O2分子的电子式:
②写出C的酸性溶液与双氧水反应的离子方程式: 。
(4)写出鉴定E中阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式: 。
三、实验题(本题包括1小题,共12分)
20.(12分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系
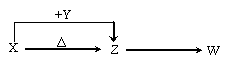 (部分反应物、产物及反应条件已略去)。请回答:
(部分反应物、产物及反应条件已略去)。请回答:
(1)W的电子式是 。(2)X与Y在溶液中反应的离子方程式是 。
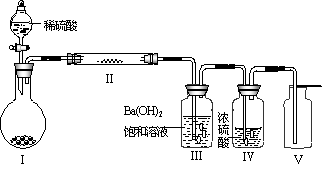 (3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用右图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用右图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。
①装置Ⅰ中反应的化学方程式是 。
装置Ⅱ中物质的化学式是
。
②用Ⅹ含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要的装置,填写编号)。
四、(本题包括2小题,共13分)
21. (4分)将15.6 g Na2O2溶于b g水中,恰好使Na+离子数与水分子数之比为1:50,则b值为多少?(请写出详细计算过程)
22. (9分)现在由等物质的量的NaHCO3和KHCO3组成的混合物a g,与100mL盐酸反应。(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示。)
(1)如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为 mol・L―1。
(2)如果盐酸过量,生成CO2的体积为 L。
(3)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道 。
(4)若NaHCO3和KHCO3不是以等物质的量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积(VCO2)范围是 。(不要求写计算过程)
![]() 高三年级第三次联考
高三年级第三次联考
![]() 化学答题卷
化学答题卷
第Ⅰ卷(共51分)
一、选择题:(每小题3分,共51分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | |||||||||
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | |
| 答案 |
第Ⅱ卷 非选择题(共49分)
二、填空题(本题包括2小题,每空2分,共24分)
18.(1) _________________ __________________
(2)_________________________________________________ _________________
19.(1)红褐色胶体E粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)①H2O2分子的电子式:
②________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:
____________________________________________________________________
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的
离子方程式: 。
三、实验题(本题包括1小题,每空2分,共12分)
20.(1)______________________ (2)__________________________________________
(3) ①___________________________________________ _________________
②___________________ ____________________
四、(本题包括3小题,共13分)
21. (4分)
22. (2分)(1)如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为 mol/L。
(2分)(2)如果盐酸过量,生成CO2的体积为 L。
(2分)(3)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道 。
(3分)(4)若NaHCO3和KHCO3不是以等物质的量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积(VCO2)范围是 。(不要求写计算过程)
高三年级第三次联考化学试题参考答案
一.选择题(本题包括17小题,每小题3分,共51分。每小题只有1个选项符合题意)
1.D 2. A 3.B 4.B 5.A 6.D 7.D 8.D 9.A 10.B 11.B 12.D 13.A
14. C 15.A 16.D 17.D
二、填空题(本题包括2小题,共24分)
18.(共8分)
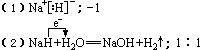
19.(共16分)(1)1nm~100nm(2分)
(2)Fe FeS
H2SO4(稀)(6分)
(3)①H![]() H(2分)
H(2分)
②2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
(4)取少量E于试管中,用胶头滴管入NaOH溶液,加热试管,可观察到试管口处湿润的红色石蕊试纸变蓝。(或其他合理答案)(2分)
(5)4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+(2分)
三、实验题(本题包括1小题,共12分)
20.(共12分)(1)![]() (2分)
(2分)
(2)![]() (2分)
(2分)
(3)①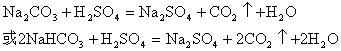 (2分) Na2O2(2分)
(2分) Na2O2(2分)
② H2O2 (2分) I、IV、V(2分)
四、(本题包括3小题,共13分)
21. (4分) 363.6 g
22.(9分) (1)5a/46
(2)22.4a/92
(3)盐酸的物质的量浓度
(4)![]() < VCO2<
< VCO2<![]()