�����꼶��ѧʮһ���¿�����
���ԭ��������C=12 Na=23 O=16 H=1 S=32 N=14
��������ѡ���� ��44�֣�
ѡ���⣨ÿС��ֻ��һ��ѡ��������⣬ÿС��2�֣���44��
1.����ÿ�����ʷ���״̬�仯���˷������Ӽ�����������ͬ�����͵��ǣ��� ��
A��ʳ�κ������ۻ�����������������B���ƺ����ۻ�
C����ɱ��������������������� D������������������ۻ�
2����ij��ԭ��������a g��12C��ԭ��������b g��NA�ǰ����ӵ�������ֵ������˵
������ȷ����
A����Ԫ�ص����ԭ������һ����12a/b��������B������ԭ�ӵ�Ħ��������aNAg/mol
C��Wg����ԭ�ӵ����ʵ���һ����![]() mol����D��Wg����ԭ��������������10W/a
mol����D��Wg����ԭ��������������10W/a
3����ʾ���б仯�Ļ�ѧ������ȷ���� ������
A�����ˮ�еμ�FeCl3��Һ�Ʊ�Fe(OH)3���壺Fe3+��3H2O![]() Fe(OH)3����3H+��������������
Fe(OH)3����3H+��������������
B���������ͭ��Һ��������ӦΪ��Cu2++2e�� =Cu
C������������ʴ��������Ӧ��4OH����4e��=O2+2H2O
D��1L0.5mol��L��1ϡ������1L 1mol��L��1����������Һ��Ӧ�ų�57.3kJ���ȣ�
��������H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(1) ����H=��114.6 kJ/mol
4���������ӷ���ʽ��ȷ���ǣ�������
A����CaCl2 ��Һ��ͨ������CO2 ���壺Ca2+��+ CO2 +��H2O =��CaCO3�� +2H+
B����FeCl3��Һ��ʴӡˢ��·�壺2Fe3+��Cu��= 2Fe2+��Cu2+
C��Al Cl3��Һ��Ͷ�����Na��2Al 3+ +6Na +6H2O = 2 Al��OH��3+6Na+ + 3H2��
D��Ca(HCO3)2��Һ�м���������Ba(OH)2��Һ ��
Ca2����2HCO3����2OH����CaCO3����CO32����2H2O
5��Ԫ��A��B��ԭ��������С��18����֪AԪ��ԭ�ӵ�����������Ϊa������������Ϊb��BԪ��ԭ�ӵ�M�������Ϊ(a��b)��L�������Ϊ(a��b)����A��B��Ԫ�����γɵĻ�����ľ�������Ϊ������������
A�����Ӿ��塡��B��ԭ�Ӿ��塡�� C�����Ӿ��塡 D����������
6��ijʵ����ֻ���ռŨ���ᡢͭƬ������ʯ����ˮ����Ƿȱ�Լ��ĽǶȿ������ܽ��е�ʵ����
����A���ⶨ�����Ũ�ȡ���B����ȡH2 ��C����ȡNa2CO3�� ��D����NaCl
7�����и����壬�ȿ���ͬ��װ����ȡ���ֿ�����ˮ���ռ���������ŨH2SO4�������
��A��NO2��NH3������B��CH4��O2 ����C��Cl2��C2H4���� ����D��SO2��H2S
8����ƿ�ֱ���Fe3+��Al3+��Mg2+��Fe2+��NH4+��Na+ �������ӵ���Һ���������������Լ����𡡡���
��A����ˮ������B��NaOH������C��HCl������D��(NH4)2S
9��������ע�к��ߵķ�Ӧ���ڷ�Ӧ�в�����ȫ���ĵ���
��A����������CO2��COͨ������Na2O2���Թܲ������õ����ȼ
��B����ʢ�е����ʵ������ɱ���CaO�Ļ������ܱ������мӼ���ˮ
��C����1molCu����2molŨH2SO4�м���
��D����ǿ����������£��������Ca(ClO)2����Һ��ͨ������CO2
10����һ��������KI��Zn��FeBr2�ֱ���������Cl2��Ӧ�����3����Ӧ��ʧ������Ŀ��ȣ���KI��Zn��FeBr2�����ʵ���֮��Ϊ����
A�� 1��2��3 ����B��3��2��1�� ��C��6��3��2������D��2��3��6
11��ij����������Ļ�ѧʽΪMxOy(y��1)����ý����Ȼ���Ļ�ѧʽ��
��A��MxCly��������B��MxCl2y������ ��C��MCly/x������ ��D��MCl2y/x
12.��ij��Һ�м���������ᣬ���ɰ�ɫ���������˺�����Һ�м��������ˮ�����а�ɫ�������ɣ��ٹ��ˣ�����Һ�м���Na2CO3��Һ�������ɰ�ɫ��������ԭ��Һ�к��е�������
��A��Na+��Cu2+��Ba2+������ ��B��Ag+��Cu2+��Ba2+
��C��Ag+��Fe3+��Ca2+����������D��Ag+��Ba2+��Al3+
13��ȡ������ɫʯ����ֽ���ڲ������ϣ�Ȼ��˳��ֱ�μ�65����HNO3��Һ��
98.3����H2SO4��������ˮ��������ֽ�����ֵ���ɫ�ֱ���
��A���ס��졢�ס�������B���졢�ڡ��� ����C���졢�졢�졡����D���ס��ڡ���
14���ڱ�״���£���NO��NO2��O2��ɵĻ�����������һ����ƿ�У�����ƿ������ˮ������ˮȫ�������������������Ҳ��������ɢ����ƿ���ˮ�����ƿ����Һ�����ʵ���Ũ��(C)��Χ��ȷ��������
��A��0��C��1/22.4��������������B��1/39.2��C��1/28
��C��1/28��C��1/22.4������������D��1/39.2��C��1/22.4
15�����������ԡ���ԭ�Ե�ǿ�������������ʵĽṹ�йأ��������ʵ�Ũ�Ⱥͷ�Ӧ�¶��йء����и������ʣ���Cu��HNO3��Һ�� ��Cu��FeCl3��Һ�� ��Zn��H2SO4��Һ��������Fe��HCl��Һ���� ��������Ũ�Ȳ�ͬ��������ͬ������ԭ��Ӧ���ǡ���������������
A���٢ۡ�����B���ۢܡ�����C���٢ڡ�����D���٢ۢ�
16������˵������ȷ����:
A��NO2��BF3��NCl3������û��һ������������ԭ�ӵ��������Ӷ�������8e- �ȶ��ṹ��
B��P4��CH4����������������Ҽ��Ƕ�Ϊ109o28�@��
C��NaCl��������Na+��������Na+����12����
D����ԭ�Ӽ�ͨ�����ۼ����γɵľ���һ�����иߵ��ۡ��е㼰Ӳ�ȡ�
17���������������ļӿ죬�����С��װʳƷ�ѱ��㷺���ܣ�Ϊ�˷�
ֹ��֬ʳƷ���������ʣ��ӳ�ʳƷ�ı����ڣ��ڰ�װ���г����뿹�������ʣ����в����ڿ��������ʵ��ǡ���
A����ʯ�ҡ���B����ԭ���ۡ� C���������ơ���D��ά����C
18���������� ���������� �۹������� ���������ƣ� 1mol�����������ʳ��ڷ����ڿ����У�����˵����ȷ����
A���������ʶ��з�����������ԭ��Ӧ
B�����������ڷ�Ӧ��ת����2mol����
C���������ӵ�����Ǣ�>��>��>��
D���������ӵ�����Ǣ�>��>��>��
19�����������ʵ���Һ�зֱ����һ������![]() ���壬������ֻ����������
���壬������ֻ����������
A�� ������ҺNa2CO3��Һ��
B. ![]() ϡ��Һ
ϡ��Һ
C. ![]() ϡ��Һ����������
D. ����
ϡ��Һ����������
D. ����![]() ��Һ
��Һ
20�����и����е��������������еĵ���������ȵ��ǡ����������������� ��������
A��Na+��Mg2+���� ��������������B��F����OH��������
![]() C��NH4+�� OH ���� ������ D��CH4��H2O
C��NH4+�� OH ���� ������ D��CH4��H2O
21�������������ʵı仯��������Ӽ��������йص��ǡ������������������� ��������
����F2��Cl2��Br2��I2���ۡ��е�������
�£����ʯ��Ӳ�ȴ��ڹ裬���ۡ��е�Ҳ���ڹ�
�ã�NaF��NaCl��NaBr��NaI���۵����ν���
�ģ�HF��HCl��HBr��HI�����ȶ������μ���
22�����˽��齫��Ԫ������Ԫ�����ڱ��Ģ�A�塣������ʵ��֧����һ�۵���ǣ���Hԭ�ӵõ�һ������ʵ��������Ӳ��ȶ��ṹ��������ӵĽṹʽΪH��H����������Ԫ���γ����ӻ�����M+[��H]�����ܷ�����ԭ�Ӽ�Ļ�ѧ�������ڷǼ��Լ��������� ��������
A��ֻ�Т٢ڢۡ�����B��ֻ�Т٢ۢܡ�����C��ֻ�Тڢۢܡ����� D���Т٢ڢۢ�
����������ѡ���⣬��56�֣�
23. ����ʵ������ܴﵽʵ��Ŀ�ĵ���__________________������ţ���
A�����ˮ�е�������ŨFeCl3��Һ��������ʺ��ɫ����ȡFe(OH)3����
B����ʢ��ϡHNO3���Թ��м���ͭƬ�����Լ��ȣ��۲����ɵ�NO����
C����pH��ֽʪ������ڼ���NH3��HCl���ִ̼�������
D���õι���ȡNaOH��Һ������õ�FeSO4��Һ�У���ȡFe(OH)2
E��������NO2������ܱղ����������ˮ�У���֤�¶ȶԻ�ѧƽ���Ӱ��
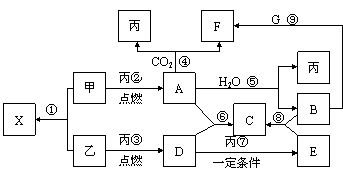 24.
�ס��ҡ���Ϊ�������ʣ��ҡ�����Ԫ�������ڱ���λ��ͬһ���塣X��A��B��C��D��E��F��G��Ϊ�����Ļ��������A��X��Ħ��������ͬ��A��G����ɫ��ӦΪ��ɫ����һ�������£��������ת����ϵ����ͼ����ش�
24.
�ס��ҡ���Ϊ�������ʣ��ҡ�����Ԫ�������ڱ���λ��ͬһ���塣X��A��B��C��D��E��F��G��Ϊ�����Ļ��������A��X��Ħ��������ͬ��A��G����ɫ��ӦΪ��ɫ����һ�������£��������ת����ϵ����ͼ����ش�
(1) д��ѧʽ����_________��E________��
(2)X�ĵ���ʽΪ____________________������
(3) д��A��H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ��___________________________________ ��
(4) д��B��G��Һ��Ӧ����F�����ӷ���ʽ�������������������������������� ��
(5) ����ͼ�ķ�Ӧ�У�������������ԭ��Ӧ���ǣ�����ţ�____________________��
25. ��ͼ��A��B��C�ֱ���ij����С����Ƶ���ȡ������������Ȫʵ�������װ��ʾ��ͼ����ȡNH3ѡ���Լ���ͼ��ʾ���ش��������⣺
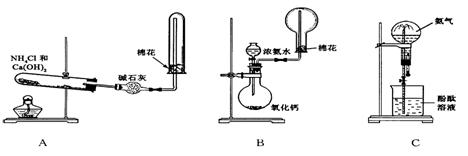 |
(1)��Aͼ��ʾ��װ�ÿ��Ʊ������NH3��
���ٷ�Ӧ�Ļ�ѧ����ʽΪ��__________��װ�����ռ�NH3���Թܿڷ������ŵ������ǣ�_________��
�ڸ�����и�����ܷ������ˮCaCl2___________��������_________________________.
(2)��Bͼ��ʾ��װ�ÿɿ�����ȡ�ϴ���NH3������Ȫʵ�顣����Bͼ��ʾ��װ�ü��Լ��ش��������⣺
�����û�ѧ����ʽ��ʾ��Ũ��ˮ����CaO���д���NH3�ݳ��Ĺ��̣�____________________.
���ڼ���NH3�Ƿ��ռ�����ʵ�鷽���ǣ�________________________________��
(3)��Cͼ��ʾ��װ�ý�����Ȫʵ�飬�ϲ���ƿ�ѳ������ﰱ��������ˮ����IJ�����__________����ʵ���ԭ���ǣ�_____________________��
�������Cװ����ƿ��NH3����������ͬ״������ͬ���H2������10��������Ȫʵ����Ϻ���ƿ��ˮ����������ƿ�ݻ���___________(�����֮����)��
26 . ͬ��Ԫ�ص�ͬ�����ʵĽṹ�����ʼ��������ԣ�Ҳ�������ԡ��ش��������⣺
�� ��֪����FCH2COOH>CH3COOH�����ƶϣ�
��BrCH2COOH����ClCH2COOH����FCH2COOH��������ǿ������˳������ţ�_________________��
�� ��֪AgCl������ϡ��ˮ�γ�������Һ��AgBr������Ũ��ˮ�γ�������Һ��AgI������Ũ��ˮ�����Ƕ�������ˮ�����ƶϣ�
��������������ˮ���ܽ���ɴ�С��˳��__________�������� ______________��
[3]��֪���Ŀռ乹�;�Ϊ�����壬NH4+�ĽṹʽΪ \s\up10(�O��N��,\s\up10(�OH������ʾ
���õ��Ӷ���Nԭ�ӵ������ṩ���� �뻭���Ľṹʽ_____________________��
27. X��Y��Z���ֶ�����Ԫ�أ����ǵ�ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij��������ڳ����¶�����ɫ���壬���ʵ������¿ɷ������±仯��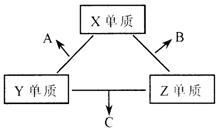
һ��B�����к��е�Zԭ�Ӹ�����C��������1����B��C���ַ����еĵ�����������10������ش��������⣺
�� ��1��XԪ�������ڱ��е�λ����_________����_________�塣
�� ��2������ͬ����Ԫ�����ʵĵݱ���ɣ�����B��C���ʵķе㷴����������Ϊ���ǵķ���֮�����_________��
�� ��3����C�ĵ���ʽ��________________��C���ӵĽṹ��________�Ρ�
��C��һ�������·�Ӧ����A�Ļ�ѧ����ʽ��__________________________��
��X��Y��Z����Ԫ�ؿ����һ��ǿ��W��C���ʵ������±�W��������һ���Ρ����ε�ˮ��ҺpH________7������ڡ�������С���������ڡ� ������ԭ���ǣ�д�����ӷ���ʽ��__________________________��
�� ��4����֪Y������Z��������C�ķ�Ӧ�ǿ��淴Ӧ����H < 0���������ʵ�����Y��Z���ֵ��ʳ���һ�ܱ������У����ʵ������ͺ��¡���ѹ�����·�Ӧ������˵����ȷ����_________��
����a���ﵽ��ѧƽ��ʱ������Ӧ�������淴Ӧ�������
����b����Ӧ�����У�Y���ʵ��������ʼ��Ϊ50%
c���ﵽ��ѧƽ��ʱ��Y��Z���ֵ����ڻ�������е����ʵ���֮��Ϊ1
28���л���A(C10H20O2)����������ζ��������������ϴ���㲨�ķ��㸳�������֪��
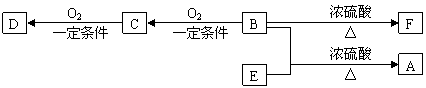 |
��B������û��֧����
��D����̼��������Һ��Ӧ�ų�������̼��
��D��E��Ϊ������ͬ�����ŵ�ͬ���칹�塣E���������ϵ���������ԭ��ȡ������һ�ȴ���ֻ��һ�֡�
��F����ʹ������Ȼ�̼��Һ��ɫ��
��1��B���Է����ķ�Ӧ�������������� (ѡ�����)��
������ȡ����Ӧ��������ȥ��Ӧ�����ۼӾ۷�Ӧ�� ��������Ӧ
��2��D��F���������Ĺ����ŵ������������������� ���������� ��
��3��д����D��E������ͬ�����ŵ�ͬ���칹��Ŀ��ܽṹ��ʽ���������������������� ������������������������������ ��
��4��E����������������ù�صȡ���֪E���Ʊ�������ͬ���䳣����ͬϵ��ݱ���������2������1�������ͼ�����һ����������ȡE���÷�Ӧ�Ļ�ѧ����ʽ��
��������������������������������������������������������������������������
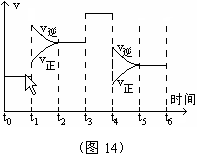
29��һ�ܱ������з������з�ӦN2+3H2![]() 2NH3����H<0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵͼ���ش��������⣺
2NH3����H<0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵͼ���ش��������⣺
��1������ƽ��״̬��ʱ�����_���������� _����A t0~t1 ������ B,t2~t3����C,t3~t4������D,t5~t6
��2��t1��t3��t4ʱ�̣���ϵ�зֱ���ʲô����������ʲô�仯��
t1ʱ������������������ ��t3ʱ������������������ ��t4ʱ������������������
��3������ʱ����У����İٷֺ�����ߵ��ǣ�������
A��t0~t1 ����������B��t2~t3���������� C��t3~t4���������� D��t5~t6
 |
30���������е�����ѧ��ѧʵ�����м��ֳ����IJ���������
���¶ȼơ�������ƿ���۵ζ��ܡ����ձ�����Բ����ƿ������Ͳ���߲�����
��1���������Ͼ������ʹ���¶ȵ��ǣ��������¶ȼƣ��������� ����д��ţ���������
Ӧ�������ɼ��ȵ����������� ����д��ţ�
��2����Ҫ�õ��¶ȼƵ�ʵ������������ ����д��ţ�
�����Ҵ���ȡ��ϩ�� ��ʯ�ͷ��� ��Ũ����ϡ�͡� �ܲⶨ����ص��ܽ��
��3���������ǻ�ѧʵ���г��õ������������������ڽ��衢���˻�ת��Һ��ʱ�����������й�ʵ������У��϶�����Ҫʹ�ò��������в������ǣ�����ĸ���ţ�_________________��
A�� һ����������������Һ������
B�� �����������ǡ�Ũ�����ˮ��С�ձ��н���Ũ�������ˮ��ʵ��
C�� ����ͨ©����ɵĹ���װ�ý��й���ʵ��
D�� ��Ũ��ˮ��Ũ������а����Ȼ��ⷴӦ��ʵ��
E��������֪Ũ�ȵ������δ֪Ũ�ȵ�����������Һ�����к͵ζ�ʵ��
F��������ͭ������ᾧˮ�����ⶨ��ʵ��
�ǣ��������Ȼ���������Һ�����ˮ���������������塡
�ο��𰸡�����������������������������������
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| �� | C | A | D | B | B | A | B | B | C | C | D |
| ��� | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| �� | D | D | B | A | C | A | C | C | C | A | A |
23 ��3�֣���ACE������24����9�֣���1����O2������SO3
![]() ��2��
��2��
��3���� 2Na2O2 + 2H2O �� 4NaOH + O2��
��4���� HCO3�� + OH�� �� CO32�� + H2O��������5������ �� ��
25����11�֣���1����2NH4Cl+Ca(OH)2 �� CaCl2+2NH3��+2H2O ��
�ƻ��������� , ʹNH3�����Թ� ,ͬʱ��ֹ��Ⱦ������
�ڲ��� ��CaCl2��+��8NH3��==��CaCl2��8NH3
��2���١� CaO��+
NH3��H2O �� NH3�� + Ca(OH)2
�� �ò�����պȡ����Ũ������ռ�NH3���Թܿڣ����������̣�˵���Թ����ռ���NH3����֮����û���ռ���������ʪ��ĺ�ɫʯ����ֽ�����ռ�NH3���Թܿڣ���ʪ��ĺ�ɫʯ����ֽ��������˵��NH3���ռ�������֮����û���ռ���
��3����ֹˮ�м�����ͷ�ι��е�ˮ��NH3�����ܽ���ˮ����ʹ��ƿ��ѹǿѸ�ټ�С ��3/4
26����6�֣���1�� �� �� �١����� ��2�� AgCl��AgBr��AgI����������������������
27����11�֣���1���ڶ�����VIA�� ��2�����
��3������������ �ڡ�
4 NH3��+��5 O2�� �� ��4 NO
+��6 H2O��������������������������
�ۡ�
<����NH4+�� +��H2O�� �� �� NH3 H2O��+
OH-����
��4��ab
28����7�֣���1�� �٢� �ܡ�����2���Ȼ� ��̼̼˫��
29����5�֣���1��ABCD���� ��2�����£��Ӵ�������ѹ������3�� A��������
30����4�֣���1���ڢۢޡ����ܢݣ�2�����٢� �ܡ���������3��E