高三年级化学学科第一学期月考试卷
第Ⅰ卷(选择题 共64分)
可能用到的相对原子质量: H 1 O 16 C 12 Na 23 P 31 S 32 Cl 35.5 K 39 Cu 64 I 127
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。)
1.下列化学用语或文字表述中无误的是
A.NaCl饱合溶液 B.氨水中主要成分是NH4OH
C.氧的同位数有O-16、O-18 D.过氧化钠是强氧化剂
2.下列化合物不能通过化合反应获得的是
A.Na2O B.FeCl2 C.SO3 D.CuS
3.下列对实验现象的描述正确的是
A.Na在空气中燃烧产生苍白色的火焰
B.Cu在氯气中燃烧产生绿色的烟
C.氢氧化钡晶体与氯化铵晶体混合,能够吸收环境的热量
D.在滴有紫色石蕊试液的溶液中通入二氧化硫,溶液的颜色变化是先变红后褪为无色
4.三氯化氮分子中每个原子最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向于氮原子。则下列关于三氯化氮的叙述错误的是
A. 在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl
B. NCl3跟水反应的产物为NH3和HClO
C. NCl3分子结构可能是三角锥形
D. NCl3分子中含有三对共用电子对
5.俄罗斯杜布纳核联合研究所和美国劳伦斯利弗莫尔国家实验室的科学家在2004年2月的美国《物理评论C》杂志上发表文章宣布, 他们新合成了元素周期表上的第115号和第113号元素。科学家在利用回旋加速器进行的实验中,用具有20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为![]() 。下列有关叙述正确的是
。下列有关叙述正确的是
A.115号元素衰变成113号元素是化学变化
B.核素![]() 中中子数与质子数之差为174
中中子数与质子数之差为174
C.113号元素最高正价应为+3
D.115号与113号元素的原子质量比为115∶113
6.下列溶液中: ①石灰水 ②H2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是
 A.只有① B.①③ C.①②⑤ D.②③④⑤
A.只有① B.①③ C.①②⑤ D.②③④⑤
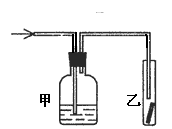
7.将潮湿的Cl2通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是
①浓硫酸 ②NaOH溶液 ③KI溶液 ④饱和食盐水
A.①② B.②③
C.①②③ D.①②③④
8.据报道,美国科学家卡尔・克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且 “N5”分子碎片带一个单位电荷正电荷,则一个“N5+”碎片内,含有共用电子对的对数是
A.4 B.6 C.8 D.10
二、选择题(本题包括8小题。每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项。多选时。该题为0分;若正确答案包括两个选项。只选一个且正确的给2分,选两个且都正确的给4分。但只要选错一个,该小题就为0分。)
9.在pH=1的溶液中,一定可以大量共存的离子组是
A.Cl-、Al3+、Na+、NH4+ B.SO42-、NO3-、Fe2+、Mg2+
C.Na+、Fe3+、SO42-、Cl- D.K+、Ca2+、Cl-、SO42-
10.假定把12C的相对原子质量定为24,把24g12C含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。则下列推断不正确的是
A.此时16O的相对原子质量为32
B.标准状况下,44gCO2的体积为11.2L
C.40gNaOH溶于水配成1L溶液,其物质的量浓度为1mol・L-1
D.44gCO2和28gCO含有相同数目的分子
11.下列反应转化关系肯定不正确的是
A.2KClO3+I2=2KIO3+Cl2
B.Na2S2+2HCl=2NaCl+S↓+H2S
C.NH2Cl+2H2O=HClO+NH3・H2O
D.CaCO3+2HClO=Ca(ClO)2+H2O+CO2↑
12.A、B、C、D均为短周期的4种元素,当A、B两种元素的两个原子分别得到两个电子形成稳定结构时A放出的能量大于B放出的能量,当C、D两元素的原子分别失去1个电子形成稳定结构时D吸收的能量大于C吸收的能量。若A、B、C、D4种元素间分别形成化合物时属于离子化合物可能性最大的是
A.C2A B.C2B C.D2A D.D2B
13.下列离子方程式书写正确的是
A.澄清石灰水中加入盐酸:Ca(OH)2+2 H+=2H2O+Ca2+
B.硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性:
Ba2++OH-+SO42―+H+=BaSO4↓+H2O
C.碳酸钠和碳酸氢钠的混合溶液中滴加少量稀硫酸:HCO3-+H+=CO2↑+H2O
D.向FeBr2溶液中通入过量Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
14.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,20 g D2O和足量的金属钠反应产生气体的分子数为0.5 NA
B.1 mol Na2O2与足量的水反应,转移的电子数为2NA
C.含1 molH2O的冰中,氢键的数目为4 NA
D.常温常压下,124 g P4含有P―P键的个数为6NA
15.四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是
A.a-b=n-m B.原子序数a>b>c>d
C.元素非金属性Z>R D.最高价氧化物对应水化物碱性X>Y
16.t℃时,将100g某物质A的溶液蒸发掉10gH2O,恢复至t℃,析出2.5g晶体,再蒸发掉10gH2O,恢复至t℃,析出7.5g晶体。下列说法中不正确的是
A.t℃时原100g溶液是饱和溶液
B.若析出的晶体中不含结晶水,则可算出t℃时A的溶解度
C.若析出的晶体中含有结晶水,且已知晶体的化学式和相关元素的相对原子质量,那么就可以计算出t℃时A的溶解度
D.根据题给条件可以计算出原溶液的质量分数Y
第Ⅱ卷(非选择题 共86分)
三、(本题有两小题,共26分)
 17.(13分)右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。某次学生实验需要0.5mol/LH2SO4溶液480ml,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
17.(13分)右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。某次学生实验需要0.5mol/LH2SO4溶液480ml,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
①实验中除了量筒、烧杯外还需要的其它仪器有: ;
②计算所需浓硫酸的体积是 mL;若该硫酸与等体积的水混合时,所得溶液中溶质的质量分数 49%(填写“<”、“=”或“>”);
③配制过程中需先在烧杯中将浓硫酸进行稀释。稀释时操作方法是: ;
④下列操作会引起所配浓度偏大的是(填写字母) 。
A、用量筒量取浓硫酸时,仰视量筒的刻度
B、容量瓶未干燥即用来配制溶液
C、浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容;
D、往容量瓶转移时,有少量液体溅出
E、烧杯未进行洗涤
F、定容时俯视刻度线
 G、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
G、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
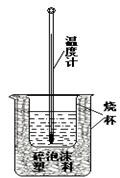
18.(13分)⑴实验室利用如右图装置进行中和热的测定。回答下列问题:
①该图中有两处未画出,他们是 、 ;
②烧杯间填满碎泡沫塑料的作用是 ;
若不用任何材料填充,则所求得的中和热(△H)将
(偏大、偏小或无影响)
③已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ/mol。若向三份等体积、等物质的量浓度的NaOH溶液中分别加入:稀醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Ql、Q2、Q3。则三者大小关系是 。
⑵化学键的键能是指气态原子间形成1mol化学键时释放的能量。如:
H(g)+I(g)→H-I(g)+297KJ 即H-I键的键能为297KJ・mol-1,也可以理解为破坏1mol H-I键需要吸收297KJ的热量。化学反应的发生可以看成旧化学键的破坏和新化学键的形成。
从手册上查得:Si―Si、Si―O和O=O的键能分别为176 kJ/mo1、460kJ/mo1和497kJ/mo1,
据此,完成下列两题
①Si―Si键能小于Si―O键能的理由是: ;
②请写出晶体硅与氧气反应生成二氧化硅的热化学方程式: 。
四、(本题有两小题,共15分)
19.(6分)实验室制取氯气的方法有多种,下列所列物质是制取氯气的某一反应的部分反应物和生成物:HCl、K2Cr2O7、CrCl3、H2O请根据可能的反应原理,完成正确的化学方程式,并用单键头表示电子转移的情况,同时指出反应中的氧化剂和氧化产物。
氧化剂: 氧化产物:
20.(9分)下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素:
| a | b | ||||||
| d | e | f | |||||
| c | g | h |
⑴上述_________元素(填字母)可以形成硬度最大的单质。
⑵ “神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的 CO2,你认为该物质应该是由上表中的________和_______元素(填字母)组成的。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子的电子式是__________,该气体与元素a的单质化合形成的分子的空间构型是 。
⑶ 在一定条件下,a与 h可形成一种化合物,当固态时,其晶体类型为_________________;该物质溶于水后的溶液呈 ________ 性(填“酸”、“碱”或“中”)。
⑷ 现有另一种元素X,其原子获得一个电子时所放出的能量比上表中所列元素中都要
大,则 X 是 __________ 元素(填名称),其在周期表中位于_________ 族。
五、(本题有三小题,共28分)
21.(8分)A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3和AgNO3中的一种。已知:
①A与B反应有气体生成 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是 。
(2)A是 ,B是 ,C是 ,D是 ,E是 。
(3)A与E反应的离子方程式是 。
22.(8分)现有下列反应关系:
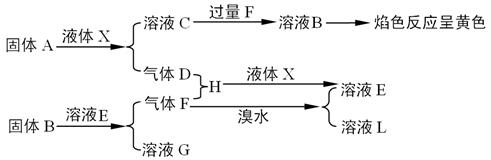
回答下列问题:
⑴固体A的电子式是
;
⑵溶液C与过量F反应生成溶液B的化学方程式:
;
⑶气体F通入溴水的离子方程式:
;
23.(12分)A~J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作杀菌消毒剂。
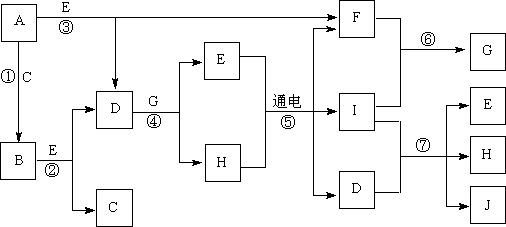
(1)写出反应⑤的化学方程式:_________________________________。
(2)写出反应⑦的离子方程式:_________________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:____________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:__________________。________极(填“阴”或“阳”)附近溶液由无色变为红色。
六、(本题有两小题共17分)
24.(8分)在室温下,向100mL Cu(IO3)2饱和溶液中加入足量的经酸化的KI溶液,发生如下的反应: 5I-+IO3-+6H+=3I2+3H2O 2Cu2++4I-=2CuI↓+I2反应完全后,用
0.10mol・L-1Na2S2O3溶液滴定,I2+2S2O32-=2I-+S4O62-,消耗了40 mLNa2S2O3溶液,计算:
(1)原饱和溶液中Cu(IO3)2的物质的量浓度。
(2)若Cu(IO3)2饱和溶液的密度为1.0g・cm-3,室温时Cu(IO3)2的溶解度是多少?
25.(9分)某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果记录如下表(假设每次实验所产生的氢气全部收集,体积在同温同压下测定)。
| 实验编号 | R的质量/g | 稀硫酸的体积/mL | 生成氢气的体积/L |
| 1 | 1.5 | 50.0 | 1.47 |
| 2 | 2.0 | 50.0 | 1.96 |
| 3 | 2.2 | 50.0 | 2.16 |
| 4 | 2.5 | 50.0 | 2.16 |
| 5 | 3.0 | 50.0 | 2.16 |
根据上述实验结果进行分析、计算,并回答下列问题:
⑴上述实验中,金属一定过量的组的编号是 ,稀硫酸一定过量的组的编号是 。
⑵若在当时的实验条件下,H2的密度为0.085g/L,求反应所用金属R的相对原子质量。
⑶若所使用的稀硫酸的密度为1.12g/mL,求反应所用的硫酸溶液中溶质的质量分数。
高三年级化学学科月考答题纸
得分
一、二选择题:(64分)
| 题号 | 01 | 02 | 03 | 04 | 05 | 06 | 07 | 08 |
| 答案 | ||||||||
| 题号 | 09 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 |
三、(本题有两小题,共26分)
17.(13分)
①
② 、
③
④
18.(13分)
⑴① 、
② 、
③
⑵①
②
四、(本题有两小题,共15分)
19.(6分)
、
20.(9分)
⑴_________
⑵________和_______ __________, 。
⑶_________________; ________。
⑷__________ _________ 。
五、(本题有三小题,共28分)
21.(8分)
(1)
(2)A: B: C: D: E:
(3)
22.(8分)
(1) (2)
(3)
23.(12分)
(1)
(2)
(3)
⑷ 、
六、(本题有两小题共17分)
24.(8分)
(1)
(2)
25.(9分)
(1) 、
(2)
(3)
高三年级化学学科月考参考答案
一、二选择题:(共64分)
| 题号 | 01 | 02 | 03 | 04 | 05 | 06 | 07 | 08 |
| 答案 | D | D | C | A | C | A | C | C |
| 题号 | 09 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | AC | BC | D | A | D | AD | BC | AD |
三、(本题有两小题,共26分)
17.(13分)
①500mL容量瓶、玻璃棒、胶头滴管
②13.6mL; >
③在250mL烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌
④ACF
18.(13分)
⑴①环形玻璃搅拌棒、硬纸板或泡沫塑料板;
②隔热、保温,减少实验过程中热量的损失;偏大
③Q2>Q3 >Ql
⑵①Si原子半径大于O原子,所以Si―Si的键长大于Si―O的键长,因而前者键能小于后者
②Si(S)+O2(g)=SiO2(S) △H=-991 kJ/mo1
四、(本题有两小题,共15分)
19.(6分)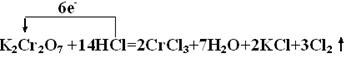
K2Cr2O7 Cl2
20.(9分)⑴ d。 ⑵ c、f,![]() 三角锥形
三角锥形
⑶ 分子晶体,酸。 ⑷ 氟, ⅦA 。
五、(本题有三小题,共28分)
21.(8分)
(1)AgCl
(2)A:Na2CO3 B:HCl C:AgNO3 D:BaCl2 E:NaHSO4
(3)2H++CO32-===CO2+H2O↑
22.(8分)
⑴![]() ⑵ NaOH+SO2==NaHSO3
⑵ NaOH+SO2==NaHSO3
⑶SO2+Br2+2H2O==4H++SO42-+ 2Br-
|
(1)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)Cl2+2OH-![]() Cl-+C1O-+H2O
Cl-+C1O-+H2O
(3)4AlCl3+6Na2O2+6H2O![]() 4Al(OH)3↓+12NaCl+3O2↑
4Al(OH)3↓+12NaCl+3O2↑
(4)2C1--2e-![]() Cl2↑ 阴
Cl2↑ 阴
六、(本题有两小题共17分)
24.(8分)
(1) 3.1×10-3mol・L-1(5分)
(2) 0.31g(3分)
25.(9分)
(1)4、5 1、2 (3分)
(2)24 (3分)
(3)16% (3分)