高三年级化学第一学期第一次月考试题
(请把答案写在答题纸上,只上交答题纸)(考试时间120分钟 满分150分)
相对原子质量 : H 1 He 4 C 12 N 14 O 16 P 31
S 32 Li 7 Na 23 K 39 Cs 133 Ba 137
Cu-64 Fe-56
一、选择题(本题包括8小题,每小题4分,共32分,每小题只有一个选项符合题意。请把答案的代号填入答题卡内)
1.下列反应中生成物总能量高于反应物总能量的是
A 碳酸钙受热分解 B 乙醇燃烧
C 铝粉与氧化铁粉末反应 D 氧化钙溶于水
2.下列各组热化学方程式程中,化学反应的△H前者大于后者的是
①C(s)+O2(g)=CO2(g); △H1 C(s)+1/2O2 (g)=CO(g); △H2
②S(s)+O2(g)=SO2(g); △H3 S(g)+O2 (g)=SO2 (g); △H4
③H2(s)+1/2O2(g)=H2O(g); △H5 2H2(g)+O2 (g)=2H2O (l); △H6
④CaCO3(s)=CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)=Ca(OH)2 (s);△H8
A ① B ④ C ②③④ D ①②③
3.下列物质性质的变化规律,与共价键的键能大小有关的是
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI极易溶于水且稳定性越来越差
C.金刚石、二氧化硅、碳化硅和晶体硅的硬度、熔点、沸点依次降低
D.AgF、AgCl、AgBr、AgI的熔点依次降低,溶解度也依次降低,颜色却依次加深
4.1999年2月1日俄罗斯和美国同时宣布,成功合成了113号和115号新元素,已知115号元素的一种核素289115X,下列有关叙述正确的是
A.115号元素的平均相对原子质量为289
B.该115号元素的这种核素中,质量数与电子数之差为184
C.该115号元素原子与碳-12原子质量之比为115∶12
D.115号元素应在第七周期第ⅤA族,可显+5价
5.下列对进行焰色反应实验操作注意事项的说明正确的是:( )
①要透过蓝色钴玻璃观察钾的火焰颜色 ②先把铂丝烧到与原来火焰颜色相同,再蘸取被检测的物质 ③每次实验后,要用盐酸或硫酸把铂丝洗净 ④实验时最好选择本身较微弱的火焰 ⑤没有铂丝,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确 C.仅有⑤不正确 D.全对
6.下列说法中正确的是:( )
A.氢键是一种强度介于离子键和共价键之间的化学键,其主要影响物质的化学性质。
B.由共价键结合而成的晶体可以是分子晶体,分子晶体中也可能含有金属阳离子。
C.含有离子键的化合物一定是离子化合物,含有极性键的分子一定是极性分子。
D. 只含共价键而无范德瓦尔斯力的晶体为原子晶体
7.从下列事实所列出的相应结论正确的是
| 实 验 事 实 | 结 论 | |
| A | NH3的水溶液可以导电 | NH3是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
8.通过复习总结,你认为下列对化学知识概括合理的是
A.氧化物不可能是还原产物,只可能是氧化产物
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.根据中和热定义可知,强酸与强碱反应时,不论反应的量为多少,经计算其中和热的数据都为 57.3 kJ/mol
D.离子反应的本质是反应物的某些离子的的浓度的减少,氧化-还原反应的本质是电子的转移(得失和偏移)
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
9.金属钠能在液氨中溶解为蓝色的液氨溶液,蓝色据认为是生成了电子的氨化物,即e(NH3)n-的缘故,有反应Na+nNH3=Na++e(NH3)n-。小心蒸去氨可得白色固体NaNH2,而且有以下反应发生:2Na+2NH3=2NaNH2+H2,下列说法不正确的是:
A.液氨不能发生电离 B.钠与液氨反应生成的氢气既是氧化产物又是还原产物
C.钠的液氨溶液是强还原剂 D.蒸发钠的液氨溶液时蓝色会逐渐褪去。
10.已知a、b、c、d、e分别是Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种物质水溶液中的一种,它们相互反应情况如下:
| 注:“↓”表示生成沉淀 “↑”表示生成气体 “—”表示无明显现象 |
| a | b | c | d | e | |
| c | ↓ | ↓ | / | ↑ | — |
| b | ↓ | / | ↓ | — | — |
可以判断c与e分别为( )
A.Ca(HCO3)2与Ba(NO3)2 B.Ca(OH)2与Ba(NO3)2
C.Na2CO3与Ca(HCO3)2 D.HCl与Ca(OH)2
11.下列各组离子,在指定的环境中可能大量共存的是
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、ClO—、Na+
B.在能使pH试纸变红色的溶液中:Na+、S2—、NO3—、CO32—
C.在加入铝粉能产生气体的溶液中:Na+、NH4+、Cl—、NO3—
D.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:K+、S2—、SO32—、NO3—
12.某溶液可能含有Na+、Ag+、Al3+、AlO2―、S2-、CO32-、SO32―、NO3-等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色为黄色。根据以上实验现象,下列结论中不正确的是( )
A.此溶液中一定有S2-、SO32―、Na+ B.此溶液中可能有AlO2―、CO32-
C.此溶液中一定没有Ag+、Al3+ D.此溶液中可能有S2-和NO3-
13.NA代表阿伏加德罗常数的值,下列说法正确的是
A.含有1 mol P的白磷晶体中,含有的P-P键的数目为1.5 NA
B.含有1 mol硅原子的二氧化硅晶体中,Si—O共价键数为2 NA
C.8.0 g Cu2S和CuO的混合物中约含有铜原子数为0.1NA
D.常温常压下,0.1mol铁与0.1molCl2充分反应,转移的电子数约为0.3NA
14.下列反应的离子方程式正确的是
A.碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O
B.向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
C.1 mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:
2AlO2-+5H+ = Al(OH)3↓+Al3++H2O
D.向硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H++H2O2=Fe3++2H2O
15.一定温度时有摩尔质量为Mg/mol的某溶质R的溶液,当加入Ag不含结晶水的R或蒸发掉Bg水,恢复到原温度时溶液均达饱和,下列说法不正确的是:
A.该温度下R的饱和溶液质量分数是A/(A+B)%
B.该温度下若R的饱和溶液物质的量浓度为Cmol/L,则溶液密度为(A+B)CM/1000B g/mL
C.R在该温度下的溶解度为100A/Bg
D.若原溶液质量分数为50A/(A+B)%,则原溶液质量为2Bg。
16.把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示:
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
下列说法正确的是( )
A、物质C一定是化合物,物质B可能是单质
B、反应后密闭容器中A的质量为19.7g
C、反应过程中,物质B和物质D变化的质量比为87∶36
D、若物质A与物质C的相对分子质量之比为194∶216,则反应中A和C的物质的量之比为1∶2
三、实验题(共2题,22分)
17.(9分)⑴指出下列实验用品或仪器(已洗涤干净)使用时的第一步操作:
①石蕊试纸(检验气体性质)
②容量瓶
⑵下列实验中所选用的仪器或结论不合理的是 (填字母,多选扣分)
A.用托盘天平称量重11.7g氯化钠晶体
B.用碱式滴定管量取25.00mL溴水
C.不宜用瓷坩埚灼烧氢氧化钠、碳酸钠
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
E.用酸式滴定管量取浓硫酸配制一定浓度的稀硫酸时,某同学取前平视,取后俯视,所配硫酸的浓度偏高。
F. 把水滴加到脱脂棉包住的过氧化钠粉末上,脱脂棉可以燃烧,说明该反应为放热反应。
(3)某含结晶水的无色透明晶体,可能是明矾或草酸晶体,为确定其成分,某校化学兴趣小组的同学设计了几种方法:①检验K+;②溶于水检验Al3+;③溶于水利用胶体性质进行检验;④溶于水用石蕊试液检验;⑤与浓硫酸混合共热,将产生的气体用澄清石灰水检验;⑥溶于水再用酸化的高锰酸钾溶液检验。你认为其中的操作步骤没有必要的是________________(填序号,多选扣分)
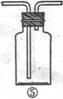
18. (13分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
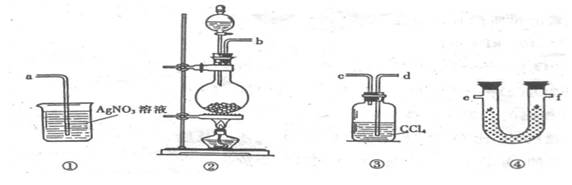
 ⑴请根据甲同学的意图,连接相应的装置,接口顺序:
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接 , 接 , 接a。
⑵U形管中所盛试剂的化学式为 。
⑶装置③中CCl4的作用是 。
⑷乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在 之间(填装置序号),瓶中可以放入 。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成 ,如果观察到
______________________________的现象,则证明制Cl2时有HCl挥发出来。
(6)乙同学把生成的氯气能通入湿润的红色布条中,发现红色褪去。对于使红色布条褪色的物质,乙同学认为氯水中存在的几种粒子都有可能。请你设计实验证明并非氯气的强氧化性或盐酸的酸性在起此作用(请简要叙述实验步骤):
四、填空题(共3题,26分)
19.(8分)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol。某同学用22g液化气(以C3H8计)做实验,测定燃烧放出热量有关数据如下:
①完全燃烧生成CO2和H2O(g)时,放出热量a kJ ;
②不完全燃烧生成CO和H2O(g)时,放出热量b kJ;
③不完全燃烧生成CO、CO2和H2O(g)时,放出热量 c kJ ;
请写出(1)能表示液化气燃烧热的热化学方程式:
(2)CO的燃烧热为 :
(3)第③次实验生成CO的物质的量为 :
20.(8分)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子间距离相同。
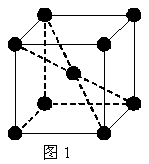
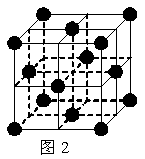
(1)在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为_______个;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为___________;
(2)纯铁晶体在晶型转变前后,二者基本结构单元的边长之比为(1183 K以下与1183 K以上之比)___________。
(3)转变温度前后两者的密度比(1183 K以下与1183 K以上之比)____。
21.( 10分) 将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。
 问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
| 序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
| (1) | 通过增大压强提高原料转化率 | |
| (2) | 使用催化剂增大反应的速率 |
问题3:化学反应中均伴随着能量的变化。如果一个化学
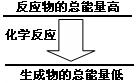 反应中,反应物的总能量和生成物的总能量有如图所示的
反应中,反应物的总能量和生成物的总能量有如图所示的
关系,则该反应过程中的能量变化是 。
已知热化学方程式为:
C(g) + O2(g)= CO2 (g) △H= —393.5KJ/mol
H2 (g) + 1/2O2 (g)= H2O (l) △H= —285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 (保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。如:4Na+O2=2Na2O 2Na+O2![]() Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
反应的原理不同: 。
五、推断题(共2题,17分)
22.(9分)已知aA、bB、cC、dD、eE、gG六种元素原子序数依次增大,原子半径按A、E、D、C、B、G的顺序增大,它们分散在三个短周期中。B是生命体的构架元素,E是同周期中半径最小的元素,也是浓缩分离铀(U)的原料,游离态的E是经过几代人以生命为代价,最终由莫瓦桑制得而荣获1906年诺贝尔化学奖,G的最高价含氧酸的产量是衡量一个国家化工实力的标志。它们的原子序数存在如下关系:①a+b=c,②![]() ,③
,③![]() ,请根据提供的信息,回答下列问题(回答问题时,必须用具体元素符号代替A、B、C、D、E、G):
,请根据提供的信息,回答下列问题(回答问题时,必须用具体元素符号代替A、B、C、D、E、G):
(1)A2是最理想的绿色能源,一般情况下固化得到的是分子晶体。20世纪末,美国卡内基实验室曾获得了它的金属晶体,进一步证明了英国物理学家贝纳尔在1925年的预言:“只要创造条件,任何非金属材料都能变成金属”的正确性。你认为由分子晶体A变成金属晶体A的最必要条件是_______________。
(2)铀是重要的战略物资,它有三种同位素:![]() U、
U、![]() U、
U、![]() U,其中
U,其中![]() U是核材料。但是
U是核材料。但是![]() U与
U与![]() U是形影相随的。分离方法是利用U与E形成UE6气体(E不存在同位素),进行多次扩散纯化分离,请问
U是形影相随的。分离方法是利用U与E形成UE6气体(E不存在同位素),进行多次扩散纯化分离,请问![]() U与
U与![]() U能进行多次扩散纯化分离的原因是_________________________。
U能进行多次扩散纯化分离的原因是_________________________。
(3)碘的非金属性比G强,请任用一离子方程式表示这一结论:
(4)D的一种单质易溶于水,原因是 ,可用湿润的淀粉碘化钾试纸检验其存在,有关反应的方程式为 。
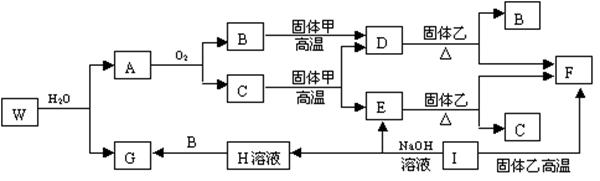
23.(8分)已知固体甲、E、I、F均为常见的单质,其中E在常温下为气态。W是由两种短周期元素组成。乙通常是一种红棕色粉末。G为白色胶状沉淀。W、G、H、I三种物质中都含有同一种的短周期金属元素。A在常温下为气态,与氧气完全反应时的体积比是1:2。各物质有如下图所示的转化关系(部分反应的产物未全部表示)。试回答下列问题:
| |
(1)B的电子式为 ,F原子的结构简图______________。
(2)有上述转化关系图中,C→E、D→F、E→F、I→F、I→E、A→B 等反应中有多个反应属于置换反应,根据要求写出反应式。
非金属元素之间的置换反应__________________________________________;
金属单质置换非金属的置换反应______________________________________;
(3)写出W和水反应的化学方程式_____________________________________。
六、计算题(共2题,21分)
24.(8分)2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
MnO4—+ Fe2++ H+= Mn2++ Fe3++ H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为 mol。
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)
的质量为 g。
(4)混合物中Cu2S的质量分数为 。
|
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 12.60 | 18.90 | 28.00 |
| 二氧化硫的体积/L | 1.12 | 1.68 | 2.24 |
| 硫的质量/g | 1.28 | 1.92 | 2.56 |
(1)样品与硫酸可能发生反应的离子方程式为 。
(2)根据上表数据分析,该样品 (填选项字母)
A.只含有Na2S2O3
B.含有Na2S2O3和Na2SO3两种成分
C.含有Na2S2O3、Na2SO3和Na2SO4三种成分
(3)试计算:该样品中各成分的物质的量之比。
(4)求所加硫酸溶液的物质的量浓度是多少?
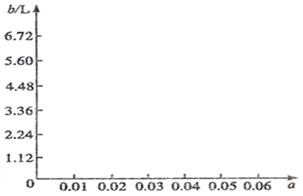
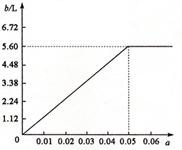
(5)若将63 g该样品与一定量的该硫酸溶液微热,欲计算生成SO2的体积,还需要提供的一个数据是(用a表示该数值,并注明单位) 。
|
高三年级第一次月考化学试题答题纸
一、选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
二选择题
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
三、实验题(共2题,22分)
17.(9分)⑴①
②
⑵不合理的是 (3)没有必要的是________________
18. (13分)
⑴ b接 , 接 , 接a。
⑵化学式为 。 ⑶作用是 。
⑷应加在 之间,瓶中可以放入 。
⑸换成 ,如果观察到
(6)
四、填空题(共3题,26分)
19.(8分)(1)
(2)
(3)
20.(8分)
(1)为_______个;为_________个;(2)___________。(3)
 21.(10分)
21.(10分)
问题1:
问题2:
| 序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
| (1) | 通过增大压强提高原料转化率 | |
| (2) | 使用催化剂增大反应的速率 |
问题3:化学反应中均伴随着能量的变化。如果一个化学
反应中,反应物的总能量和生成物的总能量有如图所示的
关系,则该反应过程中的能量变化是 。
热量的比是 (保留1位小数)。
问题4:反应物相同,反应物的浓度不同,
反应的原理不同: 。
五、推断题(共2题,17分)
22.(9分)(1)是_______________。(2)原因是_________________________。
(3)
(4)是 ,
方程式为 。
23.(8分)
| |
(1)为 ,F原子的结构简图______________。
(2)非金属元素之间的置换反应__________________________________________;
金属单质置换非金属的置换反应______________________________________;
(3)写出W和水反应的化学方程式_____________________________________。
六、计算题(共2题,21分)
24.(8分)
(1) MnO4—+ Fe2++ H+= Mn2++ Fe3++ H2O
(2)为 mol。(3)为 g。 (4)为 。
25.(13分)
(1)为 。 (2)该样品
(3)
(4)
(5)一个数据是 。
|
参考答案
17.⑴①将石蕊试纸润湿(2分) ②检验容量瓶是否漏水(2分)
⑵BD(3分)
(3)④(2分)
18. ⑴ b接e,f接d,c接a(3分)。 ⑵CuSO 4 ⑶吸收Cl2
(4)①③;湿润的KI淀粉试纸(或润湿的有色布条,或品红溶液)
(5)紫色石蕊试液(答案合理给分);紫色石蕊试液变红而不褪色。(每空1分)
(6)把红色干布条放入充满氯气的集气瓶中,布条不褪色;
把红色布条伸入稀盐酸中,红色布条不褪色(各2分)
19.
H2(g)+![]() O2(g)===H2O(1); △H=-285.0kJ/mol
O2(g)===H2O(1); △H=-285.0kJ/mol
(1)C3H8(g)+5O2(g)===3CO2(g)+4H2O(1); △H=-(2a+176)kJ/mol(3分)
(2)(2a-2b)/3 kJ/mol(2分)
(3)1.5(a-c)/(a-b)(3分)
20.(1)8 12
(2)![]()
(3)![]()
五、(本题包括1小题,共10分)
21.问题1: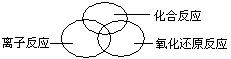 (2分)
(2分)
问题2:(1)合成氨工业 硫酸工业 (其他合理答案也正确) (2分)
问题3:放热; (2分) 4.4 :1 (2分)
问题4;Cu+4H++2NO3-(浓)=Cu2++2NO2↑+2H2O
3Cu+8H++2NO3-(稀)=3Cu2++2NO↑+4H2O(其他合理答案也正确)(2分)
22.(10分)(1)低温、高压(2分)。
(2)利用U与F化合形成UF6,根据![]() UF6与
UF6与![]() UF6式量的差异,进行多次扩散纯化分离。(2分)
UF6式量的差异,进行多次扩散纯化分离。(2分)
(3)S2—+ I2 = S+2I—,(2分)
(4)O3为极性分子所以易溶于水;
O3+2KI+H2O=2KOH+I2+ O2(各2分)
23.(8分)(1)![]() ;
;![]() 。(2分)
。(2分)
(2)C→E:H2O+C![]() CO+H2(2分);
CO+H2(2分);
I→E:2Al + 2NaOH + 2H2O = 2NaAlO2-+ 3H2↑;(2分)
(3)Al4C3 + 12H2O = 3CH4↑+ 4Al(OH)3↓(2分)
24.(8分)
(1)1、5、8、1、5、4
(2)0.007
(3)19.6
(4)40%
25.解:(1)S2O32—+2H+ S↓+SO2↑+H2O SO32—+2H+
SO2↑+H2O
(2)C
三份样品质量比为:12.60 g : 18.90 g : 28.00 g = 1:1.5:2.2
三份样品生成硫的质量比为:1.28 g : 1.92 g : 2.56 g = 1:1.5:2.0
故第一、二份样品完全反应第三份样品过量
若样品全为Na2S2O3·5H2O,则生成![]()
若样品全为Na2SO3,则生成![]()
故样品中含Na2SO4,又![]() ∴样品中含Na2SO3
∴样品中含Na2SO3
综上,样品中含有Na2S2O3·5H2O、Na2SO3、Na2SO4。答案C。
(3)选择第一份样品所提供的数据计算如下:![]()
由Na2S2O3+H2SO4 Na2SO4+ S
+ SO2↑ +H2O
0.04 mol 0.04mol 0.04mol
可知![]()
![]()
所以![]()
(4)第三份样品因过量故H2SO4全部反应。
|
![]()
故消耗n(H2SO4)=0.08 mol+0.02 mol=0.1 mol
![]()
(5)硫酸溶液的体积a L(或a mL)
设63 g样品中含x mol Na2SO3
则含Na2S2O3·5H2O为4x mol Na2SO4 x mol 则有:248×4x+126x+142x=63 x=0.05 mol
当0<a<0.05时,b=112a L 当a=0.05时,b=112a L=5.6 L 当a>0.05时,b=5.6 L