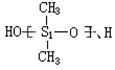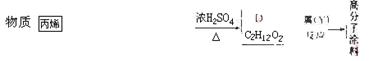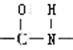高三年级上学期化学模底考试
化学试卷
YCY
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项是符合题意。)
1.遇有下列情况,及时处理有误的是 ( )
A.误食重金属盐,立即喝生牛奶或蛋清
B.皮肤不慎沾有苯酚,立即用酒精擦洗
C.金属钠着火,立刻用砂子覆灭
D.晚间进入厨房,闻有很浓的煤气味,立即开灯检查
2.下列各原了或离子的电子排布式错误的是 ( )
A.Si 1s22s22p2 B.O2- 1s22s22p6
C.Na+ 1s22s22p6 D.Al 1s22s22p63s23p1
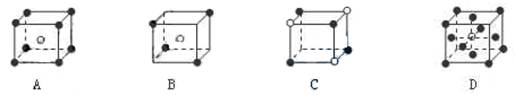
3.有下列离子晶体的空间结构示意图。图中●和化学式中M分别代表阳离子,图中○和化学式中N分别代表阴离子,则化学式为MN3的晶体结构为 ( )
|
4.氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
A.两种分子的中心原子子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
D.氨气分子是极性分子而甲烷是非极性分子。
5.在密闭容器里,A与B反应生成C,其反应速率分别用vA、vB、vC表示,已知2 vB =3 vA、
3 vC = 2vB,则此反应可表示为 ( )
A.2A + 3B = 2C B.A + 3B = 2C
C.3A + B = 2C D.A + B =C
|
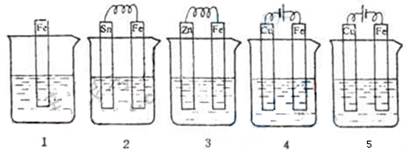
A.4>2>1>3>5 B.2>1>5>3>4
C.5>4>2>3>1 D.3>5>2>4>1
7.实验室用乙醇和浓硫酸混合加热制得的乙烯气体中含少量SO2(记为混合气体①),碳与浓硫酸共热生成的气体中有CO2和SO2(记为混合气体②)。欲除去这两种混合气体中的SO2,下列说法正确的是 ( )
A.都可通过盛有酸性KMnO4溶液的洗气瓶
B.都可通过盛有NaOH溶液的洗气瓶
C.①可用酸性KMnO4溶液洗气,②可用NaOH溶液洗气
D.①可用NaOH溶液洗气,②可用酸性KMnO4溶液洗气
|
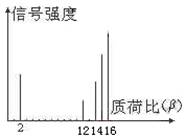
样品的质荷比如下图(假设离子均带一个单位正电
荷,信号强度与该离子多少有关),则该有机物可
能是: ( )
A.CH3OH B.C3H8
|
9.某有机物的分子结构如下表示: ,该分子中最多可以有多少个原子共平面: ( )
|
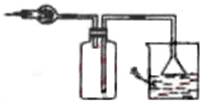
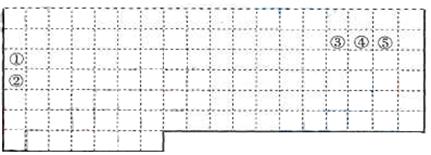
10.在实验室里可按右图所示装置干燥收集气体R,
并吸收多余的R气,则R是( )
A.CH4 B.HCl
C.Cl2 D.NH3
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包含一个选项,多选时,该题为零分;若正确答案包含两个选项,只选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题就为零分)
11.95年美国教授Lagow合成了一种链式炔碳:……―C≡C―C≡C―C≡C……。该物质的一个分子中含300~500个碳原子,性质很活泼。则下列说法错误的是: ( )
A.该物质的溶点比金刚石低
B.该物质可以使溴水褪色
C.该物质属于炔烃
D.该物质与金刚石互为同素异形体
|
A.常压下五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
![]() 13.可以充分说明反应P (g)
+ Q (g) R (g) + S
(g)在恒温下已达到平衡的是 ( )
13.可以充分说明反应P (g)
+ Q (g) R (g) + S
(g)在恒温下已达到平衡的是 ( )
A.反应容器内的压强不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和S的生成速率相等
D.反应容器内的气体总物质的量不随时间变化 ( )
14.已知在1×105Pa、298k条件下,2 mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 ( )
A.H2O(g) = H2(g) +![]() O2(g);△H = +242kJ・mol-1
O2(g);△H = +242kJ・mol-1
B.2H2 (g) + O2(g) + 2H2O (l);△H =-484kJ・mol-1
C.H2(g) +![]() O2(g)
= H2O (g);△H = +242kJ・mol-1
O2(g)
= H2O (g);△H = +242kJ・mol-1
D.2H2 (g) + O2(g) = 2H2O (g);△H =-484kJ・mol-1
15.pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是 ( )
A.反应开始时的速率:甲 = 乙
B.反应所需时间:甲<乙
C.反应开始时,酸的物质的量浓度:甲<乙
D.反应结束时,pH值:甲<乙
|
为: ( )
A.2n + 3m-a B.n + m + a C.m+ 2-a D.m + 2n +2-a
17.近几年一种新型的甜味剂――木糖醇悄悄地走入生活,进入人们的视野,因为木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防踽齿,适合糖尿病患者的优点。木糖醇是一种白色粉末状的结晶,分子式为C5H12O5,结构简式为:CH2OH(CHOH)3CH3OH,下列有关木糖醇的叙述中不正确的是 ( )
A.木糖醇是一种五元醇
B.木糖醇是一种无糖型植物甜味剂
C.木糖醇跟葡萄糖、果糖一样,属于单糖
D.木糖醇理论上可以分子内脱水生成环醚
18.甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是:
![]() (CH3)2C=O + HCN (CH3)2
C(OH)CN
(CH3)2C=O + HCN (CH3)2
C(OH)CN
![]() (CH3)2C(OH)CN
+ CH3OH + H2SO4 CH2=C (CH3)COOCH3
+ NH4HSO4
(CH3)2C(OH)CN
+ CH3OH + H2SO4 CH2=C (CH3)COOCH3
+ NH4HSO4
90年代新法的反应是:CH3C≡CH + CO + CH3OH CH2=C (CH3)COOCH3与旧法比较,新法的优点是: ( )
A.原料无爆炸危险 B.原料都是无毒物质
|
|
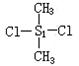
19.硅橡胶 是由二四基二氯硅烷 经两种反应而制得的,这
两种反应依次是 ( )
A.消去、加聚 B.水解、缩聚 C.氧化、缩聚 D.取代、缩聚
20.2005年9月始,“禽流感”在全球部分地区爆发,引起了人们继“非典型性肺炎”之后的世界范围内的恐慌。做好环境消毒是预防“禽流感”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-,下列有关说法中正确的是 ( )
A.ClO2的分子结构呈V型,属非极性分子
B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以1 mol物质得电子的数目表示)是Cl2的5倍
C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害
D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3 + 2NaCl3 + H2SO4= 2Na2SO4 + 2ClO2↑+ H2O
三、(本题含3小题,共28分)
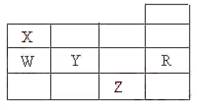
21.(10分)Ⅰ.下表中的实线表示元素周期表的部分边界。①―⑤分别表示元素周期表中对应位置的元素。
|
(1)请在上表中用实线补全元素周期表边界。
(2)元素⑤的原子核外p电子数比s电子总数多 个,元素③氢化物的电子式为 。
(3)元素④一般在化合物中显 价,但与 形成化合物时,所显示的价态则恰好相反。
|
a.元素①的单质 b.元素②的单质
c.元素①②形成的合金 d.无法判断
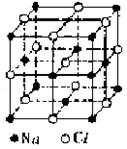
Ⅱ.已知NaCl的摩尔质量为Mg・mol-1,食盐晶体的密度
为ρg・cm-3,若右图中Na+与最邻近的Cl-的核间距离
为acm,那么阿伏加德罗常数的值可表示为
22.(8分)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题
(1)当它们pH相同时,其物质的量浓度由大到小排列是 。
(2)当它们的物质的量浓度相同时,其pH由大到小排列是 。
(3)中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为 。
(4)体积和浓度相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反需烧碱溶液的体积关系为 。
23.(10分)(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值 (填一定增大、一定减小、或可能增大也可能减小)。
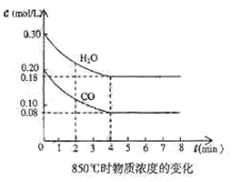
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
![]() CO (g) + H2O
(g) CO2
(g) + H2 (g) △H<0
CO (g) + H2O
(g) CO2
(g) + H2 (g) △H<0
CO和H2O浓度变化如下图,则O―4min的平均反应速率v (CO) = mol / (L・min)
|
|
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min―4min之间反应处于 状态;
C1数值 0.08mol / L(填大于、小于或等于)。
②反应在4 min―5min间,平衡向逆方向移动,可能的原因是 (单选),
表中5 min―6min之间数值发生变化,可能的原因是 (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
四、(本题含3小题,共28分)
24.(10分)有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程图生产的。流程图中:A和M (C3HO)都可发生银镜反应,M和N的分子中碳原子数相同,A的烃基上的一氯代物有3种。
|
(1)写出
|
(2)
(3)N+ O2 M O2
(4)反应 催化剂→C3H4O催化剂
|
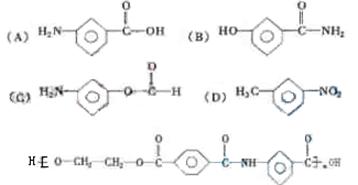
25.(11分)已知―NH3连在苯环上显碱性 连在苯环上显中性,化学式为C7H7NO2的有机物中其分子结构中有一个苯环,两个侧链(间位),符合下列条件的结构简式为:
(1)既有酸性又有碱性 ;
(2)只有酸性 ;
(3)只有碱性 ;
|
(5)由于―COOH能跟―NH2形成 ,所以可用乙二醇、对苯二甲酸跟上述既显酸性又显碱性的物质发生反应,生成高分子化合物[(C17H13NO5)]。该化合物为高强度纤维材料,其结构简式为 。
26.(7分)我国研制的长征捆绑式火箭在第一、二级发动机中用“偏二甲(基)肼”和四氧化二氮作为液体燃料。
①已知偏二甲(基)肼的相对分子质量为60,其中含碳40%,含氢13.33%,其余为氮;又知其分子中有一个氮原子不与氢原子相连。写出偏二甲(基)肼分子的化学式和结构简式:化学式 ,结构简式 。
②在发动机中偏二甲(基)肼在四氧化二氮中充分燃烧,写出该燃烧反应的化学方程式(反应中所有的氮元素均转化为N2) 。
五、(本题含2小题,共24分)
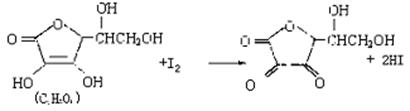
|
(1)下列说法中正确的是( )
A.上述反应为取代反应 B.滴定时可用淀粉溶液作批示剂
C.滴定时可用甲基橙作指示剂 D.锥形瓶不能用待测橙汁润洗
(2)上述实验前要配制7.50×10-3mol/L的标准碘溶液100mL。除玻璃棒外,还需要的玻璃仪器有 等(填编号)
A.容量瓶 B.烧杯 C.维形瓶 D.烧瓶
(3)标准碘液放入 (填仪器名称),滴定时,眼睛注视 ,直到滴定终点。滴定至终点的现象是 。
(4)滴定过程中能否剧烈摇动锥形瓶 (填能或不能),为什么
。
(5)若经数据处理,滴定中消耗的标准碘溶液的体积是15.00mL,锥形瓶中注入的待测橙汁是20.00mL,则此橙汁中维生素C的含量是 mg/L该橙汁 (填“是”或“不是”)纯天然的新鲜橙汁
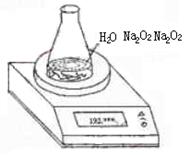
28.(12分)某种含有少量氧化钠的过氧化钠试样(试样质量为1.560g、锥形瓶和水的质190.720g),利用左图装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如表:
|
|
(1)写出Na2O2和H2O反应的化学方程式
(2)计算过氧化钠质量分数时,必需的数据是
不必作第6次读数的原因是
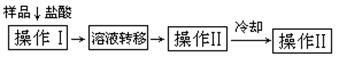
|
①操作Ⅱ的名称是
②需直接测定的物理量是
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要 、 (固定、夹持仪器除外)
④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果 (填偏大、偏小或不变)。
参考答案
1.D 2.A 3.B 4.C 5.A 6.A 7.D 8.D 9.C 10.D
11.C 12.D 13.C 14.AD 15.AC 16.C 17.C 18.CD 19.BD 20.D
21.(10分)Ⅰ.(1)略 (2)1个 H :N :H (3)-2 氟 (4)C Ⅱ.M/2a3p
22.(8分)(1)①>②>③,(2)①>②>③,(3)①=②=2/③,(4)①=②=③/2,
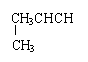 23.(10分)(1)可能增大也可能减小
(2)0.03 (3)①平衡 大于 ②d a
23.(10分)(1)可能增大也可能减小
(2)0.03 (3)①平衡 大于 ②d a
24.(10分)(1)CH3CH2CH2CHO CH2 = CHCHO (2)
![]()
(3)CH2 = CHCOOH + CH3(CH2)3OH CH2 = CHCOO(CH2)3CH3 + H2O
(4)加成反应,加聚反应
|
26.(7分)①偏二甲(基)肼分子式为:C2H8N2
|
![]() ②(3分)C2H2N2 + 2N2O 2CO2↑+ 4H2O↑+3N2↑
②(3分)C2H2N2 + 2N2O 2CO2↑+ 4H2O↑+3N2↑
27.(12分)(1)B D(2分) (2)A B (2分)
(3)酸式滴定管;锥形瓶;溶液呈蓝色(3分)
(4)不能;维生素C易被空气氧化(2分)
(5)990(2分);不是(1分)
28.(12分)(1)2Na2O2 + 2H2O = 4NaOH + O2↑
(2)试样质量、锥形瓶加水的质量、第4(或5)次读数(或用具体数值表示),锥形瓶内质量已达恒重 (3)①蒸发 ②NaCl的质量 ③烧杯 玻璃棒 ④偏大