高三年级化学上学期月考二
化 学
YCY时量:90分钟 满分:100分
第Ⅰ卷(选择题,共45分)
可能用到的原子量:C 12 O 16 Na 23 S 32 Cu 64
一、选择题(共15题,每题3分,共45分,每小题只有一个正确的选项,请将选项填写在答卷表格内)
1.2006年3月5日,温家宝在十届全国人大四次会议上所作的“政府工作报告”中指出:“抓好资源节约,建设环境友好型社会”,这是我国社会及经济长期发展的重要保证。你认为下列行为中有悖于这一保证的是 ( )
A.开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料
B.将煤进行气法处理,提高煤的综合利用效率
C.研究采煤、采油新技术,且提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle)
2.用NA表示阿伏加德罗常数,下列说法不正确的是 ( )
A.标准状态下的辛烷22.4L完全燃烧产生CO2分子数为8NA
B.18g水中所含电子数为10NA
C.46gNO2和46gN2O4中所含原子数均为3NA
D.1L 2mol・L-1的Mg(NO3)2溶液中含NO![]() 离子数为4NA
离子数为4NA
3.下列反应对应的离子方程式中正确的是 ( )
A.FeCl3溶液中加入铁粉:Fe+Fe3+ 2Fe2+
B.NH4HSO4溶液中加入少量NaOH:NH![]() +OH-
+OH- NH3・H2O
C.饱和石灰水与饱和CaCl2溶液混合:Ca2++2OH-===Ca(OH)2↓
D.氯气通入Na2SO3溶液中:Cl2+SO![]() +H2O
+H2O
SO![]() +2HCl
+2HCl
4.某溶液中含有大量的Al3+、NH![]() 、Ag+、Fe2+四种离子。向该溶液中加入足量Na2O2,微
、Ag+、Fe2+四种离子。向该溶液中加入足量Na2O2,微
热并充分搅拦后,再加入过量稀盐酸,此时溶液中大量存在的阳离子可能是 ( )
A.H+、Na+、Al3+、NH![]() B.Al3+、H+、Na+、Fe2+
B.Al3+、H+、Na+、Fe2+
C.H+、Na+、Al3+、Fe3+ D.Fe3+、Ag+、Na+、H+
5.锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合
物叙述正确的是 ( )
A.Li2SO4难溶于水 B.Li与N2反应产物是Li3N
C.LiOH易溶于水 D.LiOH与Li2CO3受热都很难分解
6.用已准确称量过的氯化钠固体配成1.00mol・L-1的NaCl溶液0.5L,下列仪器:①坩埚
②分液漏斗 ③容量瓶 ④烧瓶 ⑤胶头滴管 ⑥烧杯 ⑦玻璃棒 ⑧托盘天平,其中要
用到的是 ( )
A.③④⑤⑦ B.①②⑤⑥⑧ C.③⑤⑥⑦ D.①③⑤⑥⑦
7.已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙
炔燃烧的热化学方程式正确的是 ( )
A.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-4bkJ/mol
B.2C2H2(g)+5/2O2(g) 2CO2(g)+H2O(l);△H =-2bkJ/mol
C.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H =-2bkJ/mol
D.2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H =bkJ/mol
8.NaH是一种离子化合物,与水反应时生成烧碱和氢气,它也能与乙醇、液氨等反应产生氢气。下列有关NaH的叙述正确的是 ( )
A.跟水反应时,水既作氧化剂又作还原剂 B.NaH中阳离子半径大于阴离子半径
C.跟液氨反应时,生成氢气外,还生成铵盐
D.与乙醇反应时,放出氢气的速率比与水反应时更快
9.已知I-、Fe2+、SO2、Cl-与H2O2均具有还原性,它们在酸性溶液中还原性的强弱顺序为
Cl-<Fe2+< H2O2<I-<SO2。则下列反应不能发生的是 ( )
A.2Fe3++SO2+2H2O 2Fe2++SO![]() +4H+ B.I2+ SO2+2H2O
+4H+ B.I2+ SO2+2H2O H2SO4+2HI
C.H2O2+ H2SO4 SO2↑+O2↑+2H2O D.2 Fe3++I2 2Fe2++2I-
10.硫代硫酸钠可作为脱氯剂,已知25.0mL 0.100mol・L-1 Na2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O![]() 将转化成 ( )
将转化成 ( )
A.S- B.S C.SO![]() D.SO
D.SO![]()
11.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为 ( )
A.1:1:1 B.2:2:1 C.2:3:1 D.4:3
12.已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol
下列结论正确的是 ( )
A.碳的燃烧热大于110.5kJ/mol B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
13.向各盛有1L水的A、B、C、D四个烧杯中分别加入等物质的量的钠、氧化钠、过氧化钠和氢氧化钠,固体完全溶解后,各杯溶液中溶质的质量分数的顺序是 ( )
A.D>C>B>A B.B=C>A>D C.B=C>A=D D.B>C>A>D
14.把NaHCO3和Na2O2的混合物放在密闭容器中加热。关于混合物加热前后消耗盐酸的物质的量.下列判断正确的是 ( )
A.加热前消耗的多 B.加热后消耗的多
C.加热前后一样多 D.当Na2O2适量时才会一样多
15.由一种阳离子和两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以产生氯气,下列关于的混盐CaOCl2判断,不正确的是 ( )
A.该混盐与硫酸反应产生1molCl2时转移2NA个电子
B.该混盐的水溶液显碱性
C.该混盐具有较强的氧化性
D.该混盐中氯元素的化合价为+1价和-1价
第Ⅱ卷(非选择题,共55分)
二、填空题(本题包括5小题,共48分)
16.(6分)火箭推进器中盛有强还原剂液态肼(N2H2)和强氧化剂液态双氧水。当它们混合反应时,YC即产生大量氮气和水蒸汽,并放出大量热。已知0.4mol液态肼和足量的液态双氧水反应,生成氮气和水蒸气,放出256.652kJ的热量。
(1)反应的热化学方程式为 。
(2)又已知:H2O(l) H2O(g);△H=44kJ/mol。则16g液态肼和足量的液态双氧水反应生成液态水时放出的热量是
kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有很大的优点是
。
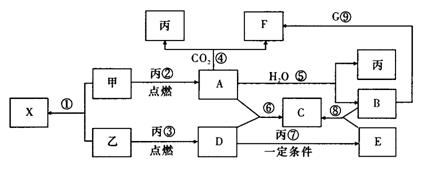
17.(12分)甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族,丙为无色气体。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同。G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图:
|
请回答:
(1)用化学式表示:丙为 ,C为 ,X的电子式为 。
(2)写出A与H2O反应的化学反应方程式
。
(3)写出B与G溶液反应的离子方程式: 。
(4)在上图的反应中,不属于氧化还原反应的是(填序号) 。
18.(8分)阅读下列材料:
①早在1785年,卡文迪许在测定空气组成时,除去空气中的氧气、氮气等已知气体后,发现最后总是留下一个体积是总体积1/200的小气泡。
②1892年,瑞利在测定氮气密度时,从空气中得到的氮气密度为1.2572g/L,而从氨分解得到的氮气密度为1.2508g/L。两者相差0.0064g/L。
③瑞利和拉姆赛共同研究后认为:以上两个实验中的“小误差”可能有某种必然的联系,并预测大气中含有某种较重的未知气体。经反复实验,他们终于发现了化学性质极不活泼的惰性气体――氩。
请回答下列问题:
(1)空气缓慢依次通过氢氧化钠溶液、浓硫酸、灼热铜粉(过量)、灼热镁粉(过量),最后用排水法收集,则依次除去的气体是 、 、 、 。
(2)材料①②的“小误差”对测定空气和氮气密度的实验而言是 (填“主要因素”或“次要因素”)
(3)材料③中科学家抓住了“小误差”而获得重大发现说明
。
|
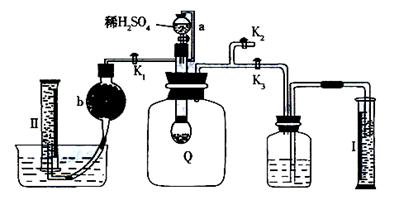
(1)Q内发生化学反应时,生成的气体是 。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是
,应当打开的是 。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是
。
(4)b中装的固体试剂是 ,为什么要缓缓打开K1?
。
(5)实验结束时,量筒I中有xmL水,量筒II中收集到ymL气体(已折算成标准状态)则过氧化钠的纯度的数学表达式是
(化成最简表达式)。
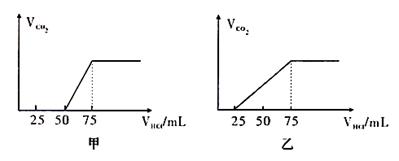
20.(12分)有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100mL,并向此稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的CO2气体体积(标况)与所加入的盐酸的体积之间的关系如下图所示:
|
试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是 ,
其物质的量之比是 ,产生的CO2气体体积(标况)是 。
乙所得溶液中存在的溶质是 。
其物质的量之比是 ,产生的CO2气体体积(标况)是 。
三、计算题(共7分)
21.在稀硫酸溶液中,4.48gCu2S和CuS的混合物与100mL
0.75mol・L-1的MnO![]() 反应生成了SO
反应生成了SO![]() 、Cu2+和Mn2+。剩余的MnO
、Cu2+和Mn2+。剩余的MnO![]() 恰好与35.0mL 1.00mol・L-1 FeSO4溶液反应。
恰好与35.0mL 1.00mol・L-1 FeSO4溶液反应。
(1)配平下列反应化学方程式:
Cu2S+ MnO![]() + H+
+ H+ Cu2++ SO![]() + Mn2++ H2O
+ Mn2++ H2O
(2)试计算原始混合物中Cu2S的质量分数。
参考答案
一、选择题:本大题共23小题,每小题3分,共计69分。
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 | C | A | C | C | B | A | A | B | C | D | B | A | B | C | A |
二、填空题
16.(1)N2H4(l)+2H2O2(l) N2(g)+4H2O(g) △H=-641.63kJ/mol
|
|
(2)2H2O+2Na2O2=4NaOH+O2↑ (3)OH-+HCO![]() =CO
=CO![]() +H2O
+H2O
(4)⑧⑨
18.(1)CO2 H2O O2 N2
(2)次要因素
(3)科学研究应有严谨的科学态度
19.(1)O2、CO2 (2)K1、K2 K3
(3)①气球逐渐变小 ②量筒II中有气体进入,水被排出
(4)碱石灰 控制气流量,使CO2能被碱石灰充分吸收
(5)78y/(53x+25y)
20.NaOH和Na2CO3 1:1 0.056L Na2CO3和NaHCO3 1:1 0.112L
三、计算题
21.(1)1 2 8 2 1 2 4
(2)解:由题意可设混合物中Cu2S和CuS的物质的量分别为x、y
MnO![]() ―― 5FeSO4
―― 5FeSO4
FeSO4溶液消耗的MnO![]() 的物质的量为
的物质的量为
35.0mL×1.00mol・L-1×1/5×10-3=0.007mol根据:
Cu2S――2MnO![]() 5CuS――8Mn
5CuS――8Mn![]()
x 2x y 8y/5 ……………………………①
可得方程式:2x+8y/5=100m×0.75mol・L-1×10-2-0.007
又由题设可得:160x+96y=4.48…………………………………………………………②
联立①②可解:x=0.01 y=0.03
原始混合物中Cu2S的质量分数为:0.01×160/4.48×100%=35.7%