高三年级化学上学期第一次月考试题
化 学
相对原子量:H 1 O 16 Na 23 Cl 35.5 S 32 Fe 56
客观卷(50分)
一 选择题(本题包括25小题,每题2分,共50分,每题只有一个正确选项符合题意)
1.你认为减少酸雨产生的途径可采取的措施是 ( )
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫; ④在已酸化的土壤中加石灰;⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
2.接触法生产H2SO4过程,对废气,废水,废渣,“废热”的处理正确的是 ( )
①尾气用氨水处理 ②污水用石灰乳处理 ③废渣用来造水泥,炼铁;④设置“废热”锅炉产生蒸气,供热或发电。
A.只有①② B.只有①③④ C.只有①②③ D.全部
3.下列各组物质晶体中,化学键的类型相同,晶体的类型也相同的是 ( )
A.SO2和SiO2 B.CCl4和KCl C.NaCl和HCl D.CO2和H2O
4.下列晶体熔化时,化学键没有被破坏的是 ( )
A.氯化铵 B.金刚石 C.冰醋酸 D.硫酸钠
5.下列各种物质中按熔、沸点由低到高顺序排列正确的是 ( )
A.O2 I2 Hg B.CO2 KCl SiO2
C.Na K Rb D.SiC NaCl SO2
6.下列变化过程一定不可逆的是 ( )
A.溶解 B.水解 C.电解 D.分解
7.一定条件下,硝酸铵受热分解的未配平化学方程式为:![]() ,在此反应中被氧化与被还原的氮原子数之比为 ( )
,在此反应中被氧化与被还原的氮原子数之比为 ( )
A.5:3 B.5:4 C.1:1 D.3:5
8.被称为万能还原剂的NaBH4,溶于水并和水反应:
![]() ,下列说法正确的是 ( )
,下列说法正确的是 ( )
A.NaBH4既是氧化剂又是还原剂;
B.NaBH4是氧化剂,水是还原剂;
C.硼元素被氧化,氢元素被还原;
D.氢气既是氧化产物又是还原产物。
9.下列事实与胶体性质无关的是 ( )
A.在豆浆里加入盐卤做豆腐;
B.河流入海处易形成沙洲;
C.一束平行光线照射蛋白质溶液,从侧面可看到光亮的通路;
D.三氯化铁溶液中滴入氢氧化钠溶液,出现了红褐色沉淀,。
10.将淀粉与碘化钾的混合溶液装在半透明袋中,浸泡于盛有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行以下实验,能证明半透明膜有破损的是 ( )
A.加入AgNO3溶液,产生黄色沉淀C
B.加入碘水,不变色;
C.加入碘水,变蓝色;
D.加入氯水,不变蓝色。
11.下列过程需通电后才可进行的是 ( )
①电离 ②电解 ③电镀 ④电泳 ⑤电化学腐蚀
A.①②③ B.②③④ C.②④⑤ D.全部
12.在透明的酸性溶液中,能大量共存的离子组是 ( )
A.![]()
![]()
![]()
![]()
B. ![]()
![]()
![]()
![]()
![]()
C.![]()
![]()
![]()
![]()
D.![]()
![]()
![]()
![]()
13.下列各组离子中,因发生氧化还原反应而不能大量共存是 ( )
A.![]()
![]()
![]()
![]()
B. ![]()
![]()
![]()
![]()
C.![]()
![]()
![]()
![]()
D.![]()
![]()
![]()
![]()
14.下列反应的离子方程式书写不正确的是 ( )
A.次氯酸钙溶液中,通入过量的二氧化碳气体
![]()
B.醋酸和碳酸氢钠溶液混合
![]()
C.氯化亚铁溶液中通入氯气
![]()
D.金属钠跟水反应
![]()
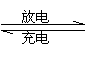 15.镍氢电池是近年开发出来可充电电池,它可以取代会产生镉污染的镉镍电池。镍氢电池的总反应方程式是:
15.镍氢电池是近年开发出来可充电电池,它可以取代会产生镉污染的镉镍电池。镍氢电池的总反应方程式是:![]()
![]() ,根据此反应式判断,下列叙述正确的是 ( )
,根据此反应式判断,下列叙述正确的是 ( )
A.电池放电时,Y电池负极周围溶液的PH不断增大
B.电池放电时,镍元素被氧化
C.电池充电时,氢元素被还原
D.电池放电时,H2是正极
16.X是第二周期元素,能与氧形成X2O5,则有关下列有关X的叙述正确的是 ( )
A.X的单质在常温下以分子晶体形式存在
B.X2O5的水化物是一种弱酸
C.X的氢化物在固体时属于分子晶体
D.、X所在族元素的单质在固态时属同类型晶体
17.1克氢气燃烧生成液态水,放出142.9Kj热,下列表示该反应的热化学方程式正确的
是 ( )
A.![]()
B.![]()
C.![]()
D.![]()
18.下列反应能用勒沙特列原理解释的是( )
A.由SO2和O2反应制SO3需使用催化剂
B.燃烧粉碎的黄铁矿矿石有利于SO2的生成
C.硫酸生产中用98.3%的硫酸吸收SO3,而不用水或稀H2SO4吸收SO3。
D.用N2和H2合成氨需采用高压
19.下列有关晶体的叙述中,不正确的是 ( )
A.金刚石的网状结构中,由共价键形成的碳原子环,其中最小的环上有6个碳原子
B.在氯化钠晶体中,每个Na+或Cl-的周围紧邻6个Cl-或6个Na+;
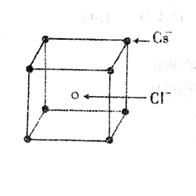
C.在氯化铯晶体中,每个Cs+周围紧邻8个Cl-,每个Cl-周围也紧邻8个Cs+
D.干冰晶体熔化时,1mol干冰要断裂2mol碳氧双键
20.用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的PH依次为升高,降低,不变的是 ( )
A.AgNO3 CuCl2 Cu(NO3)2
B.KBr Na2SO4 CuSO4
C.CaCl2 KOH NaNO3
D.HCl HNO3 K2SO4
21.除去混在SO2中的SO3气体,须通过以下哪种溶液 ( )
A.NaOH溶液 B.饱和Na2SO3溶液
C.饱和NaHCO3溶液 D.98.3%H2SO4
22.已知![]() 均具有还原性,且在酸性溶液中的还原性依次增强,。下列各反应不可能发生的是 ( )
均具有还原性,且在酸性溶液中的还原性依次增强,。下列各反应不可能发生的是 ( )
A.![]()
B.![]()
C.![]()
D.![]()
23.下列叙述正确的是 ( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电镀槽的阴极
④电解食盐水时阴极产生氢气,阳极产生氯气
⑤钢铁表面易锈蚀生成Fe2O3・nH2O
A.①②③④⑤ B.①③④⑤
C.①③⑤ D.②④
24.将含0.4mol CuSO4和0.4mol NaCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol铜,在另一电极上析出气体在标准状况下的体积是 ( )
A.5.6L B.6.72L C.13.44L D.11.2L
|
A.![]() B.
B.![]()
C.![]() D.
D.![]()
|
二、填空题(共有两大题,共23分)
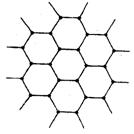
26.(9分)(1)右图为石墨的晶体结构
俯视图。在石墨晶体中C原子数与
C―C键数之比为 。
(2)I2与![]() 反应,产物之一为
反应,产物之一为![]() ,请写出并配平该反应的离子方程式
,请写出并配平该反应的离子方程式
(3)已知每克固体葡萄糖在人体中完全氧化生成液态水可释放出15.6KJ的能量,写出葡萄糖氧化的热化学方程式 。
(4)接触法制硫酸的工业设备有 , , 。
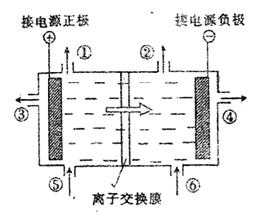
27.(14分)下图是目前世界上比较先进的电解制碱技术―离子交换膜法的示意图。
|
(1)在电解过程中,与电源正极相连的电极上所发生的方程式 。与电源负极相连的电极负极溶液PH值 。(填:不变,升高或降低)电解反应的总化学方程式为 。
(2)写出②,④表示的生成物:② ,④ (填化学式)
(3)溶液中的Na+,H+,Cl-,OH-能通过离子交换膜的是
(4)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为
(选a、b、c,多选扣分)。
,加入试剂的合理顺序为
(选a、b、c,多选扣分)。
a.先加NaOH,后加Na2CO3,再加钡试剂;
b.先加NaOH,后加钡试剂,再加Na2CO3;
c.先加钡试剂,后加Na2CO3,再加NaOH;
三、实验题(12分)
|
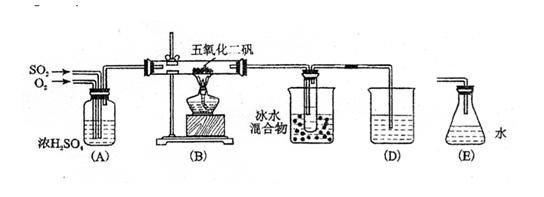
(1)装置A的作用是 。
(2)反应进行一段时间后,C中可观察到的现象是 。
(3)若将C换为E,实验过程中可观察到的现象是 ,这是因为 。
(4)使SO2和O2按体积比1:1混合,且控制通入B的速率使之充分反应,由C导出的气体是 ,气体存在的原因是 。
参考答案
客观卷(50分)
一 选择题(本题包括25小题,每题2分,共50分,每题只有一个正确选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 19 | 11 | 12 | 13 |
| 答案 | C | D | D | C | B | C | A | D | D | C | B | D | A |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 | A | C | C | C | D | D | D | D | C | B | A | D |
主观题(50分)
二、填空题(共有两大题,共23分)
26.(9分)(1)2:3 ;(2)![]()
(3)![]()
(4)沸腾炉,接触室,吸收塔。
27.(14分)(1)2Cl--2e===Cl2;升高;
2NaCl+2H2O====H2↑+Cl2↑+2NaOH。
(2)H2 、NaOH(3)Na+ H+ (4)b c
28.(1)①干燥气体 ②使两种气体混合均匀 ③通过观察气泡控制气体流速;
(2)由无色晶体析出;(3)液面上有酸雾产生;SO3与H2O剧烈反应,放出大量的热,形成酸雾;
(4)O2;SO2,SO3 SO2与O2的反应为可逆反应,不能完全转化。
29.(1)![]() ;
;
![]()
![]()
![]()
(2)1.48t
30.5.5mol/L