高三年级化学上学期第一次月考试题
化学试题
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。考试时间120分钟。作答第Ⅰ卷前,请考生务必将自己的姓名、考试证号用书写黑色字迹的0.5毫米的签字笔填写在答题卡上,并认真核对。
2.第Ⅰ卷答案必须用0.5毫米的签字笔填在答题卡上,在其他位置作答一律无效。每小题选出答案后,用0.5毫米的签字笔把答题卡上题号对应栏表格内写上答案。
可能用到的相对原子质量:
H-1 C-12 O-16 S-32 C1―35.5 Na-23 Br-80
Pd-106 I-127 Ba-137 Ag-108
第Ⅰ卷 (选择题 共64分)
一、选择题(本题包括8小题。每小题4分,共32分。每小题只有一个选项符合题意。)
1.保护环境是每一个公民的责任。下列做法:①推广使用无磷洗涤剂,②城市生活垃圾分类处理,③推广使用一次性木质筷子,④推广使用清洁能源,⑤过量使用化肥、农药,⑥推广使用无氟冰箱。其中有利于保护环境的是
A.①②④⑤ B.②③④⑥ C.①②④⑥ D.③④⑤⑥
2.下列有关说法不符合事实的是
A.同温同压下,气体的体积取决于气体的物质的量的多少
B.元素的相对原子质量取决于该元素各核素的相对原子质量和在自然界中的原子百分比
C.氯化钠投入到酒精中将形成胶体
D.氧化剂的氧化性强弱取决于该氧化剂中某元素化合价的高低
3.奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维,聚酯纤维的结构简式为:
![]() ,则下列说法不正确的是
,则下列说法不正确的是





A.羊毛与聚酯纤维的化学成分不相同
B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维单体为对苯二甲酸和乙二醇
D.由单体合成聚酯纤维的反应属加聚反应
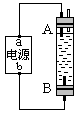 4.某学生设计了一种电解法制取Fe(OH)2的实验装置。通电后,溶液中产生大量白色沉淀,且较长时间不变色。下列说法中不正确的是
4.某学生设计了一种电解法制取Fe(OH)2的实验装置。通电后,溶液中产生大量白色沉淀,且较长时间不变色。下列说法中不正确的是
A.电源中的a 为正极,b为负极
B.可以使用NaCl溶液作电解液
C.A、B两端都必须使用铁作电极
D.B电极发生的反应为2H2O+2e-=H2↑+2OH―
5.设NA为阿伏加德罗常数,下列叙述正确的是
A.1mol FeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒
B.标准状况下,2.24 L 乙醛完全燃烧所得CO2分子数为0.2 NA
C.1L 0.1mol・L-1的醋酸溶液中的分子总数大于0.1NA
D.通过化学反应制得1mol O2,转移电子的数目一定是4NA
6.发生原电池的反应通常是放热反应,在理论上可设计成原电池的化学反应是
A.C(s)+H2O(g)=CO(g)+H2(g) ;△H>0
B.Ba(OH)2・8H2O+2NH4Cl(s)=BaCl2(aq)+2NH3・H2O(l)+8H2O(l); △H>0
C.CaC2(s)+2H2O(l)=Ca(OH)2(s)+C2H2(g) ;△H<0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ;△H<0
7.下列各组离子,在指定的环境中一定能大量共存的是
A.在pH为7的溶液中:Ag+、K+、SO42-、Cl-
B.在能使pH试纸变深蓝色的溶液中:Na+、S2-、NO3-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3-
D.在由水电离出的c(OH-)=10-13mol・L-1的溶液中:Na+、Ba2+、NO3-、I-
8.科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现A1的超原子结构A113和A114,并在质谱仪检测到稳定的Al13I-等。A113、A114的性质很象现行周期表中的某主族元素,已知这类超原子当具有40个价电子时最稳定。下列说法不正确的是
A.All4与ⅡA族元素性质相似
B.A113与卤素性质类似
C.A113在气相中与HI反应的方程式可表示为:A113+HI=HAl13I
D.A113超原子中A1原子间是通过离子键结合的
二、选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分)
9.t℃时,将100g某物质A的溶液蒸发掉10g水,恢复至t℃,析出2.5g晶体。再蒸发掉10g水,恢复至t℃,析出7.5g晶体。下列说法中不正确的是
A.t℃时原100g溶液是饱和溶液
B.若析出的晶体中不含结晶水,则可计算出t℃时A的溶解度
C.若析出的晶体中含有结晶水且已知晶体的化学式和相关元素的相对原子质量,就可以计算出t℃时A的溶解度
D.根据题给条件可以计算出原溶液溶质的质量分数
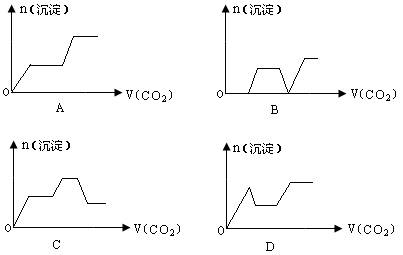
10.将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为:
11.下列反应离子方程式正确的是
A.向氯化铝溶液中加入过量氢氧化钠溶液:Al3+ + 4OH―=AlO2― + 2H2O
B.向苯酚钠溶液中通入二氧化碳:CO2 + H2O + 2C6H5O―→2C6H5OH + CO32―
C.向小苏打溶液中加入醋酸溶液:HCO3―+ HAc=Ac―+CO2↑+ H2O
D.向溴化亚铁溶液中通入过量氯气:Fe2+ + 2Br―+ 2Cl2=Fe3+ + Br2 + 4Cl―
12.1840年,俄国化学家盖斯(G・H・Hess)从大量的实验事实中总结出了一条规律:化学反应不管是一步完成还是分几步完成,其反应热是相同的,即盖斯定律。盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ/mol,则1mol C与O2反应生成CO的反应热△H为
A.-Y kJ/mol B.-(10X-Y) kJ/mol
C.-(5X-0.5Y) kJ/mol D.+(10X-Y) kJ/mol
13.2004年4月30号出版的《Science》杂志报道了中国科学家郑兰荪院士首次成功合成新型稳定小富勒烯C50Cl10,外侧有10个氯原子,其形状酷似太空船(见下图)。有关C50Cl10的说法不正确的是
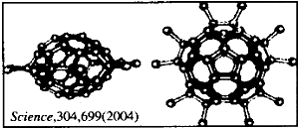
A.C50Cl10摩尔质量为955g・mol-1 B.C50Cl10晶体是原子晶体
C.C50Cl10分子中含有25个碳碳双键 D.C50Cl10分子中共用电子对数目为105
14.强酸和强碱稀溶液的中和热可表示为:
H+(aq)+OH-(aq)=H2O(1);ΔH=-57.3kJ・mol-1
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(1);ΔH1
![]() H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=![]() Na2SO4(aq)+H2O(1);ΔH2
Na2SO4(aq)+H2O(1);ΔH2
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1);ΔH3
上述反应物除已注明的外均为稀溶液,则ΔH 1、ΔH 2、ΔH 3的关系正确的是
A.ΔH1=ΔH2=ΔH3 B.ΔH2<ΔH1<ΔH3
C.ΔH2<ΔH 3<ΔH1 D.ΔH2=ΔH3<ΔH1
15.在恒温恒容的密闭容器中,发生反应3A(g)+B(g)![]() xC(g)。
xC(g)。
Ⅰ、将3molA和2molB在一定条件下反应,达平衡时C的体积分数为a;
Ⅱ、若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。下列说法正确的是
A.若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大
B.若向Ⅰ平衡体系中再加入3molA和2molB,C的体积分数若大于a,可断定x>4
C.若x=2,则Ⅱ体系起始物质的量应当满足3n(B)=n(A)+3
D.若Ⅱ体系起始物质的量当满足3 n(C) +8n(A)=12n(B)时,可断定x=4
16.甲、乙两种物质溶解度曲线如右图所示:下列说法一定正确的是
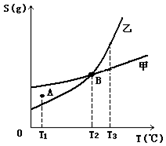 A.A点表示T1℃时甲的溶液已饱和,乙的溶液未饱和
A.A点表示T1℃时甲的溶液已饱和,乙的溶液未饱和
B.B点表示T2℃时甲、乙两物质的溶液均达饱和且两溶液
的物质的量浓度相等
C.将T3℃时甲、乙两物质的饱和溶液分别降温至T2℃,析
出的乙比析出的甲多
D.若乙中含有少量的甲,可用重结晶的方法提纯乙
第Ⅱ卷 (非选择题 共86分)
三、(本题包括2小题,共19分)
17.(8分)下列实验操作或对实验事实的叙述正确的是 (填序号)。
①为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液
②向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
③使用胶头滴管的任何实验都不允许将滴管插入液面以下
④为了获得胆矾晶体,可将CuSO4溶液蒸干、灼烧到质量不再发生变化时为止
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑥用石英坩埚高温熔融NaOH和Na2CO3的固体混合物
⑦配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
⑧用洁净的玻璃棒蘸取浓HNO3,点在pH试纸中部以测定此浓HNO3的pH
18.(11分)下图是化学研究小组设计的铜与稀硝酸反应的两个实验装置图。其中装置Ⅰ为甲同学设计。(注:NaOH溶液可吸收NOx)
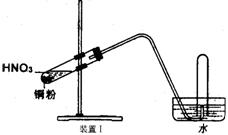
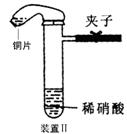
请回答下列问题:
⑴如何检验该装置Ⅰ的气密性?
。
⑵铜与稀硝酸反应的离子方程式为 。
⑶乙同学认为装置Ⅰ中收集的气体不能确定铜与稀硝酸反应生成的是NO气体,理由 ,于是他设计装置Ⅱ。
⑷化学研究小组的其它同学对上述实验进行了研究,认为装置Ⅱ虽然作了改进,但如果按装置Ⅱ进行实验,还是会出现三个问题,需要作相应改进措施。请你帮助他们填写相关内容。
问题一: 。
措施:加热或 。
问题二:试管中的气体是淡棕红色,而不是无色。
措施:
(填具体操作。不能增加装置)。
问题三: 。
措施: 。
四、(本题包括2小题,共17分)
19.(8分)无机过氧化合物的科学研究开始于18世纪初,人们相继制得了过氧化钡、过氧化钠、过氧化钾、过氧化氢等,目前无机过氧化合物逐渐成为无机化学的一个分支,其中过氧化氢是用途最广的过氧化物。试回答下列问题。
⑴Na2O2、K2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与稀硫酸作用,过滤即可制得。最适合的过氧化物是 (写电子式)。
⑵过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子方程式:
。
⑶与过氧化氢具有相同电子总数且属于非极性分子的有 、 (举两例,写化学式)。
⑷纯的过氧化氢常用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态过氧化氢反应,生成N2和H2O(g),放出256.6kJ的热量。.则该反应的热化学方程式为:
。
20.(9分)NH4NO3在不同条件(温度)下加热分解,可能发生非氧化还原反应,也可能发生氧化还原反应。
⑴若NH4NO3在通常条件下加热的分解产物不出下列范围,根据已学知识(化合价升降规律等)判断,下列反应可能的是 。
A、NH4NO3→N2+O2+H2O B、NH4NO3→NH3+HNO3
C、NH4NO3→O2+HNO3+H2O D、NH4NO3→N2+HNO3+H2O
E、NH4NO3→N2+NH3+H2O F、NH4NO3→N2O+H2O
⑵现将NH4NO3晶体在三种不同温度下加热使其分解,若分解产物能发生如图所示的转化关系(仅反应条件及反应Ⅱ、Ⅲ两个反应中生成的水被略去),回答下列问题:
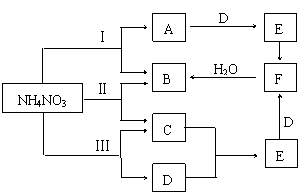

①写出下列物质的分子式
A、 E、 F、
②请写出反应Ⅲ的化学方程式 。
五、本题包括1小题,共12分。
21.(12分)某化学研究性学习小组讨论Fe3+和SO32―之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32―+H2O=2Fe2++SO42―+2H+;
二是发生双水解反应:2Fe3++3SO32―+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
【实验Ⅰ】学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,作者设计这个实验的目的是 。
【实验Ⅱ】取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是 。向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是 。将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生血红色现象的离子方程式是 。
【实验Ⅲ】换用稀释的FeCl3和Na2SO3溶液重复实验,Ⅱ、Ⅲ产生的现象完全相同。由上述实验得出的结论是 。
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是__________________________________________________________________。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①___________________________________________________________________________;
②___________________________________________________________________________。
六、(本题包括2小题,24分)
22.(10分)已知烯烃在不同条件下可与氯气发生加成反应或发生烷基氢的取代反应。现以原料A开始实现下列转化:
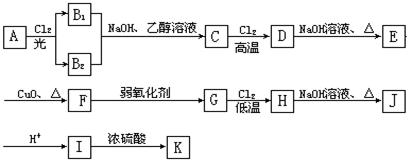
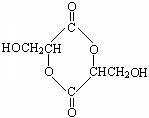 K的结构简式为:
K的结构简式为:
请回答下列问题:
⑴B1、B2的结构简式分别为: , 。
⑵E转化为F的化学方程式: 。
⑶H的结构简式为: 。
J的结构简式为 。
⑷写出上述属于加成反应的化学方程式 。
23.(14分)已知:①R-OH+HBr![]()
![]() R-Br+H2O
R-Br+H2O
②卤代烃和金属镁在乙醚中反应生成卤代烃基镁(RMgX),称为Grignard试剂,它是重要的有机合成试剂,可与羰基化合物反应制醇,反应过程如下:
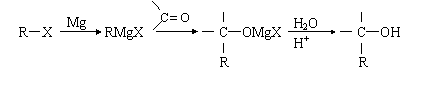

⑴现仅用A(CH3OH)而不添加任何其他有机试剂,无机试剂可自选。经多步反应(其中包括Grignard试剂的反应),得到如下反应过程:
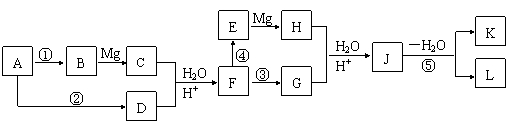

试回答下列问题:
①写出F的结构简式 ,它和A互称 。
②上述转化中的①-⑤反应,属于氧化反应的是 ,属于取代反应的是 。(只填序号)
⑵现实验室以甲醇和乙醇为原料,合成CH3COOC(CH3)3。用合成反应流程图表示出最合理的合成方案(注明反应条件)。
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:


七、本题包括2小题,共14分。
24.(6分)取50.0mL Na2CO3和Na2SO4的混合溶液,加入过量的BaCl2溶液,过滤、洗涤并干燥后得到14.51g白色固体;再用过量的稀硝酸处理该白色固体,其质量减少到4.66g。试计算:
⑴原混合溶液中Na2CO3和Na2SO4的物质的量浓度。
⑵产生的气体在标准状况下的体积。
25.(8分)有一种可溶性氯化物、溴化物、碘化物的混合物,对其进行如下测定:
①称取试样5.00g,溶于水后加入足量AgNO3溶液,使卤离子完全沉淀为卤化银,质量为
3.57g。将该卤化银加热并通入氯气使AgBr、AgI完全转化为AgCl后,其质量变为2.87g。
②称取试样15.00g,溶于水后加入氯化亚钯(PdCl2)处理后,其中只有碘化物转化为PdI2
沉淀,该沉淀的质量为2.16g。
请回答下列问题:
⑴步骤①称取的试样中,所有卤原子的物质的量之和是 mol,该试样中碘原子的物质的量是 mol。
⑵列式计算原混合物中溴的质量分数和氯的质量分数。