高三化学选择题专项训练(11)
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1、2004年4月22日是第35个“世界地球日”,我国确定的主题是“善待地球——科学发展”。下列行为中不符合这一主题的是
A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.大量开采地下水,以满足社会对水的需求
C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D.节约能源,提高能源利用率
2、下列实验操作正确的是
A.将氢氧化钠固体放在滤纸上称量
B.用10mL量筒量取8.58mL蒸馏水
C.制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D.配制氯化铁溶液时,将一定量氯化铁溶解在较浓的盐酸中,再用水稀释到所需浓度
3、在恒温时,一固定容积的容器内发生如下反应: N2O4(g)![]() 2NO2(g),达平衡时,再向容器内通入一定量的 N2O4
(g),重新达到平衡后,与第一次平衡时相比,N2O4的体积分数
2NO2(g),达平衡时,再向容器内通入一定量的 N2O4
(g),重新达到平衡后,与第一次平衡时相比,N2O4的体积分数
A.增大 B.减小 C.不变 D.无法判断
4、将A g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将B g (A>B)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是
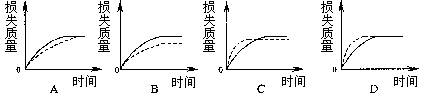
5、下列各组气体或溶液用括号内试剂加以鉴别,其中不合理的是
A.二氧化碳、二氧化硫、一氧化碳(品红溶液)
B.氯化钠、硝酸银、碳酸钠(稀盐酸)
C.酒精、醋酸、醋酸钠(石蕊试液)
D.硫酸、硝酸钡、氯化钾(碳酸钠溶液)
6、下列各分子中,所有原子都满足最外层为8电子结构的是
A.H2O B.BF3 C.CCl4 D.PCl5
7、在医院中,为酸中毒病人输液不应采用
A.0.9%氯化钠溶液 B.0.9%氯化铵溶液
C.1.25%碳酸氢钠溶液 D.5%葡萄糖溶液
8、下列离子方程式中正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:
Ba2++2OH-+2H++SO![]() == BaSO4↓+2H2O
== BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH![]() + OH-== NH3↑+ H2O
+ OH-== NH3↑+ H2O
C.苯酚钠溶液中通入少量二氧化碳:
![]() -O-+CO2+H2O —→
-O-+CO2+H2O —→ ![]() -OH+HCO
-OH+HCO![]()
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2 == 2Fe3++Br2+4Cl-
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
9、下列物质中属于共价化合物的是
A.苛性钠 B.氢碘酸 C.硫酸 D.氯气
10、常温时,向pH =2的硫酸中加入等体积的下列溶液后,滴入甲基橙试液,出现红色,该溶液可能是
A.pH =12的Ba(OH)2 B.0.005mol/L NaOH
C.pH =12的氨水 D.0.05mol/LBaCl2
11、在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法不正确的是
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌等量
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
12、若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
A.Al3+ Na+ NO![]() Cl- B.K+ Na+ Cl- NO
Cl- B.K+ Na+ Cl- NO![]()
C.K+ Na+ Cl- AlO![]() D.K+ NH
D.K+ NH![]() SO
SO![]() NO
NO![]()
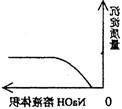
13、下列实验过程中产生的现象与对应的图形相符合的是
A.NaHSO3粉末加入HNO3溶液中 B.H2S气体通入氯水中
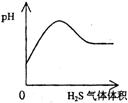
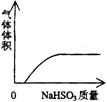
C.NaOH溶液滴入Ba(HCO3)2溶液中 D.CO2气体通入澄清石灰水中
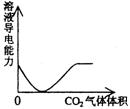
14、下列指定微粒的个数比为2﹕1的是
A.Be2+离子中的质子和电子
B.![]() 原子中的中子和质子
原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
15、以Fe为阳极,Pt为阴极,对足量的 Na2SO4 溶液进行电解,一段时间后得到4 mol Fe(OH)3沉淀,此间共消耗水的物质的量为
A.6mol B.8mol C.10mol D.12mol
16、若以w1和w2分别表示浓度为c1 mol/L和c2 mol/L硫酸的质量分数,已知2 w1=w2,则下列推断正确的是(硫酸的密度比纯水的大)
A.2c1=c2 B.2c2=c1 C.c2>2c1 D.c1<c2<2c1
17、下列说法正确的是
A.苯酚、淀粉KI、乙酸、氢氧化钾四种溶液可用FeCl3溶液一次鉴别
B.CH3CH2OH、 CH2=CHCOOH、 CH3CHO、 CH3COOH四种溶液可用新制Cu(OH)2一次鉴别
C.CaCl2溶液中混有少量HCl,可加入过量的CaO,再过滤
D、KCl溶液中混有少量KI,可通入足量Cl2后,再用乙醇进行萃取、分液
18、A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去):
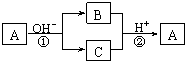 |
下列判断正确的是
A.X元素可能为Al B.X元素一定为非金属元素
C.反应①和②互为可逆反应 D.反应①和②一定为氧化还原反应
19、某温度下,某容积恒定的密闭容器中发生如下可逆反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)
H2(g)+CO2(g) ![]() H>0当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
H>0当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
A、升高温度 B、加入催化剂
C、再加入n molCO和n molH2O D、再加入2n molCO2和2n molH2
20、某温度下,在密闭容器中发生如下反应:
2A(g)+ B(g) ![]() 2C(g),若开始时只充入2mol C气体,达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol A和1mol B的混合气体,达到平衡时A的转化率为
2C(g),若开始时只充入2mol C气体,达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2mol A和1mol B的混合气体,达到平衡时A的转化率为
A.20% B. 40% C. 60% D. 80%