高三化学选择题专项训练(12)
一、 选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1、下列物质的水溶液能导电,但属于非电解质的是
A.CH3CH2COOH B.Cl2
C.NH4HCO3 D.SO2
2、水的电离过程为H2O![]() H++OH-,在不同温度下其电离常数为K(25℃)=
H++OH-,在不同温度下其电离常数为K(25℃)=![]() ,K(35℃)=
,K(35℃)=![]() 。则下列叙述正确的是
。则下列叙述正确的是
A.![]() 随着温度的升高而降低
B.
在35℃时,
随着温度的升高而降低
B.
在35℃时,![]()
C.水的电离度![]() D.水的电离过程是吸热的
D.水的电离过程是吸热的
3、已知反应A+3B![]() 2C+D在某段时间内以A的浓度变化表示的化学反应速率为1 mol・L-1・min-1,则此段时间内以C的浓度变化表示的化学反应速率为
2C+D在某段时间内以A的浓度变化表示的化学反应速率为1 mol・L-1・min-1,则此段时间内以C的浓度变化表示的化学反应速率为
A.0.5 mol・L-1・min-1 B.1 mol・L-1・min-1
C.2 mol・L-1・min-1 D.3 mol・L-1・min-1
4、某些化学试剂可用于净水。水处理中使用的一种无机高分子混凝剂的化学式可表示为 [Al2(OH)nClm・yH2O]X ,式中m等于
A.3-n B.6-n C.6+n D.3+n
5、硫代硫酸钠可作为脱氯剂,已知25.0mL 0.100 mol・L-1 Na2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O![]() 将转化成
将转化成
A.S2-
B.S
C.SO![]() D.SO
D.SO![]()
6、下列实验中用错试剂的是
A.用稀盐酸清洗做焰色反应的镍铬丝
B.用酒精萃取碘水中的碘
C.用稀硝酸洗去残留在试管壁上的铜
D.用碱石灰吸收氨气中的水蒸气
7、b g某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气。则该金属的相对原子质量为
A.2b/a B.3b/2a C.a/3b D.3b/a
8、绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列制备环氧乙烷的反应中,原子利用率最高的是
![]() A.
A.
![]() B.
B.
![]() C.
C.
![]() D.
D.
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
9、下列变化规律中正确的是
A.H2S,HCl,PH3的热稳定性由弱到强
B.物质的量浓度相等的NaCl,MgCl2,AlCl3三种溶液的pH由小到大
C.等质量的甲烷、乙烯、乙炔充分燃烧,所耗用氧气的量由多到少
D.![]() ,
,![]() ,
,![]() 的酸性由弱到强
的酸性由弱到强
10、取pH均等于2的盐酸和醋酸各100 mL分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋酸分别与锌反应的速率一样大
11、向下列溶液中通入过量CO2,最终出现浑浊的是
A.氢氧化钙饱和溶液 B.苯酚钠饱和溶液
C.醋酸钠饱和溶液 D.氯化钙饱和溶液
12、某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是
A.乙酸丙酯 B.乙酸乙酯
C.乙酸甲酯 D.甲酸乙酯
13、已知:电离度α=![]() ×100%。室温时,0.01 mol・L-1某一元弱酸的电离度α为1%,则下列说法正确的是
×100%。室温时,0.01 mol・L-1某一元弱酸的电离度α为1%,则下列说法正确的是
A.上述弱酸溶液的pH=2
B.加入等体积0.01 mol・L-1 NaOH溶液后,所得溶液的pH=7
C.加入等体积0.01 mol・L-1 NaOH溶液后,所得溶液的pH>7
D.加入等体积0.01 mol・L-1 NaOH溶液后,所得溶液的pH<7
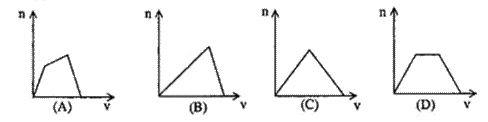
14、将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(v)的关系正确的是
15、在相同温度时100 mL 0.01mol/L的醋酸溶液与10 mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是
A.中和时所需NaOH的量 B.电离程度
C.H+的物质的量 D.CH3COOH的物质的量
16、混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是
A.向CuSO4溶液中加入适量铁粉
B.等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液
C.等物质的量的NaHCO3与Na2O2固体
D.在NaBr溶液中通入过量氯气
17、在一定温度下,某无水盐R在水中溶解度为23g,向R的饱和溶液中加入![]() 该无水盐,保持温度不变,析出R的结晶水合物Wg,从原饱和溶液中析出溶质R的质量为
该无水盐,保持温度不变,析出R的结晶水合物Wg,从原饱和溶液中析出溶质R的质量为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
18、已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A.H2O(g) == H2(g)+![]() O2(g);ΔH=+242kJ・mol-1
O2(g);ΔH=+242kJ・mol-1
B.2H2(g)+O2(g) == 2H2O(l);ΔH=-484kJ・mol-1
C.H2(g)+![]() O2(g) == H2O(g) ;ΔH=+242kJ・mol-1
O2(g) == H2O(g) ;ΔH=+242kJ・mol-1
D.2H2(g)+O2(g) == 2H2O(g);ΔH=-484kJ・mol-1
19、下面是实验室制取氨气的装置和选用的试剂,其中错误的是
A.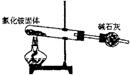 B.
B.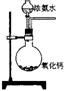 C.
C. D.
D.
20、对某酸性溶液(可能含有Br-,SO![]() ,H2SO3,NH
,H2SO3,NH![]() )分别进行如下实验:
)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。
对于下列物质不能确认其在溶液中是否存在的是
A.Br- B.SO![]() C.H2SO3 D.NH
C.H2SO3 D.NH![]()
附加题:
21.航天飞行器座舱内空气更新过程如图所示: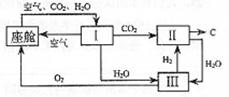
(1)Ⅱ是CO2和H2的反应装置,该反应的化学方程式:
。
(2)从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,宇航员每天消耗28molO2,呼出23molCO2,则宇航员每天呼出的气体中含H2O mol。
(3)以下是另一种将CO2转化为O2的实验设想:
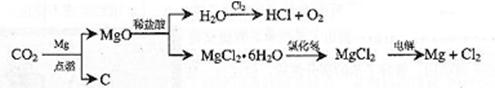
其中,由MgCl2・6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:
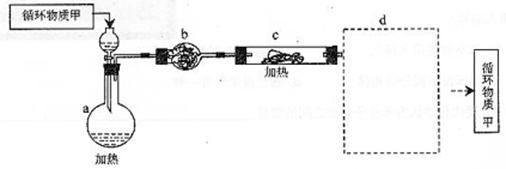 ①上图中,装置a由
、
、双孔塞和导管组成。
①上图中,装置a由
、
、双孔塞和导管组成。
②循环物质甲的名称是 。
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是
。
④装置b中填充的物质可能是 (填入编号)
c.硅胶 f.碱石灰 g. 无水氯化钙 h.浓硫酸
⑤设计d装置要注意防止倒吸,请在方框中画出d装置的简图,并要求与装置c的出口处相连(铁架台不必画出)。