高三化学选择题专项训练(15)
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1、随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
2、久置于空气中的下列物质,因被氧化而呈黄色的是
A.浓硝酸 B.氯化亚铁溶液
C.溴苯 D.溴化银
3、下列每组物质发生状态变化所克服的粒子间的相互作用属于同类型的是
A.食盐和蔗糖熔化 B.钠和硫熔化
C.碘和干冰升华 D.二氧化硅和氧化钠熔化
4、提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
5、下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A.H3O+、NO![]() 、Fe2+、Na+ B.Ag+、NO
、Fe2+、Na+ B.Ag+、NO![]() 、Cl-、K+
、Cl-、K+
C.K+、Ba2+、OH-、SO![]() D.Cu2+、NH
D.Cu2+、NH![]() 、Br-、OH-
、Br-、OH-
6、2001年9月1日将执行国家食品卫生标准规定,酱油中3―一氯丙醇(ClCH2CH2CH2OH)含量不得超过1ppm。相对分子质量为94.5的氯丙醇(不含主![]() 结构)共有
结构)共有
A.2种 B.3种 C.4种 D.5种
7、下列过程中,不涉及化学变化的是( )
A.用明矾净化水
B.甘油加水作护肤剂
C.烹鱼时加入少量的料酒和食醋可减少腥味,增加香味
D.烧菜用过的铁锅,经放置常出现红棕色斑迹
8、下列化合物中阴离子半径和阳离子半径之比最大的是
A.CsF B.NaBr C.KCl D.LiI
二、选择题(本题包括12小题,每小题4分,共48分。每小题有一个或两个选项符合题意。)
9、铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(标况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为
A.9.02g B.8.51g C.8.26g D.7.04g
10、在一密闭容器中,反应aA (g)![]() bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向逆反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数增加了 D.a>b
11、将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
A.c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B.c (Ac-)>c (Cl-)>c (HAc)>c(H+)
C.c (Ac-)=c (Cl+)>c (H+)>c (HAc)
D.c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-)
12、1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:
X(g)+a Y(g)![]() b Z(g)
b Z(g)
反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的![]() ,则a和b的数值可能是
,则a和b的数值可能是
A.a=1,b=1 B.a=2,b=1
C.a=2,b=2 D.a=3,b=2
13、以下实验能获得成功的是
A.用钠检验乙醇中是否有水
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
14、![]() 代表阿伏加德罗常数值,下列说法正确的是
代表阿伏加德罗常数值,下列说法正确的是
A.9g重水所含有的电子数为![]()
B.1molMgCl2中含有离子数为3![]()
C.![]() 氯气与足量NaOH溶液反应转移的电子数为
氯气与足量NaOH溶液反应转移的电子数为![]()
D.1molC10H20分子中共价键总数为30![]()
15、类推是在化学学习和研究中常用的思维方法,但类推出的结论最终要经过实践的检验才能决定其正确与否,下列几种类推结论中不正确的是
A.钠、镁都是活泼金属,由金属钠和镁引起火灾都不能用干冰灭火器灭火
B.NaHSO3溶液能与NaAlO2反应生成白色沉淀,NaHCO3溶液也能与NaAlO2反应生成白色沉淀
C.NH4Cl、NH4I结构相似,将两种固体分别加热,都分解生成HX和NH3
D.原电池中通常是活泼金属做负极,不活泼金属做正极,用铜和铝与浓硝酸构成原电池时,铝是负极
16、某硝酸盐受热分解的产物为金属氧化物和NO2、O2。下列相关叙述正确的是
A.分解产生的气体能使余烬木条复燃,证明其中含有氧气
B.若分解的固体产物全为CuO,则产生的混合气体从理论上说可恰好完全溶解于水
C.若产生NO2和O2的物质的量之比为6:1,则金属元素在分解过程中化合价降低
D.若3.76g Cu(NO3) 2无水晶体受热分解,得到1.52g固体,则固体中有Cu2O 0.72g
17、对于某些离子的检验及结论一定正确的是
A.加入稀盐酸,产生无色并能使澄清石灰水变浑浊的气体,一定有CO32-或SO32-
B.加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.某气体能使湿润红色石蕊试纸变蓝,该气体一定显碱性
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
18、在化学上,常用一条短线表示一个化学键。在如图所示的结构中,直线不表示化学键或不完全表示化学键的是

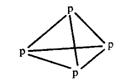
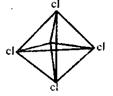
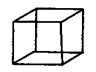
A.石墨 B.白磷 C.CCl4 D.C8H8(立方烷)
19、某学生用优质大理石与稀盐酸反应制取CO2,实验结果表示如下图,对于图中曲线的叙述中正确的是
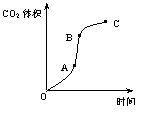 A.AB段表示反应速率最快,因产物中的CaCl2可能有催化作用,且反应为放热反应
A.AB段表示反应速率最快,因产物中的CaCl2可能有催化作用,且反应为放热反应
B.BC段表示反应速率最快,在该时间内收集到的气体最多
C.OC段表示随时间增加,反应速率逐渐增大
D.OC段表示反应产物中气体体积随时间的变化关系
20、某温度下,在一容积可变的密闭容器里,反应2A(g) ![]() B(g) + 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol、4mol。在保持温度和压强不变的条件下,下列说法正确的是
B(g) + 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol、4mol。在保持温度和压强不变的条件下,下列说法正确的是
A.充入1mol稀有气体氦(He),平衡将向正反应方向移动
B.充入A、B、C各1mol,平衡将向正反应方向移动
C.将A、B、C各物质的量都减半,C的百分含量不变
D.加入一定量的A气体达平衡后,C的百分含量一定增加
三、非选择题
21、根据下面的反应路线及所给信息填空。
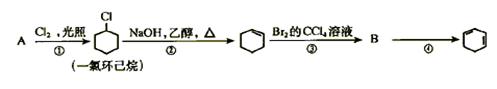
(1)A的结构简式是 ,名称是 。
(2)①的反应类型是 ;②的反应类型是 。
(3)反应④的化学方程式是:
。
22、在一定条件下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1 mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到的N2多1.4g。
(1)写出反应的化学方程式并标出电子转移的方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量可能各是多少。