������ѧͳһ��������
��������������������������������������ѧרҵ��3��
�������������������������������������ˣ�ʷ�����������������ڣ�2006.10.18
�����õ���ԭ������ H��1�� C��12����N��14����O��16����Na��23�� S��32�� K��39
�ڢ����ѡ���⡡��70�֣�
һ��ѡ���⣨ÿ��ֻ��һ����ȷ�𰸣�ÿ��3�֣���30�֣�
1����ӦE+F===G���¶�T1�½��У���ӦM+N===K���¶�T2�½��У���֪T1>T2����E��F��Ũ�Ⱦ�����M��N��Ũ�ȣ�������������ͬ���������ߵķ�Ӧ����
A��ǰ�ߴ�����������B�����ߴ���������C��һ������������������ D�����ж�
2����NA��ʾ�����ӵ�������ֵ��������������ȷ����
A��100g98%��Ũ�����к���ԭ�Ӹ���Ϊ4NA
B��1mol �������к���̼̼˫����ԼΪ3��6.20��1023
C����״���£�22.4LCH4��CH3Cl�Ļ���������еķ�����ĿΪNA
D��60gSiO2�����к�SiO2������ԼΪ6.02��1023
3�������±����г������ݣ��ж������Ȼ�ѧ����ʽ��д����ȷ����
��
| ���� ѧ�� �� | H��H | Cl��Cl | H��Cl |
| ����1mol��ѧ��ʱ�ų������� | 436kJ��mol��1 | 243kJ��mol��1 | 431kJ��mol��1 |
A��![]()
B��![]()
C��![]()
D��![]()
4�������з����Ե�ͬλ�س�֮Ϊ�ȶ�ͬλ�أ��ȶ�ͬλ�ط������ڽ�20����ֲ������ѧ����̬ѧ�ͻ�����ѧ�о��л�ù㷺Ӧ�á�����½����̬ϵͳ�о��У�![]()
![]()
![]()
![]()
![]() �ȳ�������������ָʾ������й�˵����ȷ����
�ȳ�������������ָʾ������й�˵����ȷ����
A��![]() ԭ�Ӻ���������Ϊ16
ԭ�Ӻ���������Ϊ16
B��![]()
![]() ��
��![]()
![]() ����Է���������ͬ
����Է���������ͬ
C��![]() ��
��![]() ԭ�Ӻ��ڵ����������2
ԭ�Ӻ��ڵ����������2
D��![]() ���Ľ��OH����������
���Ľ��OH����������![]() ���ĸ�ǿ
���ĸ�ǿ
5��SO2�dz����Ĵ�����Ⱦ��֮һ���ҹ��涨������SO2�������ó���0.02mg/L�����д�ʩ���ܹ�����SO2�ŷ�������
������Ȼ������ú̿������ȼ�Ϣ�ʹ��ˮú�������ú����ȼ�Ϣ����᳧ʹ��V2O5���������ӿ�SO2��ת�����ʢܽ���״ú���飬�����ȼ��Ч�ʢ���ú�м���ʯ�Һ�ȼ�â�ѭ�������������ų���β��
A���٢ڢۢܢݡ������� B���٢ۢݢޡ������� C���٢ڢݢޡ������� D���ڢۢܢ�
6�� 2005��10��12�գ�������������Ա������������
2005��10��12�գ�������������Ա������������
��Ȫ��������˳�����ղ���5���ȫ���أ������
�ҹ������˺�����ҵ��ȡ���µ�ͻ�ơ���ͼ�ǡ�������
��������ʱ����Ƭ�� �ƶ���ǧ�ֵĻ���ͷɴ��ľ�
�����Ǵ��������ģ���ѧ��Ӧ���������ʹ�õ�ȼ
����ƫ������[(CH3)2NNH2]���������ʱ�����Ļ�ѧ��
ӦΪ��C2H8N2��2N2O4��2CO2����3N2����4H2O����
�����йظ÷�Ӧ��˵����ȷ����
A���÷�Ӧ����������ƫ�����¡����� ��B���÷�Ӧ����ʱֻ�з��ȹ���û�����ȹ���
C���÷�Ӧ�е�Ԫ�صĻ��ϼ����ߡ�������D���÷�Ӧ��ÿ����1mol CO2ת��8mol����
7��������ڻ�ѧѧ�Ƶķ�չ�����˷dz���Ҫ�����á����з������������
���� ����������к��е�Hԭ�Ӹ��������ΪһԪ�ᡢ��Ԫ���
�� ���ݷ�Ӧ���Ƿ��е��ӵ�ת�ƽ���ѧ��Ӧ��Ϊ������ԭ��Ӧ�ͷ�������ԭ��Ӧ
�� ���ݷ�ɢϵ�Ƿ���ж��������ɢϵ��Ϊ��Һ���������Һ
�� ���ݷ�Ӧ�е���ЧӦ����ѧ��ѧ��Ӧ��Ϊ���ȷ�Ӧ�����ȷ�Ӧ
A���٢ۡ��������� B���ڢܡ��������� C���٢ڢܡ��������� D���ڢۢ�
| a | ||||
| b | c | |||
| d | e | |||
| f |
8����ͼ��a��b��c��d��e��fΪԪ�����ڱ���ǰ4���ڵ����ڵ�һ����Ԫ�أ������й�������ȷ����
A��b��c��e����Ԫ�صĵ������Ӱ뾶��С��ϵ�� e>b>c
B������Ԫ���У�dԪ�ص��������ȶ�
C��c���⻯��е��f�⻯��ķе��
D��bԪ�س�0���⣬ֻ��һ�ֻ��ϼۡ�
9�� 24gʯӢ��80gʯ��ʯ�ڸ����³�ַ�Ӧ���ų��������ڱ�״���µ������
�� A��4.48L�������� B��8.96L������ C��11.2L������ D��17.92L
10��һ�����Ͳ���B4C���������������������ߺ����Ƚ�����������B4C���ƶ���ȷ����
A��B4C��һ�ַ��Ӿ��塡������������ B��B4C��һ�����Ӿ���
C��B4C��һ��ԭ�Ӿ��塡������������ D���÷�������4����ԭ�Ӻ�1��̼ԭ�ӹ���
����ѡ���⣨ÿ����1-2����ȷ�𰸣�ÿ��4�֣����ַ�2�֣���40�֣�
11����NAΪ����٤��������ֵ��������������ȷ����
A��92gNO2��N2O4��������к��е�ԭ����Ϊ6NA
B����״���£�11.2LSO3�к��еĵ�����Ϊ20NA
C��0.5mol/L��Ba(OH)2��Һ��OH������ĿΪNA
D��1molMg��������O2��N2��Ӧ����MgO��Mg3N2ʱ��ʧȥ�ĵ�������Ϊ2 NA
12���Ʊ��谱�����ƵĻ�ѧ����ʽ���£�![]() +
+
![]() ���ڸ÷�Ӧ������˵���У���ȷ����
���ڸ÷�Ӧ������˵���У���ȷ����
A����Ӧ�У���Ԫ�ر�������̼Ԫ�ر���ԭ
B��HCN�������������ǻ�ԭ��
C��CaCN2�ǻ�ԭ���H2����������
D��COΪ�������H2Ϊ��ԭ����
13����һ�ܱ������������·�Ӧ��aX(g)��bY(g) ![]() nW(g)����H��Q
nW(g)����H��Q
ij��ѧ��ȤС���ͬѧ���ݴ˷�Ӧ�ڲ�ͬ�����µ�ʵ�����ݣ���������������ͼ��
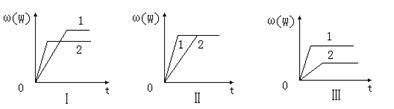
���У���(W)��ʾW�ڷ�Ӧ������еİٷֺ�����t��ʾ��Ӧʱ�䡣������������ʱ�����з���������ȷ����
A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P2��P1��a��b��n
B��ͼ���������ͬ��ͬѹ�´����Է�Ӧ��Ӱ�죬��1ʹ�õĴ���Ч����
C��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P1��P2��n��a��b
D��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1��T2��Q��0
14�������������顢�Ҵ���������������ȼ��ʱ�Ļ�ѧ��ֱ��ת��Ϊ���ܵ�װ�ý�ȼ�ϵ�ء�
ȼ�ϵ�صĻ������Ϊ�缫������ʡ�ȼ�Ϻ������������ֵ�����������ʿɸߴ�80%��һ
����ͷ����ֻ��40%���ң���������ȾҲ�١������й�ȼ�ϵ�ص�˵���������
A������ȼ�ϵ�صĸ�����Ӧ���������������顢�Ҵ�������
B������ȼ�ϵ�س����ں����������ԭ��֮һ�Ǹõ�صIJ���Ϊˮ����������֮��ɹ��Աʹ��
C���Ҵ�ȼ�ϵ�صĵ���ʳ���KOH���õ�صĸ�����ӦΪ
C2H5OH��12e����2CO2����3H2O
D������ȼ�ϵ�ص�������ӦΪO2��2H2O��4e����4OH��
15�����з�Ӧ�����ӷ���ʽ��д�������
A��Ca(HCO3)2��Һ�м���������Ba(OH)2��Һ����
Ca2����2HCO3����2OH����CaCO3����CO32����2H2O
B��3mol��Cl2ͨ�뺬2molFeI2����Һ�С�������
2Fe2����4I����3Cl2��2Fe3����6Cl����2I2
C��FeS�����м���ϡHNO3��������������������
FeS��2H����Fe2����H2S��
D����������Һ��ͨ��������CO2
![]()
16��ij��Һ�к���CH3COO����SO42����SO32����HCO3����CO32�����������ӡ���������Na2O2����������к����ܴ������ڵ�������
A��CH3COO����SO42����HCO3������������������������������������ B��SO42����SO32����CO32��
C��SO32����HCO3���������� ������������������������������������������D��CH3COO����SO42����CO32��
17����ͼ�����Ǻ�ѹ�ܱ����������Ǻ����ܱ�����������������ͬʱ���ڢ��зֱ����3mol Z����ʼʱ���������ΪV L���������·�Ӧ���ﵽƽ��(X��Y״̬δ֪)��aX(?)��2Y(?)![]() 3Z(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ3:2:2��������˵��һ����ȷ���ǡ�����
3Z(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ3:2:2��������˵��һ����ȷ���ǡ�����
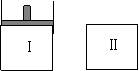
��������
A����X��Y��Ϊ��̬����ƽ��ʱ����ƽ��Ħ����������
B����X��Y����Ϊ��̬����ƽ��ʱX�IJ��ʣ���
C����X��Y��Ϊ��̬�������ʼ��ƽ������ʱ�䣺��>��
D����XΪ��̬��YΪ��̬������ƽ������ڢ����ټ���1molZ������ƽ��ʱZ�����������С
18����SO2ͨ��Fe��NO3��3��Һ�У���Һ����ɫ��Ϊdz��ɫ���������ֱ�Ϊ�ػ�ɫ����ʱ������BaCl2��Һ���������ɫ������������һϵ�б仯�����У����ձ���ԭ����
A��SO2�� B��Cl - ������C��Fe3+���������� D��NO3 -
19����pH=1��ij����Һ��pH=13������������Һ�У�������������Ƭ���ų�H2�����ʵ���֮��Ϊ3: 1��ԭ�������
A������Һ�������ͬ�����Ƕ�Ԫǿ�ᡡ
B������ΪһԪǿ�ᣬ����Һ������Ǽ���Һ�����3��
C������Һ�������ͬ����������
D������ǿ�ᣬ������Һ��Ũ�ȱ�NaOH��ҺŨ�ȴ�
20������A~D���飬ÿ����������Ӧ������������Ӧ����ͬһ�����ӷ���ʽ��ʾ����
| ��I�� | ��II�� | |
| A | ����SO2ͨ��Ba(OH)2��Һ | ����SO2ͨ������Ba(OH)2��Һ |
| B | ����Ũ��ˮ����Al2(SO4)3��Һ | ����Al2(SO4)3��Һ����Ũ��ˮ |
| C | 0.1mol Cl2ͨ�뺬0.2mol FeBr2����Һ | 0.3 molCl2ͨ��0.2molFeBr2��Һ�� |
| D | ����BaCl2��Һ������Na2SO4��Һ���� | ����Ba(NO3)2��Һ�����MgSO4��Һ���� |
�ڶ�������ѡ���� ��80�֣�
����ʵ���⣨��28�֣�
21��(12��) ijѧ��ȡ������Na2SO3��7H2O 50.00g�����ܱ������о�6000C���ϵ�ǿ�������أ�������������������غ����Ʒ�����൱����ˮ�������Ƶļ���ֵ�����Ҹ�Ԫ�ص����Ҳ���ϼ���ֵ������������ˮ��ȴ������Һ�ļ��Դ�����ͬʱ���Ƶ���������Һ����������ʵ���˼������λͬѧ���������ַ�������
��1���������غ����Ʒ����ˮ�����Һ��Ϊ�����ܽ⣬�ɲ�ȡ������ �Ĵ�ʩ���۲췢����Ʒȫ���ܽ⣬��Һ���塣
��2��ȡ������1����������Һ�������������������� (��һ����)�ữ���Ȼ�����Һ�а�ɫ������˵�������к��������� �������ӷ��ţ���
��3����ȡ������1����������Һ���Թ��У��μ��������ᣬ�������ݲ�����ͨ�������� �����ŵ���������ζ��˵������������ ���壬д�����ɸ���������ӷ�Ӧ����ʽ�� ��������������������������������ͬʱ������Һ����ǣ�ԭ���ǣ��������ӷ���ʽ��ʾ�������������������������������� ��
��4����������ʵ�飬��ͬѧ����������������ʵ���еķ�������������һ����ѧ����ʽ��ʾ������������������������������ ����һ��Ӧ������ʵ���������� ����ǡ�����ȷ����Ӧ��ȫ��
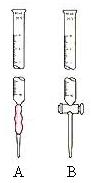 ��22����12�֣���֪��KMnO4��MnO2�����������¾��ܽ�������������MnԪ�ؾ�����ԭΪMn2����ij�о�С��Ϊ�ⶨ���̿���MnO2������������ȷ��ȡ1.20g���̿���Ʒ����һ�ձ��У�����2.68g�����ƹ��壬�ټ��������ϡ���Ტ���ȣ����ʲ��μӷ�Ӧ���Ҳ������ᣩ����ַ�Ӧ����ȴ����ȥ���ʣ���������Һȫ��ת�Ƶ�100mL����ƿ�в����ݺ��ã�ȷ��ȡ20.00mL 0.0400mol��L��1��KMnO4����Һ������ƿ�У��ٴ�����ƿ��ȡ��������Һ����һ�ྻ�Ҳ�©ˮ�ĵζ����н��еζ���������25.00mL����Һʱǡ����ȫ��Ӧ����ش��������⣺
��22����12�֣���֪��KMnO4��MnO2�����������¾��ܽ�������������MnԪ�ؾ�����ԭΪMn2����ij�о�С��Ϊ�ⶨ���̿���MnO2������������ȷ��ȡ1.20g���̿���Ʒ����һ�ձ��У�����2.68g�����ƹ��壬�ټ��������ϡ���Ტ���ȣ����ʲ��μӷ�Ӧ���Ҳ������ᣩ����ַ�Ӧ����ȴ����ȥ���ʣ���������Һȫ��ת�Ƶ�100mL����ƿ�в����ݺ��ã�ȷ��ȡ20.00mL 0.0400mol��L��1��KMnO4����Һ������ƿ�У��ٴ�����ƿ��ȡ��������Һ����һ�ྻ�Ҳ�©ˮ�ĵζ����н��еζ���������25.00mL����Һʱǡ����ȫ��Ӧ����ش��������⣺
�� д��MnO2���������Ƶ����ӷ���ʽ�������������� ���������� ��
�� ��MnO2���������ƺ����Һȫ��ת�Ƶ�100mL����ƿ�еľ���������������������������������������������� ��
�� ������ƿ��ȡ���IJ�����ҺӦ������������ѡ�A����B�����ζ����У��ζ�ǰ������еIJ������������������� ���ζ��������Ƿ���Ҫָʾ����������ѡ��ǡ��������ش��ǡ�����д��ָʾ�������ƣ����ش𡰷���д���жϵζ��յ���������������� ��
�� ���ܷ�������о�С��������̿���MnO2��������������������ѡ��ܡ��������ش��ܡ�������������������ش𡰷���˵��ԭ�������������������������� ��
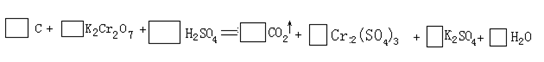
23��(4��)1932�꣬������ѧ��ʦLinus Pauling��������ԣ���ϣ����ĸ�ֱ�ʾ���ĸ��
����ȷ����������ԭ��ij����������Դ�С��Linus Pauling�ٶ�F�ĵ縺��Ϊ4����ͨ��
�Ȼ�ѧ��������������Ԫ�صĵ縺�ԡ�Linus Pauling����������Ԫ�صĵ縺�����£�
| H��2.1 | ||||||
| Li��1.0 | Be��1.5 | B��2.0 | C��2.5 | N��3.0 | O��3.5 | F��4.0 |
| Na��0.9 | Mg��1.2 | Al��1.5 | Si��1.8 | P��2.1 | S��2.5 | Cl��3.0 |
| K��0.8 | Ca��1.0 | Ga��1.6 | Ge��1.8 | As��2.0 | Se��2.4 | Br��2.8 |
| Rb��0.8 | Sr��1.0 | In��1.7 | Sn��1.8 | Sb��1.9 | Te���� | I��2.5 |
| Cs��0.7 | Ba��0.9 | Tl��1.8 | Pb��1.9 | Bi��1.9 | Po��2.0 | At��2.2 |
| Fr��0.7 | Ra��0.9 |
�ش��������⣺
��Ԥ��TeԪ�ئֵķ�Χ���������� ��
�ƴ�����ʵ������������Ԫ�صĵ縺�Բ�ֵС��1.7ʱ��������Ԫ��ͨ���γɹ��ۻ�����õ���ʽ��ʾAlBr3���γɹ������������������������������������� ��
�ģ�����⣨��52�֣�
24����11�֣����ᾧ���Ƭ״���л���У�������������������������֯�л��ͺͷ������ã��ʿ�������ҽҩ��ʳƷ�����ȷ��档�Իش��������⣺
��1������Ŀ��Ϣ��֪����Ӧ�����������ᣨ����ǿ����ǿ��
��2������ķ���ʽΪH3BO3����֪H��O�ɼ���������ӽṹʽΪ���������� ��
��3���о��������ڴ��������£�Ԫ�ص�ԭ�����γɷ��ӻ�����ʱ�����������дﵽ8�����ȶ��ṹ��������֪0.01mol������Ա�20mL 0.5mol��L -1NaOH��Һǡ����ȫ�к�,�ݴ��Ʋ�������ˮ��Һ�����Ե�ԭ���ǣ������ӷ���ʽ��ʾ����������������������������
д��������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ������������������������������������
��4������ͼ״���Ũ������ڵ������£������ɻӷ�������������д��������ȫ�����ķ���ʽ��
����������������������������������������������������������
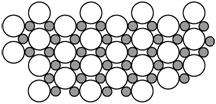 ��5����ѧ�ҷ�����þ��39 Kʱ�ʳ����ԣ�����þ���������ģ���У�þԭ�Ӻ���ԭ���Ƿֲ��Ų��ģ�һ��þһ����������У���ͼ�Ǹþ����ۿռ���ȡ���IJ���ԭ����Z�᷽���ͶӰ��������þԭ��ͶӰ����������ԭ��ͶӰ��ͼ�е���ԭ�Ӻ�þԭ��ͶӰ��ͬһƽ���ϡ�������ͼȷ����þ�Ļ�ѧʽΪ��������
��5����ѧ�ҷ�����þ��39 Kʱ�ʳ����ԣ�����þ���������ģ���У�þԭ�Ӻ���ԭ���Ƿֲ��Ų��ģ�һ��þһ����������У���ͼ�Ǹþ����ۿռ���ȡ���IJ���ԭ����Z�᷽���ͶӰ��������þԭ��ͶӰ����������ԭ��ͶӰ��ͼ�е���ԭ�Ӻ�þԭ��ͶӰ��ͬһƽ���ϡ�������ͼȷ����þ�Ļ�ѧʽΪ��������
25����10�֣��õ绡���ϳɵĴ�������̼�ܳ����д�����̼����˳�������ʣ������ֿ������������������ᴿ���䷴ӦʽΪ��
�������ƽ������Ӧ�Ļ�ѧ����ʽ��
�ƴ˷�Ӧ�������������������� ����������ĵ���ʽ������������ ��
��H2SO4��������Ӧ�б��ֳ������������������� ����ѡ���ţ�����ѡ���۷֣�
A���ԡ�������B�����ԡ������������� C��ˮ�ԡ��������� D��ˮ��
��������Ӧ��������0.2molCO2���壬��ת�Ƶ��ӵ����ʵ������������� mol.
��26.(9��)��2molSO2��1molO2�����������ɱ䣬ѹǿ�㶨���ܱ������У���һ���¶��·������·�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)����H��0,����Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1 mol���Իش��������⣺
2SO3(g)����H��0,����Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1 mol���Իش��������⣺
�ŷ�Ӧ���е�t1ʱ��SO2���������Ϊ������ ��
 ������t1ʱ����һ�����������Ar��,SO2�����ʵ���������
������__________�����������С�����䡱����
������t1ʱ����һ�����������Ar��,SO2�����ʵ���������
������__________�����������С�����䡱����
������t1ʱ���£����´ﵽƽ��״̬����ƽ������������������ʵ������� 2.1mol���<������>����=����������˵��ԭ�� ________________________________________________________________________������
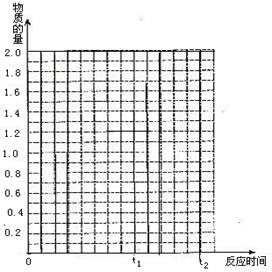
���������������䣬��t1ʱ�ټ���0.2molSO3��0.1molO2����1.8molSO3����ͼ����A��t0��t1��t2�����ʱ����SO2�����ʵ����仯���ߡ�
27����12�֣���ѧ�Ҵӻ��ʳ�������![]() �м�����Ϊ
�м�����Ϊ![]() �����ʣ����ⶨ��������������ˮ����ˮ����
�����ʣ����ⶨ��������������ˮ����ˮ����![]() ��
��![]() ����������ʽ���ڣ�ֲ��ĸ�ϵ��������
����������ʽ���ڣ�ֲ��ĸ�ϵ��������![]() ������������ʱ��������һ�����ư���N4���ӣ�N4���Ӳ��ܱ�ֲ�����ա�
������������ʱ��������һ�����ư���N4���ӣ�N4���Ӳ��ܱ�ֲ�����ա�
��ش��������⣺
��1��N4��N2�Ĺ�ϵ��ȷ�������������������� ������ţ�
A. ͬ�ֵ��ʡ�������B. ͬλ�ء����������� C. ͬ���칹�塡���������� D. ͬ��������
��2��![]() ����������������
����ܡ����ܡ����Ͳ�ľ�һ��ʩ�ã�
����������������
����ܡ����ܡ����Ͳ�ľ�һ��ʩ�ã�
��3����֪���ס�![]() �Ŀռ乹�;�Ϊ�����壬
�Ŀռ乹�;�Ϊ�����壬![]() �ĽṹʽΪ
�ĽṹʽΪ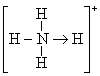 ��
��![]() ��ʾ���õ��Ӷ���Nԭ�ӵ������ṩ�������ף�P4���ĽṹʽΪ
��ʾ���õ��Ӷ���Nԭ�ӵ������ṩ�������ף�P4���ĽṹʽΪ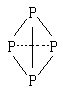 ���뻭��
���뻭��![]() �Ľṹʽ������������������
��������������
�Ľṹʽ������������������
��������������
��4����֪Һ���д�����ƽ��![]() ����ѧ����Һ���м���������藍�CsOH�����������ˮ����ʹҺ���е�
����ѧ����Һ���м���������藍�CsOH�����������ˮ����ʹҺ���е�![]() ����N4���ӣ���д��Һ����������路�Ӧ�Ļ�ѧ����ʽ��������������������
������������������ ��
����N4���ӣ���д��Һ����������路�Ӧ�Ļ�ѧ����ʽ��������������������
������������������ ��
��5������һ����![]() ��NH3��H2O��ˮ��Һ��Ϊ��������Һ�����ڴ���Һ�м���������ǿ���ǿ��ʱ����Һ��pH�������䣬������������ӷ���ʽ��˵����
��NH3��H2O��ˮ��Һ��Ϊ��������Һ�����ڴ���Һ�м���������ǿ���ǿ��ʱ����Һ��pH�������䣬������������ӷ���ʽ��˵����
����ʱ��![]()
�Ӽ�ʱ��![]()
����![]() ��
��![]() �Ĵ������ڣ�����������ʱ����Һ��C(H+)��C(OH��)�������ֲ��䣻
�Ĵ������ڣ�����������ʱ����Һ��C(H+)��C(OH��)�������ֲ��䣻
����һ����![]() ��
��![]() ����Һ��Ҳ���л������ã�д������Һ�м�������ǿ���ǿ��ʱ���������ӷ�Ӧ����ʽ��
����Һ��Ҳ���л������ã�д������Һ�м�������ǿ���ǿ��ʱ���������ӷ�Ӧ����ʽ��
����ʱ����������������������������������������
�Ӽ�ʱ���������������������������� �������� ��
28����10�֣�t��ʱ����3molA��2molB����ͨ�����Ϊ2L���ܱ�������(�ݻ�����)���������·�Ӧ��3A(��)+B(��) ![]() xC(��)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��ΪO.4mol/L������д���пհף�
xC(��)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��ΪO.4mol/L������д���пհף�
(1)x=__________��
(2)�Ƚϴﵽƽ��ʱ��A��B����Ӧ���ת����֮��Ϊ��(A)����(B)������������ ��
(3)��������ԭƽ�������������ͨ����������(������A��B��C������Ӧ)������˵������ȷ����____________(��д��ĸ���)
������A����ѧƽ��������Ӧ�����ƶ����� B����ѧƽ�����淴Ӧ�����ƶ�
������C����ѧƽ�ⲻ�ᷢ���ƶ��������� D�������淴Ӧ�Ļ�ѧ��Ӧ���ʱ��ֲ���
(4)��t��ʱ������ԭƽ��������������ٳ���amolC����ʹ�ﵽ�µ�ƽ��ʱ�������ʵ����ʵ���������ԭƽ����ͬ��������Ӧ�ٳ���____��______(��A��B)________mol(��a��ʾ)��
��������������������������������������ѧרҵ��3����
�������������������������������������ˣ�ʷ�����������������ڣ�2006.10.18
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | C | B | B | C | D | B | A | D | C |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| AD | B | AB | C | AC | D | CD | D | C | BD |
|
��4��4Na2SO3==== 3Na2SO4��Na2S
22����12�֣��š� MnO2��C2O42����4H����Mn2����2CO2����2H2O ��2�֣�
�ơ� ���ձ��е���Һ�ز�������������ƿ�У�������������ˮϴ���ձ�2��3�Σ�ϴ��Һ���ز�������������ƿ�С� ��2�֣�
�ǡ� B����ȷ��������¼�������������������һ�δ���Һʱ����ƿ�е���Һ�ɺ�ɫ��Ϊ��ɫ���ڰ�����ڲ����Ժ�ɫ�� ��ÿ��1�֣�
�ȡ� �ܡ���87.0��������ÿ��1�֣�
23����4�֣�
��2.0���֣�2.4��������������
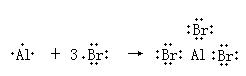
�ơ����������������� ����д��˫�۷�����ʽ��
24����11�֣���1���� (1�֣�
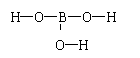 ��2������������������������������
(2�֣�
��2������������������������������
(2�֣�
��3��B(OH)3+H2O![]() [B(OH)4]��+H+�� (2�֣�
[B(OH)4]��+H+�� (2�֣�
����B(OH)3+NaOH=NaBO2+2H2O������(2�֣�
��4��B(OH)3+3CH3OH![]()
![]() B(OCH3)3+3H2O��(2�֣�
B(OCH3)3+3H2O��(2�֣�
��5��MgB2��(2�֣�
25����10�֣���1��3��2��8��3��2��2��8H2O ��2�֣������� ��2��K2Cr2O7��2�֣�
![]() ��
��
��������2�֣�����������3��A��2�֣�����������4��0.8mol��2�֣�
26����9�֣���1��9.5%��3�֣�������2������1�֣� ����3������1�֣��������¶ȷ�Ӧ�����ȷ�Ӧ������У�����ѧƽ�����淴Ӧ�����ƶ�������������ʵ�������2�֣���
������4����ͼ�ԣ���2�֣���ע�⣺t0��t1ʱֻҪ��������꣨0��2�� ��ƽ��������꣨t1��0.2������ʾ��ͼ�����֣�t1��t2 ��ƽ����ʱ�����ֱ�ߣ��������ڣ�t1��0.4��
27����12�֣���1��D��2�֣����������� ��2�����ܣ�2�֣�
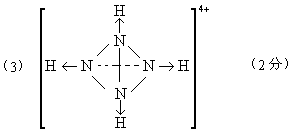
��4��![]() ��2�֣�
��2�֣�
��5��![]() ��2�֣�
��2�֣�
���� ![]() ��2�֣�
��2�֣�
28����ÿ��2�֣���10�֣�
��1�� x=4������ ��2����2:1 ������3��C��D���� ����4����B���� a/4 ��