高三化学上册第三次月考试卷
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5 K:39 Fe:56 Cu:64 Zn:65 Br:80 Ag:108 I:127
第I卷:选择题(共50分)
一、选择题:(以下每题只有1个选项符合题意,2′×10)
1.最近,医学家们通过放射性14C标记的C60发现: 一种C60羧酸衍生物在特定条件下可通过断裂DNA杀死细菌,从而控制爱滋病毒.下列有关14C的说法正确的是
A. 与14N所含中子数相同
B. 与C60均为碳的同素异形体
C. 与12C互为同位素
D. 质量数为14,原子序数为6,核内有8个质子
2.在下列各说法中,正确的是
A.△H > 0 kJ・mol-1表示放热反应,△H < 0 kJ・mol-1表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 molBa(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热
3.下列有关说法中,错误的是
A.NH4H是一种离子晶体,其中氢离子的核外电子排布与氦原子相同
B.在石墨晶体中,碳原子与共价键的个数比为2:3
![]() C.三种氢化物的沸点高低:HBr>HCl>HF
C.三种氢化物的沸点高低:HBr>HCl>HF
D.甲基的电子式为
4.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有
A.滴加石蕊试液显红色的溶液
Fe3+ 、NH![]() 、Cl- 、SCN-
、Cl- 、SCN-
B.pH值为1的溶液
Na+ 、Mg2+
、Cl-、NO![]()
C.水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO![]() 、Br-、Ba2+
、Br-、Ba2+
D.所含溶质为Na2SO4的溶液
K+ 、CO32-、NO![]() 、Al3+
、Al3+
5.在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末a g,反应后温度恢复到25℃,下列有关该溶液的说法正确的是
A.溶液中c (Ba2+ ) 将增大 B.溶液的pH将增大
C.溶液中Ba2+ 总数将减少 D.溶液中c (OH― ) 减小
6.设NA表示阿伏加德罗常数,下列说法中不正确的是
A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
B.标准状况下的22.4L辛烷完全燃烧,生成的二氧化碳的分子数目一定为8NA
C.0.01molMg在空气中完全燃烧,生成MgO和Mg3N2,转移电子数目为0.02 NA
D.125gCuSO4・5H2O晶体中含有0.5 NA个Cu2+
7.下列事实,不能用勒夏特列原理解释的是
A.对2HI(g) ![]() H2(g) + I2(g) ,平衡体系增大压强可使颜色变深
H2(g) + I2(g) ,平衡体系增大压强可使颜色变深
B.溴水中有下列平衡Br2 + H2O
![]() HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
C.反应CO + NO2![]() CO2 + NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2 + NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.工业制硫酸的反应中,为提高二氧化硫的转化率,理论上应采取降低温度的措施
8.下列4组溶液,不用试剂也能鉴别开来的是
① AgNO3溶液、稀氨水 ② NaAlO2溶液和盐酸
③ NaHCO3、NaHSO4、Ba(NO3)2、NH4Cl ④ NaNO3、FeCl3、NaCl、AgNO3
A.只有① B.①② C.①②③ D.全部
9.某学生欲完成2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的实验是
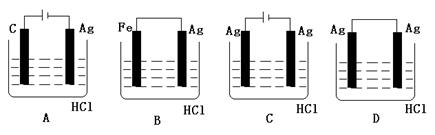
10.某溶液中含有CH3COO-、SO42-、SO32-、HCO3-、CO32-等五种离子。将过量的Na2O2固体加入其中后,仍能大量存在的离子是
A.CH3COO-、SO42-、CO32- B.SO42-、SO32-、CO32-
C.SO32-、HCO3- D.CH3COO-、SO42-、HCO3-
二、选择题:(每小题有1―2个选项符合题意,少选得1分。2′×15)
11.有X、Y、Z、M四种金属,已知:X可以从Y的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子氧化性强于Y的离子。则这四种金属的活动性由强到弱的顺序是
A.X>Y>Z>M B.X>Z>M>Y C.M>Z>X>Y D.X>Z>Y>M
12.在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
|
C.Mg3N2 + 6H2O=3Mg(OH)2↓+2NH3↑ D.NH4Cl +NaOH === NaCl + H2O + NH3 ↑
13.A、B、C、D、E五种短周期元素。A、B、C位于同一周期相邻位置,A和C的原子序数之比为3∶4,A、B、C分别与D形成的化合物分子中都含有10个电子。E的原子结构示意图中从内到外各层的电子数之比为1∶4∶1。则下列叙述中正确的是
A.A和C形成的某种化合物能与E的单质在一定条件下发生置换反应
B.实验室制备B、D两种元素形成的化合物发生的反应属于氧化还原反应
C.由A、C原子和B、D原子分别构成的分子都是极性分子
D.由A、B、C、D四种元素组成的化合物中不可能含有离子键
14.在一定条件下,硫酸铵的分解反应为:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O当有n mol电子转移时,下列说法不正确的是
A.有2n mol (NH4)2SO4分解 B.有![]() 原子被还原
原子被还原
C.生成![]() 氧化产物 D.生成7n mol H2O
氧化产物 D.生成7n mol H2O
15.下列说法可以实现的是:①酸性氧化物均能与碱发生反应;②盐溶液与弱酸反应可以生成强酸;③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成;④两种酸溶液充分反应后,所得溶液呈中性;⑤有单质参加反应,但该反应不是氧化还原反应
A.②③④⑤ B.①③④⑤ C.①②③⑤ D.①②③④⑤
16.下列离子方程式中不正确的是
A.向Ba(OH)2溶液中逐滴加入H2SO4溶液至刚好沉淀完全:
Ba2++OH-+H++SO![]() =BaSO4↓+H2O
=BaSO4↓+H2O
B.用Pt电极电解MgCl2溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.碳酸氢钠溶液与硫酸氢钠溶液反应:HCO![]() +H+=CO2↑+H2O
+H+=CO2↑+H2O
 D.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
D.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
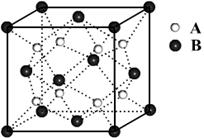
17.某离子晶体的晶体结构中最小重复单元如右图所示:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
A.B2A B.BA2
C.B7A4 D.B4A7
18.容积相同的甲、乙密闭容器,甲为恒容、乙为恒压,分别充入
2 molSO2和1 mol
O2,同时发生反应: 2SO2(g)+O2(g)![]() 2SO3(g),同温度下分别达到平衡,测得甲中SO2的转化率为25%,下列说法中正确的是
2SO3(g),同温度下分别达到平衡,测得甲中SO2的转化率为25%,下列说法中正确的是
A.反应过程中甲容器中的反应速率比乙中的大
B.甲容器反应达到平衡时所需时间比乙容器少
C.乙容器中SO2的转化率大于25%
D.平衡时,乙容器中SO2、O2、SO3的浓度之比一定为2:1:2
19.按如图甲装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是
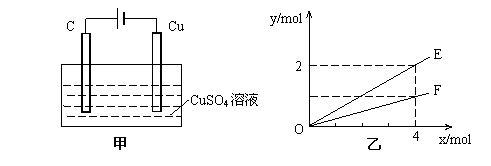

A.E表示生成铜的物质的量 B.E表示反应消耗水的物质的量
C.F表示反应生成氧气的物质的量 D.F表示生成硫酸的物质的量
20.无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
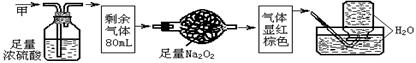
A.NH3、NO2、N2 B.NH3、NO、CO2 C.NH3、NO2、CO2 D.NO、CO2、N2
21.在铜的催化作用下氨气与氟气反应,得到一种三角锥形分子M和一种铵盐N。下列有关说法不正确的是
A.该反应的化学方程式为:4NH3 + 3F2 = NF3 + 3NH4F
B.M是极性分子,其还原性比NH3强
C.M既是氧化产物,又是还原产物
D.4moNH3参加反应失去12mol电子
22.已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl。在标准状况下,向100mLFeCl3溶液中通入a L的H2S气体后,再加入足量的铁粉充分反应。所得溶液经测定金属阳离子的浓度为3mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为
A.1.5mol/L B.1 mol/L C.2 mol/L D.无法确定
23.下列叙述正确的是
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.相同物质的量浓度,相同体积的强酸与强碱溶液混合,反应后pH=7
C.原子失去电子所形成的离子,不一定具有稀有气体原子的电子层结构
D.某元素在化学变化中由化合态变为游离态,不能确定该元素一定被还原
24.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH。则电解过程中转移的电子数为
A.0.1mol B.0.2mol C.0.3mol D.0.4mol
25.下列说法正确的是
A.某二元弱酸的酸式盐NaHA溶液中: c(H+)+c(A2-)=c(OH-)十c(H2A)
B.0.020 mol/L的HCN(aq)与0.020 mol/L NaCN(aq)等体积混合得到碱性混合溶液中:
c(Na+)> c(CN-)
C.在物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的混合溶液中:
c(CH3COOH)+c(CH3COO-)=0.01 mol/L
D.c(NH4+)相等的(NH4)2SO4溶液、NH4HCO3溶液、NH4Cl溶液:
c[(NH4)2SO4] > c(NH4HCO3) > c(NH4Cl)
第Ⅱ 卷:非选择题(共58分)
三、填空题:本大题共6小题,共50分。
26.(6分)在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,有关反应的离子方程式是_________________________ ;在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失,有关反应的离子方程式是______________________ __ 。从以上事实可知,ClO-、I2、SO42-的氧化性由弱到强的顺序是_____________________________。
27.(8分)A、B、C、D均为4种常见的短周期元素,常温下A、B可形成两种常见的液态化合物,其最简式分别为BA和B2A;B与D可形成分子X,也可形成阳离子Y,X、Y在水溶液中酸、碱性正好相反;C+的焰色反应呈黄色。
⑴C元素在周期表中的位置是 ;液态X类似B2A,也能微弱电离且产生电子数相同的两种离子,则液态X电离方程式为 。
⑵M、N是由A、B、C、D四种元素中任意三种元素组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且M溶液中水的电离程度小于N溶液中水的电离程度。 则M、N分别为(填化学式) ;若将0.1mol・L-1M和0.2mol・L-1N两溶液等体积混合所得溶液中离子浓度的大小顺序为 。
28.(12分) CO不仅是家用煤气的主要成分,也是重要的化工原料。美国近年来报导了一种低温低压催化工艺,把某些简单的有机物经“羰化”反应后可以最后产生一类具有优良性能的装饰性高分子涂料、粘合剂等。如下图所示:
CO不仅是家用煤气的主要成分,也是重要的化工原料。美国近年来报导了一种低温低压催化工艺,把某些简单的有机物经“羰化”反应后可以最后产生一类具有优良性能的装饰性高分子涂料、粘合剂等。如下图所示:
 |
图中G(RCOOR,)的一种同分异构体是E的相邻同系物;而H的一种同分异构体则是F的相邻同系物。已知D由CO和H2按物质的量之比为1∶2完全反应而成,其氧化产物可发生银镜反应;H是含有4个碳原子的化合物。试写出:
(1)结构简式:E 、G 、R,基 。
(2)G的两个同类别同分异构体的结构简式(不带R字母) 。
(3)反应类型:X 、Y 、Z 。
![]()
![]() (4)写出下列转化的化学方程式:
(4)写出下列转化的化学方程式:
① A+CO+H2O E;②F+D H。
① ;
② 。
29.(6分)甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银四种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面的问题:
(1)这几种溶液分别是甲: ,丙: 。
(2)写出乙与丁反应的离子方程式: 。
30.(12分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
|
肼―空气燃料电池放电时:
正极的电极反应式是 。
负极的电极反应式是 。
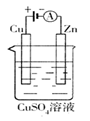
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应是 。(写电极反应式)
②假设使用肼―空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池
理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
31.(6分)工业上制硫酸的设备分为三大部分,一是沸腾炉、二是接触室、三是吸收塔。在沸腾炉内煅烧黄铁矿生成二氧化硫;在接触室内有催化剂存在下二氧化硫进一步与氧气结合,生成三氧化硫;三氧化硫流经吸收塔时,采用98.3%的浓硫酸吸收,使三氧化硫最终与水化合形成硫酸。
下面的装置是仿照工业上制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98.3%的浓硫酸吸收三氧化硫。
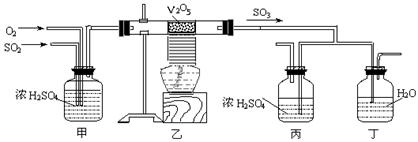
请回答下列问题:
(1) 写出沸腾炉内煅烧黄铁矿的反应方程式:______________________________ _ ____;
(2) 上图中的乙、丙分别相当于工业上制取硫酸装置中的__________________________ __;
(3) 处理尾气的方法是_____________________________ _。
四、计算题:本题包括1小题,8分。
32.为测定某氧化物(化学式为M2O)中M是何种金属,做以下实验:称取该氧化物
23.2 g溶于适量的稀硝酸中,再配成250mL溶液。取该溶液50mL用惰性电极进行电解,当刚好电解完全时,电极上析出M4.32g。请通过计算回答以下问题:(写出解题过程)
(1)M是什么金属?
(2)电解过程中,导线上流过的电子个数是多少?
(3)最初配成的溶液中,该金属离子的物质的量浓度是多少?
(4)若此电解液在电解后体积为40mL,此时溶液的pH是多少?
化学答题纸 成绩
三、填空题:本大题共6小题,共50分。
26.(6分)离子方程式是_________________________ ;离子方程式是______________________ 。氧化性由弱到强的顺序是_________________________ ____。
27.(8分)
⑴位置是 ;电离方程式为 。
⑵ 则M、N分别为(填化学式) ;
离子浓度的大小顺序为 。
28.(12分)
(1)结构简式:E 、G 、R,基 。
(2)两个结构简式(不带R字母) 。
(3)反应类型:X 、Y 、Z 。
(4)① ;
② 。
29.(6分) (1)甲: ,丙: 。
(2)离子方程式: 。
30.(12分)(1)热化学方程式是 。
(2)正极的电极反应式是 。
负极的电极反应式是 。
(3) ①锌片上发生的电极反应是 。
②空气 L。
(4)离子方程式是 。
31.(6分)
(1) 反应方程式:______________________________ _____;
(2) 乙、丙分别相当于工业上制取硫酸装置中的____________________ ________;
(3) 处理尾气的方法是_____________________ ________ _。
四、计算题:本题包括1小题,8分。
32.
(1)M是 。
(2)电解过程中,导线上流过的电子个数是 。
(3)最初配成的溶液中,该金属离子的物质的量浓度是 。
(4)若此电解液在电解后体积为40mL,此时溶液的pH是 。
请写出解题过程:
试卷参考答案
一、二选择题:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | C | B | C | B | C | B | A | D | C | A | D | A | A |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 | AD | D | AB | B | C | D | B | BD | C | CD | D | B |
三、填空题:本大题共6小题,共50分。
26.(6分,每空2分)
ClO-+2I-+2H+=I2+Cl-+H2O;
SO32-+I2+H2O=SO42-+2H++2I-; SO42-<I2<ClO-
27.(8分)⑴第3周期第IA族 ⑵2NH3![]() NH4++NH2- ⑶NaOH和NH4NO3
NH4++NH2- ⑶NaOH和NH4NO3
c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) ……………………………………(每空2分)
28.(共12分)
(1)E:CH2=CHCOOH;G:CH2=CHCOOCH3;R,基:―CH3。 (各1分 共3分)
(2)HCOOCH2CH=CH2;CH3COOCH=CH2。 (各1分 共2分)
![]() (3)X:加成反应;Y:消去反应;Z:加聚反应。
(各1分 共3分)
(3)X:加成反应;Y:消去反应;Z:加聚反应。
(各1分 共3分)
(4)①HC≡CH + CO + H2 H2C=CHCOOH (各2分 共4分)
![]() ②C H3CH2COOH
+ CH3OH
CH3CH2COOCH3 +H2O
②C H3CH2COOH
+ CH3OH
CH3CH2COOCH3 +H2O
29.(6分,每空2分)(1)CaCl2 AgNO3
(2)CO32―+2H+=CO2↑+H2O
30.(共12分,每空2分)
(1)N2H4(1)+O2(g)=N2(g)+2H2O(1);△H=-624kJ/mol
(2)O2+2H2O+4e-=4OH-
N2H4+4OH--4e-=4H2O+N2↑
(3)①Cu2++2e-=Cu ②112
(4)ClO-+2NH3=N2H4+Cl-+H2O
31.(6分,每空2分)(1)![]()
(2)乙(接触室),丙(吸收塔)
(3)用碱液吸收。
四、计算题:本题包括1小题,8分。
32.(8分,每问2分)(1)Ag或银 (2)![]() (3)
(3)![]() (4)0
(4)0