高三化学一轮复习综合模拟题三
1.下列不符合当今化学研究方向的是
A.发现新物质 B.合成新材料
C.研究化学反应的微观过程 D.研究化学反应中原子守恒关系
2.ClO2 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:![]() ;下列说法正确的是
;下列说法正确的是
A.KClO3在反应中得到电子 B.ClO2 是氧化产物
C.H2C2O4在反应中被还原 D.1 mol KClO3 参加反应有 2 mol 电子转移
3.下列实验操作正确的是
A.粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
B.容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水
C.不慎将浓苛性钠溶液沾到皮肤上,立即用H2SO4 中和并洗涤
D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
4.右图中a、b、c、d、e为周期表前4周期的一部分,下列叙述正确的是
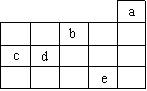
A.b元素除0价外,只有一种化合价
B.五种元素中,c元素形成的单质性质最稳定
C.c、d元素最高价氧化物的水化物酸性:c > d
D.e元素在自然界中主要存在于海水中
5.下列实验方案中,不可行的是
A.用加入足量铜粉的方法除去Cu(NO3) 2 溶液中混有的AgNO3
B.用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体
C.加入NaOH溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.先后添加石蕊试液、BaCl2 溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和碳酸钾五种无色溶液鉴别开
6.以NA表示阿佛加德罗常数,下列说法正确的是
A.乙烯、丙烯的混合物1.4 g中含有0.1 NA个碳原子
B.用电解法精炼铜时转移0.1 NA电子时阳极溶解6.4 g铜
C.13.6 g熔融的KHSO4 中含有0.2 NA个阳离子
D.标准状况下,11.2 L水中含0.5 NA个氧原子
7 .由Na2O2、Na2CO3、NaHCO3、NaCl中某几种组成的混合物,向其中加入足量的盐酸有气体放出。将气体通过足量的NaOH溶液,气体体积减少。将上述混合物在空气中加热,有气体放出。下列判断正确的是
A.混合物中一定不含Na2CO3、NaCl B.混合物中一定有Na2O2、NaHCO3
C.无法确定混合物中是否含有NaHCO3 D.混合物中一定不含Na2O2、NaCl
8.SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L,下列措施中能够减少SO2排放量的是 ①用天然气代替煤炭做民用燃料 ②使用水煤气或干馏煤气做燃料 ③硫酸厂使用V2O5作催化剂,加快SO2的转化速率 ④将块状煤粉碎,提高其燃烧效率 ⑤在煤中加入石灰后燃用 ⑥循环处理吸收塔放出的尾气
A.①②③④⑤ B.①③⑤⑥ C.①②⑤⑥ D.②③④⑥
![]() 9.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
9.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
A.N4属于一种新型的化合物 B.N4与N2互为同素异形体
C.N4沸点比P4(白磷)高 D.1mo1N4气体转变为N2将吸收882kJ热量
10.下列物质能通过化合反应直接制得的是
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl
A.只有①②③ B.只有②③ C. 只有①③④ D.全部
11.下列说法正确的是
A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子型化合物
12.在加入铝粉能放出H2的溶液中,可能大量共存的是
A.NH4+、NO3-、CO32-、Na+ B.Na+、Ba2+、Mg2+、HCO3-
C.NO3-、K+、SO42-、Cl- D.NO3-、Na+、Fe2+、K+
13.某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是
①有晶体析出 ②c[Ca(OH)2]增大 ③pH不变 ④c(H+)c(OH-)的积不变 ⑤c(H+)一定增大
A ① B ①③ C ①②④ D ①⑤
14.干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量。某些干燥剂的干燥效率数据如下:
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
分析以上数据,下列有关叙述错误的是
A.MgO的干燥性能比CaO好
B.干燥效率可能与干燥剂的阴、阳离子的半径大小有关
C.MgCl2可能是比CaCl2更好的干燥剂
D.上述干燥剂中阳离子对干燥性能的影响比阴离子小
15.教材是学习的重要材料,但不能迷信教材。下列是中学化学教材中摘录的部分表述内容,根据你所学的化学知识判断,其中不够科学严密的是
A.除了加入电解质可使某些胶体聚沉外,将两种带相反电荷的胶体混合,也能发生聚沉。
B.离子方程式不仅可以表示一定物质间的某个反应,而且可以表示所有同一类型的离子反应。
C.元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果。
D.不同的化学反应,具有不同的反应速率,这说明,参加反应的物质的性质是决定化学反应速率的重要因素。
16. (5分)铝及其化合物在生活中有着广泛应用。在我国南方某些地区,当地居民常采用往水中加明矾的方法来处理水中的悬浮杂质。其原理为
。明矾处理后的水中含有较多的阴离子为 ;写出用化学方法验证水中含有这种阴离子的操作和现象:
。
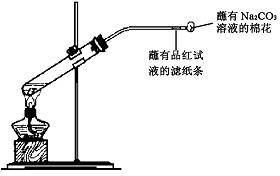 17.(7分)①某同学用下图所示装置制备SO2
并验证其性质,试管内有一小片铜片和浓硫酸,试管内发生反应的化学方程式为
;导管中品红试纸的作用是
;导管口蘸有碳酸钠溶液的棉花的作用是
;相关的化学方程式是
。
17.(7分)①某同学用下图所示装置制备SO2
并验证其性质,试管内有一小片铜片和浓硫酸,试管内发生反应的化学方程式为
;导管中品红试纸的作用是
;导管口蘸有碳酸钠溶液的棉花的作用是
;相关的化学方程式是
。
②实验室中现有下列实验用品:氢硫酸、NaOH溶液、KMnO4溶液、脱脂棉、镊子、pH试纸、玻璃棒请设计实验验证SO2的还原性,简述实验操作步骤和现象
。
18.(8分)根据溴的性质,填写下列表格中关于液溴保存方法的选择及有关原因的解释: ①广口瓶②细口瓶③玻璃塞④橡皮塞⑤水封⑥煤油封⑦棕色瓶⑧无色瓶
| 选择保存方法 | 解释 | |
| (1) | ||
| (2) | ||
| (3) | ||
| (4) |
19.A是一种无色透明的晶体,进行如下实验:
①取少量A晶体做焰色反应实验,透过蓝色钴玻璃观察,火焰呈紫色。
②取少量A晶体溶于水可以得到无色的溶液,该溶液使石蕊变红。
③取少量A的溶液加过量氨水,有白色沉淀B生成。
④过滤除去③中的B后,再在滤液中滴加氯化钡溶液,有白色沉淀C生成,C不溶于稀硝酸。
⑤取少量B滴加氢氧化钠溶液,得无色溶液D。
⑥取少量B滴加盐酸,得无色溶液E。
⑦将47.4gA晶体在120℃下加热脱水,剩余物的质量为25.8g。
根据上述实验现象和结果确定A、B、C、D、E,写出它们的化学式。
A ______ __;B____ ____;C___ _____;D_____ ___;E_______ _。
答案:1、D 2、A 3、D 4、D 5、B 6、A 7、B 8、C
9、B 10、D 11、D 12、C 13、D 14、D 15、A
16.(5分)明矾溶于水电离出来的铝离子水解生成氢氧化铝胶体(1分);吸附水中的悬浮物而使水得到净化(1分);SO42-(1分);取适量净化后的水加入试管中,先向试管中滴加少量盐酸,再加入BaCl2溶液(1分),若产生白色沉淀,则说明净化后的水中含有SO42-(1分);
17.(共11分)(8分)①Cu + 2H2SO4(浓)![]() CuSO4+SO2↑+ 2H2O;(2分)
CuSO4+SO2↑+ 2H2O;(2分)
验证SO2的漂白性(1分); 吸收多余的SO2防止污染大气(1分);
SO2+Na2CO3 = Na2SO3 + CO2 (2分);
②用镊子夹取脱脂棉蘸取KMnO4溶液,然后将棉团代替碳酸钠溶液的棉团(1分),过一段时间观察棉团紫色消失或变浅,则证明SO2具有还原性(1分)。
18、.(8分)
| 选择保存方法 | 解释 | |
| (1) | ② | 液体药品存放在细口瓶中,便于倾倒液体 |
| (2) | ③ | 液溴能腐蚀橡皮塞,不能腐蚀玻璃塞 |
| (3) | ⑤ | 液溴溶解于煤油,在水中的溶解度小,密度大于水,用水封将减少溴的挥发 |
| (4) | ⑦ | 水封后上层溴水中的HBrO见光分解. |
19、
[答案]A是KAl(SO4)2·12H2O;B为Al(OH)3;C为BaSO4;D为NaAlO2;E为AlCl3。
[解析]分析①可知,A晶体中含有钾离子。分析②可知,A晶体溶于水后显酸性,可判断A溶于水可电离出H+或A中含有易水解的阳离子。分析③、⑤、⑥可知,A晶体中可能含有Al3+。分析④可知,A晶体中含有SO42-。综合以上各个分析结果可得出A可能是明矾等。再根据⑦中的数据进行计算后可确证A是KAl(SO4)2·12H2O。
[方法指点]这类试题中往往有多条信息,需要解题者对每条信息一一进行分析,再把分析所得的结论进行综合,才能得出判断的结论。解题过程中,还常常边分析边综合。有的考生能顺利对单个信息进行分析判断,但对多信息的分析判断能力较差。高考复习训练中要重视培养分析处理多条信息作出判断的能力。