普通高等学校招生全国统一化学考试2
(江苏卷)
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1.我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的23He。每百吨23He核聚变所释放的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以24He的形式存在。下列说法正确的是
A. 24He原子核内含有4个质子
B. 3He和24He互为同位素
C.23He 原子核内含有3个中子
D.24He的最外层电子数为2,所以24He具有较强的金属性
2.下列各项中表达正确的是
A.F-的结构示意图: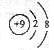 B.CO2的分子模型示意图:
B.CO2的分子模型示意图:![]()
C.NaCl的电子式:![]() D.N2的结构简式:
D.N2的结构简式:![]()
3.2004年4月22日是第35个“世界地球日”,我国确定的主题是“善待地球――科学发展”。下列行为不符合这一主题的是
A.采用“绿色化学” 工艺,使原料尽可能转化为所需要的物质
B.大量开采地下水,以满足社会对水的需要
C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D.节约能源,提高能源利用率
4.下列关于浓硫酸叙述正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
5.向一种溶液中滴加另一种溶液后,溶液的颜色不发生变化的是
A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液
C.碘水中滴加淀粉碘化钾溶液 D.高锰酸钾酸性溶液中滴加亚硫酸钠溶液
6.X、Y是元素周期表ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C. X的气态氢化物比Y的气态氢化物稳定
D.Y的单质能将X从NaX的溶液中置换出来
7.下列实验操作正确的是
A.将氢氧化钠固体放在滤纸上称量
B.用10 mL量筒量取8.58 mL蒸馏水
C.制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D.配制氯化铁溶液时,将一定量的氯化铁溶解在较浓的盐酸中,再用水稀释到所需浓度
8.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应时消耗的HCl和NaOH物质的量之比为
A.1:1 B.2:1 C.3:1 D.1:3
二、选择题(本包括10小题,第9~16题每小题4分,第17、18题每小题5分,共42分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,俣只要选错一个该小题就为0分)
9.下列分离或提纯物质的方法错误的是
A.用渗析的方法精制氢氧化铁胶体
B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
D.用盐析的方法分离、提纯蛋白质
10.用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好完全中和时,消耗盐酸和醋酸溶液的体积分别为V1和V2,则V1和V2的关系正确的是
A.V1>V2 B.V1<V2 C.V1=V2 D.V1≤V2
11.阿伏加德罗常数为6.02×1023 mol-1。下列叙述中正确的是
A.标准状况下,2.24 L苯中约含有3.612×1023 个碳原子
B.常温常压下,氧气和臭氧的混合物16 g中约含有6.02×1023个氧原子
C.25℃时,1 L pH=13的氢氧化钠溶液中约含有6.02×1023个氢氧根离子
D.0.5 mol CH4中约含有3.01×1024个电子
12.已知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量共存的离子组是
A.Al3+、CH3COO-、Cl- B.Mg2+、Ba2+、Br-
C.Mg2+、Cl-、I- D.Na+、NH4+、Cl-
13.下列反应的离子方程式书写正确的是
A.硫酸铝溶液加入过量的氨水 Al3++3OH-===Al(OH)3↓
B.电解饱和食盐水
2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.碳酸钙与盐酸反应 CaCO3+2H+===Ca2++CO2↑+H2O
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2===Fe3++2H2O
14.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O
2ClO2↑+K2SO4+2CO2↑+2H2O
下列说法正确的是
A.KClO3在反应中得到电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.1 mol KClO3参加反应有2 mol电子转移
15.有4种有机物: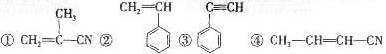 ,其中可用于合成结构简式为
,其中可用于合成结构简式为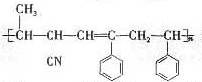 的高分子材料的正确组合为
的高分子材料的正确组合为
A.①③④ B.①②③ C.①②④ D.②③④
16.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌―锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-===Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g
17.草酸是二元弱酸草酸氢钾溶液呈酸性。在0.1 mol・L-1KHC2O4溶液中,下列关系正确的是
A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)=0.1 mol・L-1
C.c(C2O42-)>c(H2C2O4)
D.c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
18.在容积固体的密闭容器中,存在如下反应:A(g)+3B(g)![]() 2C(g);△H<0
2C(g);△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
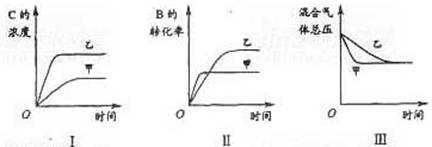
下列判断一定错误的是
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
第二卷(非选择题,共76分)
三、(本小题包括2小题,共22分)
19.请按要求填空
(1)用已准确称量的1.06 g Na2CO3固体配制0.100 mol・L‑1 Na2CO3溶液100 mL,所需要的仪器为: 。
(2)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为: 、蒸发、结晶、 。
(3)除去KCl溶液中的SO42-离子,依次加入的溶液为(填溶质的化学式): 。
20.有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
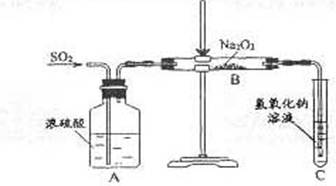
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成Na2SO3和O2,该反应的化学方程式是:
。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。
。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。
为检验是否有Na2SO4生成,他们设计了如下方案:
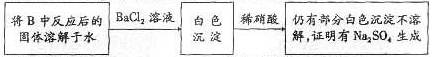
上述方案是否合理? ,请简要说明两点理由:
① ,② 。
四、(本题包括2小题,共18分)
21.下图中,A是一种无色液体,G是极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。
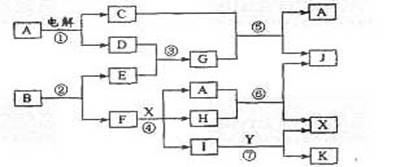
请按要求填空:
(1)写出下列物质的化学式:A: ,E: ,F: ,Y: 。
(2)反应⑤的化学方程式为: 。
(3)1 mol B通过反应②得到 1 mol F,B中F的质量分数为72%,则B的化学式为 。
22.1919年,Langmuir 提出等电子原理:原子数相同、电子总数相同的分子、互称为等电子体。等电子体的结构相似,物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:
和 ; 和 。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO2-互为等电子体的分子有: 、 。
五、(本题包括2小题,共18分)
23.(8分)含有氨基(―NH2)的化合物通常能够与盐酸反应,生成盐酸盐。如:
R―NH2 +HCl →R―NH2・HCl (R―代表烷基、苯基等)
现有两种化合物A和B,它们互为同分异构体。已知:
①它们都是对位二取代苯;
②它们的相对分子质量都是137;
③A既能被NaOH溶液中和,又可以跟盐酸成盐,但不能与FeCl3 溶液发生显色反应;B既不能被NaOH溶液中和,也不能跟盐酸成盐;
④它们的组成 元素只可能是C、H、O、N、Cl 中的几种。
请按要求填空:
(1)A和B的分子式是 。
(2)A的结构简式是 ;B的结构简式是 。
24.(10分)环己烯可以通过丁二烯与乙烯发生环化加成反应得到:
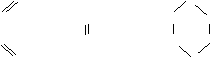 CH2
CH2
CH2
CH2
![]()
![]()
![]() CH + CH2 → CH CH2 (也可表示为
CH + CH2 → CH CH2 (也可表示为 ![]() )
)
CH CH2 CH CH2
CH2 CH2
丁二烯 乙烯 环己烯
实验证明,下列反应中反应物分子的环外双键比环内双键更容易被氧化:
![]()
![]()
![]()
现仅以丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
丁二烯→① A →② B →③ C →④ D →⑤![]() △
△
请按要求填空:
(1)A的结构简式是 ;B的结构简式是 。
(2)写出下列反应的化学方程式和反应类型:
反应④ ,反应类型 。
反应⑤ ,反应类型 。
六、(本题包括2小题,共18分)
25.(8分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热该混合物,逸出能使湿润的红色石蕊试纸变蓝的气体;用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33g。另一份加入含0.001 mol KMnO4的酸性溶液,MnO4-恰好完全被还原为Mn2+。
(1)该结晶水合物中含有的两种阳离子是 和 ,阴离子是 。
(2)试通过计算确定该结晶水合物的化学式。
26.(10分)石油化工是江苏省的支柱产业之一,聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2=CH2 +Cl2 → CH2Cl―CH2Cl……………………………①
CH2Cl―CH2Cl → CH2 = CHCl +HCl……………………… ②
请回答以下问题:
(1)已知反应①中二氯乙烷的产率(产率= 实际产量/理论产量)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t。
(计算结果保留1位小数)
(2)为充分利用副产物氯化氢,该工厂后来将下列反应运用于生产:
2CH2= CH2 +4HCl +O2→ 2CH2Cl―CH2Cl +2H2O………………………③
由反应①、③获得二氯乙烷,再将二氯乙烷通过反应②得到氯乙烯和副产物氯化氢,副产物氯化氢供反应③使用,形成了新工艺。
由于副反应的存在,生产中投入的乙烯全部被消耗时,反应①、③中二氯乙烷的产率依次为a%、c%;二氯乙烷全部被消耗时,反应②中氯化氢的产率为b%。试计算:反应①、③中乙烯的投料比为多少时,新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余(假设在发生的副反应中即不生成氯化氢,也不消耗氯化氢)。