普通高等学校招生全国统一考试化学测试
(北京卷)
(化学部分)
6.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是
A.植物油不能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
7.近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80MPa下合成出金刚石,具有深远意义。下列说法不正确的是
A.由二氧化碳合成金刚石是化学变化
B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠
D.金刚石中只含有非极性共价键
8.下列指定微粒的个数比为2:1的是
A.Be2+离子中的质子和中子 B.12H原子中的质子和中子
C.NaHCO3晶体中的阳离子和阴离子 D.BaO2(过氧化钠)固体中的阴离子和阳离子
9.用NA表示阿伏加德罗常数,下列叙述中正确的是
A.0.1 mol・L-1稀硫酸100 mL中含有硫酸根个数为0.1 NA
B.1 mol CH3+(碳正离子)中含有电子数为10 NA
C.2.4 g金属镁与足量的盐酸反应,转移电子数为2NA
D.12.4 g白磷中含有磷原子数为0.4NA
10.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.Na2SO3溶液(BaCl2) B.FeCl2溶液(KSCN)
C.KI(淀粉溶液) D.HCHO溶液(石蕊试剂)
11.已知0.1 mol・L-1的二元酸H2A溶液的pH=4.0,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:[Na+]+[H+]=[HA-]+[OH-]+2[A2-]
D.在Na2A溶液中一定有:[Na+]>[A2-]>[H+]>[OH-]
12.从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O===7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
A.Cu2S既是氧化产物又是还原产物
B.5 mol FeS2发生反应,有10 mol电子转移
C.产物中的SO42-离子有一部分是氧化产物
D.FeS2只作还原剂
13.20℃时,饱和KCl溶液的密度1.174g・cm-3,物质的量的浓度为4.0 mol・L-1,则下列说法中不正确的是
A.25℃时,饱和KCl溶液的浓度大于4.0 mol・L-1
B.此溶液中KCl的质量分数为![]()
C.20℃时,密度小于1.174g・cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g・cm-3
14.在一定温度下,一定体积的的密闭容器中有如下平衡:H2(气)+I2(气)![]() 2HI(气)。已知H2和I2的起始浓度均为0.10 mol・L-1,达到平衡时HI的浓度为0.16 mol・L-1。若H2和I2的起始浓度均变为0.20 mol・L-1,则平衡时H2的浓度(mol・L-1)是
2HI(气)。已知H2和I2的起始浓度均为0.10 mol・L-1,达到平衡时HI的浓度为0.16 mol・L-1。若H2和I2的起始浓度均变为0.20 mol・L-1,则平衡时H2的浓度(mol・L-1)是
A.0.16 B.0.08 C.0.04 D.0.02
26.(16分)
(1)化合物A(C6H10O)是一种有机溶剂。A可以发生以下变化:
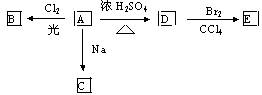
①A分子中的官能团名称是 ;
②A只有一种一氯取代物B。写出由A转化为B的化学方程式 ;
③A的同分异构体F也可以有框图内A的的各种变化,且F的一氯取代物有三种。
F的结构简式是 。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号) 。
①加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是 。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。
“TBHQ”的结构简式是 。
27.(15分)X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应:Y+X→A(气),Y+Z→B(气)。请针对以下两种情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
①Y的化学式是 ;
②生成固体C的化学方程式是 。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式是 ;
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是 ;
③将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是 。
28.(18分)资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
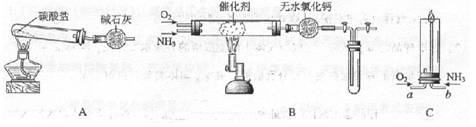
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是 ;
碱石灰的作用是 。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精灯加热:
①氨催化氧化的化学方程式是 ;试管内气体变为红棕色,该反应的化学方程式是 。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因
。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的顺序是 ,其理由是 。
②氨气燃烧的化学方程式是 。
29.(12分)有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12 L气体(标准状况),则样品①中氧化铜的质量为 g.
(2)乙取样品② a g强热,生成的气体不能使澄清的石灰水变浑浊。再将反应后的固体与足量的稀硝酸微热,充分反应后,有b g固体剩余,该剩余固体的化学式为 。样品②中氧化铜质量为 g(以含a、b的代数式表示)。
(3)丙称量样品③强热后剩余的固体,质量比样品减少了c g,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 。