无机物的推断及检验
一、选择题
1.图示为含同一种元素的a、b、c、d、e五种物质的转化关系。其中a是单质,b是气态 氢化物,c、d是氧化物,e是该元素最高价氧化物对应水化物,则a不可能是( )
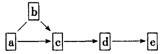
①F2 ②N2 ③C ④S
A.只有① B.②和④
C.③和④ D.①和③
2.某白色固体可能由①NH4Cl ②AlCl3 ③NaCl ④AgNO3 ⑤KOH中的一种或几种组成,此固体投入水中得澄清溶液,该溶液可使酚酞呈红色,若向溶液中加稀硝酸到过量,有白色沉淀生成。对原固体的判断不正确的是( )
A.肯定存在① B.至少存在②和⑤
C.无法确定是否有③ D.至少存在①、④、⑤
3.在下列溶液中,分别加入少量的二氧化锰粉末,可能发生反应的是( )
A.KI溶液 B.酸性KI溶液
C.KOH溶液 D.K2CO3溶液
4.下列各组溶液,不用其它试剂就不能将它们区别开的是( )
A.石灰水和碳酸钠 B.偏铝酸钠和盐酸
C.石灰水和磷酸 D.硫酸铝和氢氧化钠
5.气体X可能含有NH3、Cl2、HBr、CO2中的一种或几种。已知X通入AgNO3溶液时产生淡黄色沉淀,该沉淀不溶于稀硝酸,若将X通入澄清石灰水中,不见沉淀生成,有关气体X的成分说法正确的是( )
A.一定含HBr B.一定不含CO2
C.一定不含NH3,可能含有CO2 D.可能含有CO2和Cl2
6.下列各组溶液,常温下用化学方法、但不用任何其它试剂就可以将它们区别开的是 ( )
A.硫酸铜、氯化钡、氢氧化钠、硝酸钡
B.氢氧化钙、氯化钠、碳酸钠、氯化钡
C.氯化亚铁、硫酸钠、氯化铝、氢氧化钠
D.氯化钡、硝酸钾、碳酸钠、硫酸钠
7.下列实验所得的结论正确的是( )
A.在含S2-、Br-、I-离子的溶液中通入Cl2,再滴入淀粉溶液后显蓝色 ,则溶液中不再有S2-
B.某盐与盐酸反应生成的气体能使石灰水变浑浊,则该盐一定是碳酸盐
C.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量铁粉,过滤后在母液中加盐酸,发现有白色沉淀析出,则滤渣中可能有铜和银
D.检验Na2SO3溶液是否被氧化,取样加入少量Ba(NO3)2,再用HNO3酸化,若有白色沉淀析出,则说明Na2SO3已被氧化
8.某固体X与浓H2SO4共热时能生成一种酸性气体,把氨水加入X溶液中,能生成白色沉淀,继续加氨水,沉淀消失,则X可能是( )
A.AlCl3 B.AgNO3 C.CuCl2 D.Mg(NO3)2
9.有X、Y、Z三种试液,在Ba(OH)2溶液中加入X,有白色沉淀生成,在沉淀中加入Y,沉淀溶解并产生气体,最后加入Z又产生白色沉淀,则试液X、Y、Z可能依次是( )
A.Na2CO3、H2SO4、MgSO4 B.Na2CO3、Na2SO3、Na2SO4
C.K2CO3、HCl、AgNO3 D.Na2CO3、HNO3、MgSO4
10.下列各组溶液,只用组内溶液互相混合的方法就能鉴别的组别是( )
A.Na2SO4、BaCl2、KNO3、NaCl B.Na2SO4、Na2CO3、BaCl2、HCl
C.NaOH、Na2SO4、FeCl3、MgCl2 D.NaCl、AgNO3、NaNO3、HCl
二、非选择题
11.已知:Ag(NH3)2+2H+=Ag++2NH4+,今有一白色固体,可能是由 Al2(SO4)3,AgNO3,BaCl2,NH4Cl,KOH,Na2S中的2种或3种组成,为确 定该白色固体组成,进行以下实验:取白色固体少许,加入适量蒸馏水充分振荡,得到无色 溶液;取无色溶液少许,滴加稀硝酸,有白色沉淀生成。
(1)此白色固体必须含有的物体是①第一组________;②第二组________。
(2)若要确定白色固体的组成,还需做的实验是________________。
12.X、Y、Z、W为常见的四种单质,常温下X是固体,Y是液体,Z是无色气体。W为黄绿 色气体。其反应关系如下,其中B的溶液显强酸性。
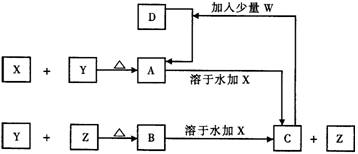
(1)根据反应推断X、Y、Z的化学式:X________ Y________Z________
(2)指出X的元素在元素周期表中的位置:________________
(3)写出A溶于水后加入X的离子方程式:________________
(4)写出C与过量W反应的离子方程式:________________
13.下图是中学化学中常见的物质间化学反应关系图示,其中本注明用量的物质间的反 应均按恰好充分反应处理,其它有关信息已在框图中说明:
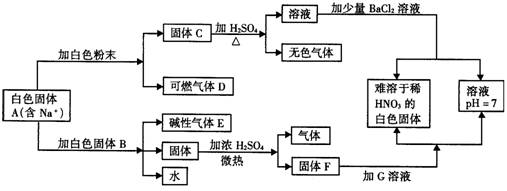
(1)写出下列物质的化学式:
A:________ C:________ D:________ E:________ F:________ G:________
(2)写出下列反应的化学方程式:
A![]() D气体________________
D气体________________
(3)白色固体B的化学式是否能确定?________理由是__________________________
14.氯气和二氧化氮气体在室温下可以化合生成一种新的气态化合物A,为了测定A的组成进行以下实验,取Cl2、NO2混合气总体积5L,测定反应后所得气体体积随Cl2在原混合气体中所占体积分数x的变化而变化的规律。实验测知当Cl2所占体积分数为0.2或0.6 时,反应后的总体积均为4L。
(1)通过分析和计算求得化合物A的化学式为________,发生反应的化学方程式为________________
(2)试讨论当x的取植范围不同时,反应后总体积V随x变化的函数关系。
_____________________________,__________________________
无机物的推断及检验一参考答案
1.A 2.B 3.B 4.A 5.AC 6.C 7.A 8.B 9.CD 10.BC
11.(1)①Al2(SO4)3和过量的KOH的混合物 ②AgNO3和过量的KOH、NH4Cl的混合物 (2)继续滴加衡KNO3至溶液明显呈酸性,若白色沉淀溶解,为Al2(SO4)3、KON的混合物,若白色沉淀不溶解,为AgNO3、NH4Cl、KOH的混合物。
12.(1)Fe、Br2、H2 (2)第4周期Ⅷ族
(3)Fe+2Fe3+![]() 3Fe2+
3Fe2+
(4)2Fe2++4Br-+3Cl![]() 2Fe3++2Br2+6Cl-
2Fe3++2Br2+6Cl-
13.(1)A:NaOH C:Na2CO3 D:CH4 E:NH3 F:NaHSO4 G:Ba(OH)2
(2)CH3COONa+NaOH![]() Na2CO3+CH4
Na2CO3+CH4![]()
(3)不能:只能确定含有NH![]() ,而阴离子可能是Cl-、Br-、CO
,而阴离子可能是Cl-、Br-、CO![]() 等。
等。
14.(1)NClO2 (元素符号顺序可颠倒) Cl2+2NO2![]() 2NClO2
2NClO2
(2)x≤![]() V=(1-x) x>
V=(1-x) x>![]() V=2.5(x+1)
V=2.5(x+1)