高三化学月考题
化 学
相对原子质量:
H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27
S:32 Cl:35.5 K:39 Ca:40 Fe:56 Cu:64 Zn:65
一、选择题(每小题只有一个符合题意的选项,共计45分)
1.用NA表示阿佛加德罗常数,下列说法不正确的是 ( )
A.标准状态下的辛烷22.4L完全燃烧产生CO2分子数为8NA
B.18g水中所含电子个数为10 NA
C.46gNO2和46gN2O4中所含原子数均为3 NA
D.1L2mol・L-1的Mg(NO3)2溶液中含NO-3个数为4 NA
2.已知在酸性介质中下列物质氧化KI时,自身发生如下变化: Fe3+→Fe2+;MnO-4→Mn2+;Cl2→2Cl-;HNO3→NO如果分别用等物质的量的物质去氧化KI,得到I2最多的是( )
A.Fe3+ B.MnO-4 C.Cl2 D.HNO3
|
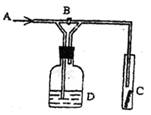
从A处通干燥的氯气,C中干燥的红色布条无变
化,如关闭B,C中干燥的红色布条褪色,则D
中所装溶液是 ( )
A.浓H2SO4 B.饱和NaCl溶液
C.NaOH溶液 D.NaBr溶液
4.咖喱是一种烹饪辅料,若沾到白色衬衣上,用普通肥皂清洗,黄色污渍变成红色,经水漂洗后红色又恢复到黄色,据此现象,你认为咖喱汁与下列何种试剂可能有相似的化学作用 ( )
A.品红溶液 B.石蕊试液
C.氯水 D.KI-淀粉液
5.向BaCl2溶液中通CO2气体,无明显现象,但若先向溶液中通入下列何种气体后再通CO2就会出现白色浑浊 ( )
A.SO2 B.Cl2 C.HCl D.NH3
6.某地区的地表层存在大量KNO3、Na2SO4・10H2O等矿物,你认为该地区的气候特点是
( )
A.干旱 B.多雨 C.旱季雨季分明 D.洪涝
7.由两种金属组成的混合物50g,在氯气中充分燃烧后,固体质量增加71g,原金属混合物可能是 ( )
A.铝和铁 B.铝和镁 C.钠和钾 D.锌和铜
8.下列有关物质性质的叙述中正确的是 ( )
A.氯化铜浓溶液呈蓝色
B.钠在空气中燃烧产物里阴、阳离子个数比为1:1
C.向饱和Na2CO3溶液中通一定量CO2,一定可以看到浑浊
D.向饱和NaOH溶液中通过量CO2气体,一定会出现浑浊
9. 0.5mol CH4气体完全燃烧生成CO2气体和液态水时放出热量445KJ,表示该过程的热化学反应方程式正确的是 ( )
A.2CH4(g)+4O2(g) 2CO2(g)+4H2O(l) △H=+890KJ・mol-1
B.CH4(g)+2 O2(g) CO2(g)+2H2O(l) △H=+890KJ・mol-1
C.CH4(g)+2 O2(g) CO2(g)+2H2O(l) △H=-890KJ・mol-1
D.![]() CH4(g)+O2(g)
CH4(g)+O2(g) ![]() CO2(g)+H2O(l)
△H=-890KJ・mol-1
CO2(g)+H2O(l)
△H=-890KJ・mol-1
10.饮用水的消毒剂有多种,其中杀菌能力强,又不影响水质的理想消毒剂是 ( )
A.漂白粉 B.苯酚 C.氯气 D.臭氧
11.已知BrCl能发生如下发应
与金属:n BrCl+2M MCln+MBrn
与 水:BrCl+H2O HBrO+HCl下列判断不正确的是 ( )
A.BrCl是共价化合物
B.与水反应时,BrCl既是氧化剂也是还原剂
C.BrCl分子中存在极性键
D.BrCl具有强的氧化性,其氧化性比Br2强
12.下列反应对应的离子方程式中正确的是 ( )
A.FeCl3溶液中加入铁粉:Fe+Fe3+ 2Fe2+
B.NH4HSO4溶液中加入少量NaOH:NH+4+OH- NH3・H2O
C.饱和石灰水与饱和CaCl2溶液混合:Ca2++2OH- Ca(OH)2↓
D.氯气通入Na2SO3溶液中:Cl2+SO32-+H2O SO42-+2HCl
13.NaH是一种离子化合物,与水反应时生成烧碱和氢气,它也能与乙醇,液氨等反应产生氢气。下列有关NaH的叙述正确的是 ( )
A.跟水反应时,水作氯化剂
B.NaH中阳离子半径大于阴离子半径
C.跟液氨反应时,生成氢气外,还生成铵盐
D.与乙醇反应时,放出氢气的速率比与水反应时更快
14.用98%(质量分数)的浓硫酸来配制一定体积的1.0mol・L-1的稀硫酸时,不需要用到下列哪种仪器 ( )
A.玻璃棒 B.胶头滴管 C.托盘天平 D.容量瓶
15.苹果汁中含有Fe2+,它是人们喜欢的一种补铁饮料,现榨的苹果汁在空气中会由淡绿色逐渐变为棕黄色。若榨汁时加入维生素C,可以防止这种现象发生。这说明维生素C具有 ( )
A.氧化性 B.还原性 C.碱性 D.酸性
二、填空题(每空2分,共计32分)
16.多硫离子Sx2-(x是2―6的整数)在碱性溶液中被BrO-3氧化成SO2-4,BrO-3自身被还原成Br-,该反应的离子方程式是(要配平)
该反应中Sx2-作还原剂。每1mol Sx2-失去 mol电子。若通过测定BrO-3与OH-的用量情况来确定x的值,至少需要确定以下A―C中的 才能确定Sx2-中的x的值.
A.BrO-3或OH-的绝对用量 B.BrO-3与OH-的绝对用量
|
![]() C.两者用量比多硫化钠是一种重要的多硫化物,利用反应2Na+xs
Na2Sx在一
C.两者用量比多硫化钠是一种重要的多硫化物,利用反应2Na+xs
Na2Sx在一
定条件下制成的钠硫可逆电池是目前推广使用的一种新型高能电池,该电池工作时的正极反应是 ,给该电池充电时,钠极反应与外电源的
极相连接。
17.下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体其余均为气体。根据图中关系推断:
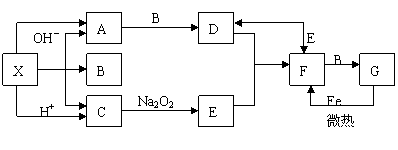 |
(1)化学式X A B
(2)写出C→E的化学反应方程式
(3)实验室收集气体D和F的方法依次是 法和 法。
18.口香糖的生产已有很久历史,咀嚼口香糖有很多益处,但其残留物也会带来污染。为研究口香糖残留物的粘合力与温度的关系,一位同学在研究性学习中通过实验,测定了除去糖分的口香糖与瓷砖地面的粘合力,得到了如下表所示的一组数据:
|
| 温度 (℃) |
(N) | ||||||
| 1 | 15 | 2.0 | ||||||
| 2 | 25 | 3.1 | ||||||
| 3 | 30 | 3.3 | ||||||
| 4 | 35 | 3.6 | ||||||
| 5 | 37 | 4.6 | ||||||
| 6 | 40 | 4.0 | ||||||
| 7 | 45 | 2.5 | ||||||
| 8 | 50 | 1.4 |
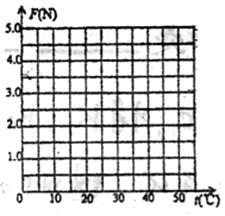
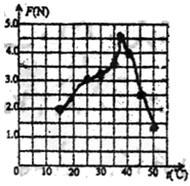
(1)请根据测得的数据,在坐标图中绘出粘合力F随温度变化的曲线,将数据转化为
坐标图的优点是 。
(2)该同学准备通过问卷调查了解当地口香糖的消费量和人们对其污染的认识。在确
定调查对象时,他有两种选择:一是公众;二是口香糖的消售商店。请你在两者中选择一个,并说明你选择的理由。
。
(3)请从不同的角度提出两个减小口香糖污染的建议或措施:
①
②
三、实验题(33分)
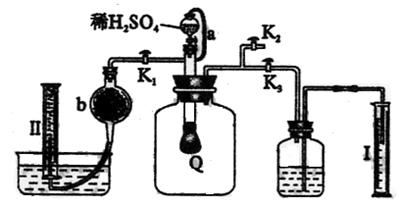
19.为了测定已部分变质的过氧化钠样品的纯度,设计右图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开了漏斗的活塞,将稀硫酸滴入气球中。请填空:
|
(1)Q内发生化学反应时,生成的气体是 。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是
,应当打开的是 。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开
K1,这时可观察到的现象是
。
(4)b中装的固体试剂是 ,为什么要缓缓打开K1
。
(5)实验结束时,量筒I中有x mL水,量筒II中收集到y mL气体(已折算成标准状
态),则过氧化钠的纯度的数学表达式是
(需化成最简表达式。本空3分)
20.SO2是主要的大气污染物之一,为了粗略地测量周围环境中SO2的含量,某学生课外活动小组设计了下图的实验装置。
(1)检查该装置的气密性时,先在试管中加入适量水,使玻璃管未端浸没在水中,然
后 (填写操作方法),若看到 (填现象)时,表明装置气密性良好。
(2)向试管中加入5×10-1的碘水1.0mL,用适量蒸馏水稀释后再滴入2―3滴淀粉溶液,配制成溶液A,测定指定地点空气中SO2含量时,推拉注射器的活塞,反复抽气,当溶液 (填颜色变化情况)时,可认为反应恰好完全进行,此时停止抽气,该反应的化学反应方程式是 。
(3)我国环境空气质量标准中对SO2含量的最高限值如下表:
| 浓度限值(mg・m-3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
该学生活动小组分成了第一和第二两个实验小组,使用相同的实验装置和溶液A,在同一地点测定空气中SO2含量,当恰好完全反应时,记录抽气次数为第一小组120次,第二小组140次(假定每次抽气均为500mL),据此可计算出空气中SO2含量,第一小组结果为 mg・m-3,第二小组结果为 mg・m-3。
(4)你认为第 小组的实验更接近实际情况,该地空气中SO2含量属 级标准,如两小组所用药品和装置均无问题,你认为导致另一小组实验误差较大的主要原因是 。
高三第一次月考题
化学参考答案
一、选择题(每小题只有一个符合题意的选项,共计45分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| A | B | B | B | D | A | C | D | C | D | B | C | A | C | B |
二、填空题(每空2分,共计32分)
16.3Sx2-+6(x-1)OH-+(3x+1)BrO-3 3xSO2-4+(3x+1)Br-+3(x-1)H2O
6x+2 C xS+2e-=Sx2- 负
17.(1)NH4HCO3 NH3 H2O
|
(3)排水 向上排空气
18.(曲线折线均给分)
(1)使数据反映的规律更加直观
(2)公众―更便于了解人们对口香糖污染的认识或销售商店―更便于了解当地的口香糖消费量
(3)①研制、生产可食的口香糖
②改善口香糖成分,使其离开口腔后粘合力迅速减小或制订相关法规,加强人们保持环境的意识
三、实验题
19.(1)O2和CO2 (2)K1、K2 K3
(3)①气球逐渐变小 ②量筒II中有气体进入,水被排出
(4)碱石灰 控制气流量,使CO2能被碱石灰充分吸收
(5)![]()
20.(1)轻轻向外拉注射器活塞 试管中玻璃管口有气泡冒出
(2)蓝色刚好褪去 SO2+I2+2H2O H2SO4+2HI
(3)0.53 0.46
(4)一 三 第二小组抽气速度过快,空气中SO2未被碘水充分吸收