高三化学有机化学综合练习(二)
可能用到的相对原子质量: H: 1 O: 16 N: 14 Na: 23 Cl: 35.5 C: 12 Ca: 40
一、选择题(下列各题只有1个选项符合题意。每小题2分,共20分。)
1.下列变化中,属于化学变化的是
①橡胶的老化 ②油脂的硬化 ③石油的裂化 ④蛋白质的盐析
A.①②③④ B.只有①②③
C.只有①③ D.只有②③
2.生活中的一些问题常涉及到化学知识,下列叙述中正确的是
① 使用明矾可软化硬水;② 硫酸钡难溶于水和酸,可做X光透视肠胃的药剂;③ 铁制品在干燥的空气中容易生锈;④ 医疗中消毒用的是体积分数为75%的酒精;⑤ 棉花、蚕丝和人造毛的主要成分都是纤维素;⑥ 福尔马林是混合物,可用来制作生物标本
A.①②③ B.④⑤⑥ C. ①③⑤ D.②④⑥
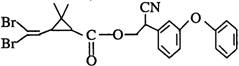 3.拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:
3.拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:
下列对该化合物叙述正确的是
A.属于芳香烃 B.属于卤代烃
C.在酸性条件下不水解 D.在一定条件下可以发生加成反应
![]()
![]()
![]()
![]()
![]() 4.X是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已
4.X是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已
CN CN OCOCH3
被广泛应用于声、热、光的传感等方面。它是由HC≡CH、(CN)2、CH3COOH三种单体通过适宜的反应形成的。由X的结构式分析合成过程中发生反应的类型有 ①加成反应 ②取代反应 ③缩聚反应 ④加聚反应 ⑤酯化反应
A.①④⑤ B.①④ C.①②④ D.①②③
5. 下列除去括号内杂质的有关操作方法不正确的是
A.淀粉溶液(葡萄糖):渗析
B.乙醇(乙酸):加KOH溶液,分液
C.甲醛溶液(甲酸):加NaOH溶液,蒸馏
 D.肥皂液(甘油):加食盐搅拌、盐析、过滤
D.肥皂液(甘油):加食盐搅拌、盐析、过滤
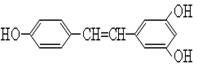
白藜芦醇(其结构如右图所示)广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌作用。
6.能够跟1mol白藜芦醇起反应的Br2或H2的最大用量分别是
A.1mol 1mol B.3.5mol 7mol C.3.5mol 6mol D.6mol 7mol
7. 下列有关白藜芦醇的说法不正确的是
A.具有弱酸性 B.能与NaOH溶液反应
C.不能发生水解反应 D.不能发生加聚反应
8.下列式子表示一种有机物的结构,关于它的性状的叙述不正确的是
A.它有酸性,能与纯碱溶液反应
B.可以水解,水解产物只有一种
C.1mol该有机物与NaOH溶液共热,最多能消耗6mol的NaOH
D.该有机物能与溴水发生取代反应
9.有8种物质:①甲烷;②苯;③聚乙烯;④聚异戊二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯。既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是:
A.③④⑤⑧ B.④⑤⑦⑧ C.④⑤⑧ D.③④⑤⑦⑧
10.工业上将苯蒸气通过赤热的铁合成一种传热载体化合物,其分子中苯环上的一氯代物有3种,1mol该化合物催化加氢时最多消耗6molH2,则该传热载体化合物是
A.![]() B.
B.![]()
C.![]() D.
D.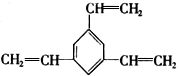
二、选择题(下列各题只有1个选项符合题意。每小题3分,共30分。)
11.某链状有机物分子中含m个-CH3,n个-CH2-, a个![]() 其余为-OH,则羟基的数目可能是
其余为-OH,则羟基的数目可能是
A.2n+3a-m B.a+2-m C.n+m+a D.a+2n+2-m
![]()
![]()
![]()
![]()
![]() 12.X是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已
12.X是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已
CN CN OCOCH3
被广泛应用于声、热、光的传感等方面。它是由HC≡CH、(CN)2、CH3COOH三种单体通过适宜的反应形成的。由X的结构式分析合成过程中发生反应的类型有 ①加成反应 ②取代反应 ③缩聚反应 ④加聚反应 ⑤酯化反应
A.①④⑤ B.①④ C.①②④ D.①②③
13.为了除去苯中混有的少量苯酚,下列的实验正确的是
A.在分液漏斗中,加入足量1mol・L-1NaOH溶液,充分振荡后,分液分离
B.在分液漏斗中,加入足量1mol・L-1FeCl3,充分振荡后,分液分离
C.在烧杯中,加入足量浓溴水,充分搅拌后,过滤分离
D.在烧杯中,加入足量冷水,充分搅拌后,过滤分离
![]() 14.3个氨基酸(R-CH-COOH,烃基R可同可不同)失去2个H2O缩合成三肽化合物,
14.3个氨基酸(R-CH-COOH,烃基R可同可不同)失去2个H2O缩合成三肽化合物,
![]() NH2
NH2
现有分子式为C36H57O18N11的十一肽化合物完全水解生成甘氨酸(C2H5O2N)、丙氨酸(C3H7O2N)、谷氨酸(C5H9O4N),在缩合成十一肽化合物时,这三种氨基酸的物质的量之比为
A.3:3:5 B.3:5:3 C.5:3:3 D.8:7:7
15.下列有机物中,对于可能在一个平面上的最多原子数目的判断,正确的是
A.丙烷最多有6个原子处于同一平面上
B.环己烷最多有12个原子处于同一平面上
C.苯乙烯(![]() )最多有16个原子处于同一平面上
)最多有16个原子处于同一平面上
 D.CH3CH=CH-C≡C-CF3最多有10个原子处于同一平面上
D.CH3CH=CH-C≡C-CF3最多有10个原子处于同一平面上
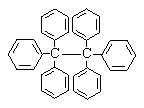
16.六苯乙烷为白色固体,其结构表示如图:
下列有关说法中不正确的是
A.它是一种芳香烃,易溶于乙醚中
B.它的分子式为C38H30,是非极性分子
C.它的一氯代物有三种同分异构体
D.在同一平面上的原子最多有14个
17.过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,他可由冰醋酸与过氧化氢在一定条件下制得;他可以迅速杀灭多种微生物,包括多种病毒(如:SARS
病毒)、细菌、真菌及芽孢,有关过氧乙酸的叙述正确的是
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸可与苯酚混合使用
C.由过氧化氢与醋酸制取过氧乙酸的反应属于氧化还原反应
D.浓过氧乙酸中加入少许紫色石蕊试液,振荡后试液一定呈红色
18.一有机物A可发生如下变化,已知C为羧酸,而C、E都不能发生银镜反应,则A可能的结构有
|
|
![]() D E
D E
A.2种 B.3种 C.4种 D.5种
19.有一气体有机物X,有三种同分异构体。取3.0g X充分燃烧后,把生成物依次通过盛有浓硫酸和碱石灰的两个试剂瓶,分别增重3.8g和8.8g。下列判断正确的是
A.X的分子式C2H2D2 B.X的分子式C2HD3
C.X可合成高分子化合物 D.X分子中所有原子均在同一平面上
20.美国科学家威廉・诺尔斯、柏利・沙普利斯和日本化学家野依良治因通过使用快速和可控的重要化学反应来合成某些手性分子的方法而获得2001年的诺贝尔化学奖.所谓手性分子是指在分子中,当当一个碳原子上连有彼此互不相同的四个原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.凡是有一个手性碳原子的物质一定具有光性活性.例如,有机化合物:![]() 有光学活性,分别发生如下反应①与甲酸发生酯化反应;②与NaOH水溶液共热;③与银氨溶液作用;④在催化剂存在下与氢气作用后,生成的有机物无光学活性的是
有光学活性,分别发生如下反应①与甲酸发生酯化反应;②与NaOH水溶液共热;③与银氨溶液作用;④在催化剂存在下与氢气作用后,生成的有机物无光学活性的是
A.①③ B.②③ C.②④ D.③④
三、填空简答(27分)
21.(6分)1992年世界新技术发明中的七项发明奖中有一项是关于“结束PET塑料的烦恼”。软塑料瓶是聚对苯二甲酸乙二酯制成的,它的废料成为人们头痛的问题(垃圾),其处理方法是将聚酯磨成粉末,然后加人甲醇进行醇解(酯交换),使PET分解成小分子,其原理可用化学方程式表示:
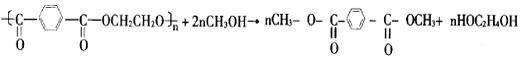 |
若将分解得到的产物提纯后,再重新合成PET,写出反应的化学方程式(有机物写结构简式)和反应类型。
反应(1)______________________________________________ ,反应类型;____________。
反应(2)______________________________________________,反应类型;____________。
22.(6分)松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
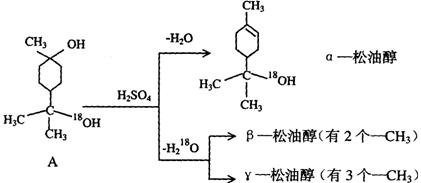
(1)α-松油醇的分子式 。
(2)α-松油醇所属的有机物类别是 (多选扣分)。
(a)醇 (b)酚 (c)饱和一元醇
(3)α-松油醇能发生的反应类型是 (多选扣分)。
(a)加成 (b)水解 (c)氧化
(4)在许多香料中松油醇还有少量以酯的形式出现,写出RCOOH和α-松油醇反应
的化学方程式 。
(5)写结构简式:β-松油醇 ,γ松油醇 。
23.(15分)2000年10月10日,瑞典皇家科学院宣布,美国加利福尼亚大学的艾伦-J-黑格、美国宾夕法尼亚大学的艾伦-G-马克迪尔米德和日本筑波大学的白川秀树三位科学家因为对导电聚合物的发现和发展而获得本年度诺贝尔化学奖。 20世纪70年代,白川英树掌握一种方法,能控制黑色的聚乙炔薄膜中两种异构体的比例,这两种异构体被称为顺式聚乙炔和反式聚乙炔。一天,由于误放多出千倍的催化剂,令他惊奇的事发生了,眼前出现银色的聚乙炔薄膜,原来是纯净的反式聚乙炔.他在另一种温度下重复实验,又出现铜色的聚乙炔薄膜,证实是纯净的顺式聚乙炔。
1977年,白川教授等人发现,在塑料聚乙炔中添加碘这一杂质后,聚乙炔便像金属那样具有导电性。聚乙炔具有导电性,关键是聚乙炔的特殊结构和碘这一杂质在起作用.
![]() (1)试用化学方程式表示聚乙炔的形成过程
。
(1)试用化学方程式表示聚乙炔的形成过程
。
(2)若已知白川英树发现银色的聚乙炔薄膜是
纯净的反式聚乙炔,其结构片段如右图所示,
请写出铜色的聚乙炔薄膜-顺式聚乙炔的结构片段
![]() 。
。
(3)导电聚合物的研究成果,还对分子电子学的迅速发展起到推动作用。日本的赤木教授成功合成了具有螺旋状链式结构的聚乙炔如图。试设想螺旋状链式结构的聚乙炔是否可以用来制成电子零件中不可缺少的线圈和电磁体 。
(4)现有银色的聚乙炔薄膜和铜色的聚乙炔薄膜以及聚苯乙烯的混合物共13g,若完全燃烧,则消耗的氧气及生成的二氧化碳的量能否确定 ,其原因是
。
(5)一种与聚乙炔具有相同最简式的有机物,其相对分子质量是52,该分子是由电石为原料合成的,它是合成某种橡胶的中间体,它有多种同分异构体。
①它的一种链式结构的同分异构体的结构简式是 。该同分异构体的分子中,所有的原子是否共面 ,所有的碳原子是否共线 。
②它的另一种同分异构体的每个碳原子均达到饱和,且空间构型中碳与碳之间的夹角都相同,该同分异构体的分子中直接键合的三个碳原子间的夹角是 ,请画出它的空间构型 。
(6)另一种与聚乙炔具有相同最简式的有机物,其相对分子质量是104。
①若该化合物分子的一氯代物只有一种同分异构体;则该有机物的结构简式
为 。它的二氯代物有 种同分异构体;三氯代物有 种同分异构体。
②若该有机物为芳香烃,则其结构简式为 。该分子中,是否所有原子一定在同一平面内 。
四、实验题(10分)
24.(10分)已知,1,2―二溴乙烷的主要物理性质是
| 熔点 | 沸点 | 密度 | 溶解性 |
| 9.79℃ | 131.4℃ | 2.18g・cm-3 | 难溶于水易溶于醇醚等 |
下图为实验用乙烯与液溴作用制取1,2―二溴乙烷的部分装置图,
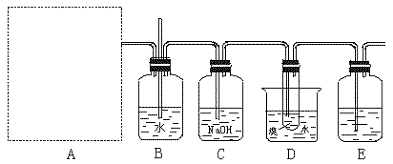
(1)试在方框内画出乙烯的发生装置图。
(2)B、D中都盛有水,这两个装置的作用分别是 。
(3)C和E装置都盛有NaOH溶液,它们的作用是 。
(4)试写出以乙醇、浓硫酸、液溴为主要原料生成1,2―二溴乙烷的主要化学反应方程式 。
五、计算题(13分)
25.(6分)饱和一元醇A和B,B分子中碳原子比A多1,取A和B混合物4.8 g与足量金属Na反应,产生标准状况下H2 1.344 L,试确定A和B的结构式;A和B的物质的量之比为多少?
26.(7分)有总物质的量一定的甲烷和某有机物A(分子式为CaHbOc,a≥1、c≥1、b为正整数)的混合物。
(1)若混合物中甲烷和A不论以何种比例混合,其完全燃烧所生成的水的物质的量不变,则A的组成必须满足的条件是 ;符合此条件的A中,相对分子质量最小的A的分子式为 。
(2)若混合物中甲烷和A不论以何种比例混合,其完全燃烧所消耗的氧气和生成的水的物质的量均不变,则A的组成必须满足的条件是 ;符合此条件的A中,相对分子质量最小的A的分子式为 。
(3)若有机物CxHy(x、y为正整数)和CaHbOc(a≥x)不论以何种比例混合,只要混合物的总物质的量一定,完全燃烧时所消耗的氧气和生成的水的物质的量均不变,那么,这两种有机物的组成必须满足的条件是(用含x、y、a、b、c等的代数式表示)
。