高三化学有机化学综合练习(三)
可能用到的相对原子质量: H: 1 O: 16 C: 12 N: 14 Na: 23 Cl: 35.5
一、选择题(下列各题只有1个选项符合题意。每小题2分,共20分。)
1.下列变化属于化学变化的是
①钝化 ②煤的气化 ③煤的干馏④石油的裂化 ⑤石油的分馏 ⑥油脂的皂化
A.全是 B.除②③外 C.除②⑤⑥外 D.除⑤外
2.生活中的一些问题常涉及到化学知识,下列叙述不正确的是
A.糯米中的淀粉一经发生水解反应,就酿造成酒
B.福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水
C.棉花和人造丝的主要成分都是纤维素
D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气
3.一类组成最简单的有机化合物叫硅烷, 它的分子组成与烷烃相似.,下列有关说法中错误的是
A.硅烷的分子通式可表示为SinH2n+2 B.甲硅烷燃烧生成二氧化硅和水
C.甲硅烷(SiH4)的密度小于甲烷(CH4) D.甲硅烷的热稳定性强于甲烷
4.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断反应物与水反应产物正确的是
A.ZnC2水 解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
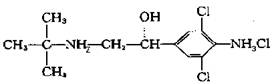 5.据新闻媒体报道,在香港、广东等地发生了多起因食用含有“瘦肉精”的猪肉和猪内脏而引起的中毒事件。“瘦肉精”一般可使猪等畜禽生长速率、饲料转化率、瘦肉率提高10%以上,因此常被广泛滥用。“瘦肉精”的结构简式如右图所示,下列说法不正确的是
5.据新闻媒体报道,在香港、广东等地发生了多起因食用含有“瘦肉精”的猪肉和猪内脏而引起的中毒事件。“瘦肉精”一般可使猪等畜禽生长速率、饲料转化率、瘦肉率提高10%以上,因此常被广泛滥用。“瘦肉精”的结构简式如右图所示,下列说法不正确的是
A.分子式为C12H19N2Cl3O
B.能发生消去反应
C.能与NaOH溶液反应
D.分子中苯环上的一溴代物有两种
6.白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是 ①检验自来水中是否含氯离子②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否含甲醇
A.①② B.①④ C.②③ D.③④
7.在绿色化学工艺中,理想状态是反应物中的原子全部转化为欲制得的产物.如用
CH3C≡CH合成CH2=C(CH3)COOCH3,欲使原子利用率达到最高,还需要的反应物是
A.H2和CO2 B.CO2和H2O C.CO和CH3OH D.CH3OH和H2
8.若某有机物分子中只含有C、N、H三种元素,以n(C)、n(N)分别表示C、N的原子数目,则H原子数最多为
A.2n(C)+2+n(N) B.2n(C)+2+2n(N)
C.2n(C)+1+2n(N) D.3n(C)+2n(N)
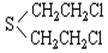 9.黑龙江省齐齐哈尔市2003年8月4日发生一起侵华日军遗弃化学毒剂芥子气泄漏致多人受伤事件。芥子气被称为“毒气之王”,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点219℃,液体密度1.27g/cm-3;难溶于水,易溶于有机溶剂(汽油、煤油、酒精),能溶于动植物脂肪中;能与高锰酸钾及硫化钠溶液反应。战争使用状态为液滴态或雾状。下列有关芥子气的叙述不正确的是
9.黑龙江省齐齐哈尔市2003年8月4日发生一起侵华日军遗弃化学毒剂芥子气泄漏致多人受伤事件。芥子气被称为“毒气之王”,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点219℃,液体密度1.27g/cm-3;难溶于水,易溶于有机溶剂(汽油、煤油、酒精),能溶于动植物脂肪中;能与高锰酸钾及硫化钠溶液反应。战争使用状态为液滴态或雾状。下列有关芥子气的叙述不正确的是
A.它能与漂白粉反应 B.它遇水能水解
C.它易溶于水和汽油 D.它能发生消去反应
10.约翰·芬恩(John fenn)等三位科学家因在蛋白质等大分子研究领域的杰出贡献获得了2002年的诺贝尔化学奖。下列有关说法正确的是
A.蚕丝、羊毛、棉花的主要成分都是蛋白质
B.蛋白质溶液不能产生丁达尔效应
C.蛋白质溶液中加入CuSO4溶液产生盐析现象
D.蛋白质在紫外线的照射下将失会去生理活性
二、选择题(下列各题只有1个选项符合题意。每小题3分,共30分。)
11.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实能说明上述观点的是
A.甲醛和甲酸都能发生银镜反应
B.乙烯能发生加成反应,而乙烷不能发生加成反应
C.苯酚与溴水直接就可反应,而苯与溴水反应则需要加铁屑
D.苯酚和乙酸都可以与NaOH反应
12.乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是
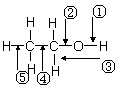 A.和金属钠作用时,键①断裂
A.和金属钠作用时,键①断裂
B.和浓硫酸共热至170 ℃时,键②和⑤断裂
C.和乙酸、浓硫酸共热时,键②断裂
D.在铜催化下和氧气反应时,键①和③断裂
13.将1L C3H8与aL O2混合起来点燃,C3H8完全反应后所得混合气体的体积为bL(气体的体积均在120℃、101Kpa时测定),使得bL混合气体通过足量的碱石灰,知气体的体积为 cL。若b-c=6,则a值为
A.4.3 B.4.5 C.5.0 D.6.0
14.某有机物的分子式为C8H8,经研究表明该有机物不能发生加成反应和加聚反应,在常温下难于被酸性KMnO4溶液氧化,但在一定条件下却可与Cl2发生取代反应,而且其一氯代物只有一种。下列对该有机物结构的推断中一定正确的是
A.该有机物中含有碳碳双键 B.该有机物属于芳香烃
C.该有机物分子具有平面环状结构 D.该有机物具有三维空间的立体结构
15.a molCH2=C(CH3)- C(CH3)= CH2和b mol CH2=CH-CN加聚形成高聚物A,A在适
量O2中完全燃烧,生成的CO2、H2O(g)、N2在相同条件下的体积比依次为
12∶8∶1。则a∶b为
A.1∶1 B.1∶2 C.2∶3 D.3∶2
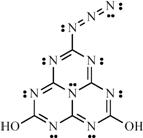 16.1994年伟大的化学家鲍林(Linus Pauling)教授谢世时,留给后人很多谜团,其中一个结构式如图所示。老人为什么画这个结构式?它是生命前物质?它能合成吗?它有什么性质?不得而知。也许这是永远无法解开的谜;也许你有朝一日能解开它。某同学对此结构及性质有如下的推测,你认为不正确的是
16.1994年伟大的化学家鲍林(Linus Pauling)教授谢世时,留给后人很多谜团,其中一个结构式如图所示。老人为什么画这个结构式?它是生命前物质?它能合成吗?它有什么性质?不得而知。也许这是永远无法解开的谜;也许你有朝一日能解开它。某同学对此结构及性质有如下的推测,你认为不正确的是
A.它的分子式是C6N10H2O2
B.该物质最多可以有18个原子处于同一个平面上
C.它可以与别的物质发生加成反应
D.因其含氮量高,有可能作炸药
17.化合物甲,乙、丙有如下反应转化关系:
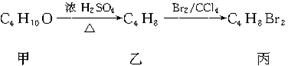
丙的结构简式不可能是
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
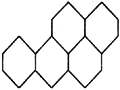 18.苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照物),其结构式中有5个环互相并合如图。每个碳原子上都有1个双键(C=C),分子中共有m个双键,五个环都处在同一平面上,分子中可能同时处于同一平面上的原子数为n个,则m、n分别为
18.苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照物),其结构式中有5个环互相并合如图。每个碳原子上都有1个双键(C=C),分子中共有m个双键,五个环都处在同一平面上,分子中可能同时处于同一平面上的原子数为n个,则m、n分别为
A.10、30 B.10、32 C.11、30 D.11、32
19.有机物甲可氧化生成羧酸,也可还原生成醇,由甲生成的羧酸和醇在一定条件下,可以生成化合物乙,其分子式为C2H4O2。下列叙述中不正确的是
A.甲分子中C的质量分数为40% B.甲在常温常压下为无色液体
C.乙比甲的沸点高 D.乙和甲的最简式相同
![]() 20.3个氨基酸(R-CH-COOH,烃基R可同可不同)失去2个H2O缩合成三肽化合物,
20.3个氨基酸(R-CH-COOH,烃基R可同可不同)失去2个H2O缩合成三肽化合物,
![]() NH2
NH2
现有分子式为C36H57O18N11的十一肽化合物完全水解生成甘氨酸(C2H5O2N)、丙氨酸(C3H7O2N)、谷氨酸(C5H9O4N),在缩合成十一肽化合物时,这三种氨基酸的物质的量之比为
A.3:3:5 B.3:5:3 C.5:3:3 D.8:7:7
三、填空简答(27分)
21.(6分)实验室中常用格氏试剂制取醇类,格氏试剂(RMgX)的制法是:
|
![]() RX+Mg RMgX(R为烃基,x为卤素)
RX+Mg RMgX(R为烃基,x为卤素)
|
![]()
![]()
![]()
![]() RMgX+R’CHO
R—CH—O—MgX
R—CH—OH+Mg(OH)X
RMgX+R’CHO
R—CH—O—MgX
R—CH—OH+Mg(OH)X
R’ R’
|
|
以A为原料合成乙酸异丁酯(CH3—C—O—CH—CH2—CH3)的流程如下(部分反应物及反应条件没有列出),A主要来源于石油裂解气,A的产量常作为衡量石油化工水平的标志。试回答:
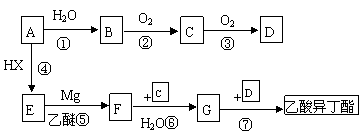 |
(1)上述流程中,属于或含加成反应的是(填写序号)_________________。
(2)写出F的结构简式_________________。
(3)写出下列反应的化学方程式:
反应①__________________________________。
反应⑦__________________________________。
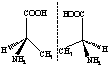 22.(15分)美国科学家威廉·诺尔斯、柏利·沙普利斯和日本化学家野依良治因通过使用快速和可控的重要化学反应来合成某些手性分子的方法而获得2001年的诺贝尔化学奖.所谓手性分子是指在分子结构
22.(15分)美国科学家威廉·诺尔斯、柏利·沙普利斯和日本化学家野依良治因通过使用快速和可控的重要化学反应来合成某些手性分子的方法而获得2001年的诺贝尔化学奖.所谓手性分子是指在分子结构![]() 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。例如, 我们学过的普通氨基酸中丙氨酸
( 如图所示 )即为手性分子,它有两种形状:(S)- 丙氨酸和 (R)- 丙氨酸, 它们互为镜像。不管我们如何旋转这些图形,都不能让他们互相重叠.这种现象称为对映异构。
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。例如, 我们学过的普通氨基酸中丙氨酸
( 如图所示 )即为手性分子,它有两种形状:(S)- 丙氨酸和 (R)- 丙氨酸, 它们互为镜像。不管我们如何旋转这些图形,都不能让他们互相重叠.这种现象称为对映异构。
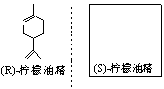
(1)柠檬油精是手性分子,有两种对映异构体(如图所示),进入人体会感受到不同味道,其中一种是柠檬味,而一种是橘味.请在右图方框中划出具有柠檬味的(S)- 柠檬油精的结构。
(2) 乳酸![]() 是人体生理活动的一种代谢产物,乳酸中是否存在对映异构体
;乳酸分子中可能处于同一平面的原子数目最多为
。
是人体生理活动的一种代谢产物,乳酸中是否存在对映异构体
;乳酸分子中可能处于同一平面的原子数目最多为
。
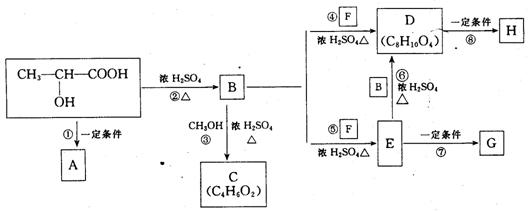
(3)下图是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
请回答下列问题:
1)写出C、D的结构简式:C , D 。
2)指出反应②③所属的类型:② ③ 。
3)写出下列反应的化学方程式:① , ⑤ 。
4)作为隐形眼镜的制作材料,对其性能的要求除应具有良好的光学性能外,还应具有良好的透气性和亲水性.一般采用E的聚合物G而不是D的聚合物H来制作隐形眼镜,其主要理由是 。
23.(6分)2002年诺贝尔化学奖之一授予“发明了利用核磁共振技术测定溶液中生物大分子三维结构方法”的科学家。质子核磁共振谱(NMR)是研究有机化合物结构的最有力手段之一。在所研究化合物的分子中,每一种结构类型的等价(或称为等性)H原子,在NMR谱中都给出相应的峰(信号).谱中峰的强度是与分子中给定类型的H原子数成比例的.例如,乙醇的NMR谱中有三个信号,其强度比为3:2:1.
(1)在常温下测得的某烃C8H10的NMR谱上,观察到两种质子给出的信号,其强度之比为2:3,试确定该烃的结构简式 .该烃在光照下生成的一氯代物在NMR谱中可产生几种信号 ,试确定强度比为 .
(2)在常温下测定相对分子质量为128的某烃的NMR,若观察到两种质子给出的信号,且其强度之比为1:1,则该烃的结构简式为 .若观察到两种质子给出的信号,且其强度之比为9:1,则该烃的结构简式为 .
(3)最近报道在 –100oC的低温下合成了化合物X,元素分析仪得出其分子式为C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,而碳的化学环境却有2种,而且,分子中既有C—C单键,又有C=C双键.温度升高将迅速分解.X的结构式是 .
四、实验题(9分)
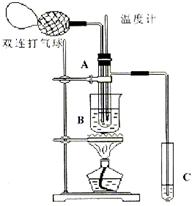
24.(9分)乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图14所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60°C~80°C时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下:
| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8°C | 117.9°C | 290°C | 197.2°C | 100°C |
 请回答下列问题:
请回答下列问题:
(1)试管A内在60°C~80°C时发生的主要反应的化学方程式为(注明反应条件)________________________。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在_____________;当试管A内的主要反应完成后温度计水银球的位置应在________________________________,目的是_____________________________。
(3)烧杯B的作用是____________________;烧杯B内盛装的液体可以是____________(写出一种即可)。
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。
所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。
该方案为___________________________________________________________。
五、计算题(14分)
25.(6分)有A、B两种饱和一元醇,它们分子中碳原子数相差1,且沸点A>B。已知它们的混合物7.8g充分燃烧生成CO213.2g,求A、B可能是何种醇?并写出它们的结构简式。
26.(8分)汽车尾气污染是一重大公害,汽车的内燃机中,汽油气化后与空气按一定比例混合进入气缸,发动机用电火花引燃,温度迅速升高,气体体积急剧膨胀,产生压力推动活塞运动,并排出尾气,为简化讨论,设汽油的成分为辛烷,并设空气中O2的体积分数为20%,其余为N2。
(1)设辛烷气体与空气的体积比(相同条件下)为a,要使辛烷完全燃烧,计算a的最小值amin。
(2)若辛烷与空气的体积比大于amin时,污染大气的有害气体相对增多的是何种成分 ,当其体积为n L时,其化学反应方程式为 。
(3)若辛烷与空气的体积比大于amin时,则尾气中所含污染大气的有害成分增多的是 ,产生此气体的化学反应方程式为 。