高三化学实验综合练习(一)
可能用到的相对原子质量: H: 1 O: 16 N: 14 Na: 23 Cl: 35.5 C: 12 Ag:108
一、选择题(下列各题只有1个选项符合题意。每小题2分,共16分。)
1.下列实验操作时,一般情况下不应该相互接触的是
A.用胶头滴管向试管滴液体时,滴管尖端与试管内壁
B.向容量瓶中注入溶液时,移液用的玻棒与容量瓶颈内壁
C.用移液管向锥形瓶内注液时,移液管的尖嘴与锥形瓶内壁
D.实验室将气体HCl溶于水时,漏斗口与水面
2.下列事故处理不正确的是
A.不慎把浓硫酸沾在手上,立即用干布拭去,再用水冲洗
B.不慎把苯酚沾在手上,立即用70℃以上的热水冲洗
C.金属钠着火,应立即用沙土灭火
D.酒精灯不慎碰翻着火,用湿布盖灭
3.给50mL某液体加热的操作中,以下仪器必须用到的是
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥铁架台 ⑦泥三角 ⑧坩埚 ⑨铁三脚架
A.②③⑤⑧ B.③⑥⑦⑧ C.①③④⑥ D.②③⑤⑥
4.实验室制取下列各组气体时,两种气体均能使用启普发生器制取的是( )
A.H2 、CO2 B.O2 、NH3 C.Cl2 、HCl D.C2H2 、H2
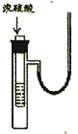 5.右图小试管中盛有几毫升水,与大试管连通的U型细玻管内放有少
5.右图小试管中盛有几毫升水,与大试管连通的U型细玻管内放有少
量的水(已染成红色)。如沿小试管壁小心地慢慢注入3毫升浓硫酸,
静置片刻后,U型细玻管中可观察到的液面现象是
A.左高右低 B.左低右高
C.左右一样高 D.来回振动
6.下列有关加热操作中错误的是
A.用酒精灯加热时,受热物应放在内焰部分
B.加热试管中的液体时,液体体积不超过试管容积的1/3
C.用水浴加热时,温度计要插在水浴中
D.用坩埚加热时,坩埚要放在泥三角上
7.用pH试纸检测溶液的pH值时的正确操作是
A.将pH试纸浸入溶液中,观察并比较变色情况
B.用蒸馏水冲洗玻棒后,用玻棒蘸取溶液点在试纸上,与标准比色卡比色
C.将试纸用少量蒸馏水润湿沾在玻棒的一端,在溶液里浸一下,与标准比色卡比色
D.用洁净、干燥的玻棒蘸取溶液,点在试纸上,与标准比色卡比色
8.下列使用托盘天平的操作中,正确的是
A.调整天平时,应先将游码放在刻度尺中间,然后调节左,右螺丝
B.称量物应放在右盘,砝码应放在左盘
C.加砝码时应按其质量由小到大的顺序添加,最后移动游码
D.称量结束时用镊子将砝码夹回砝码盒中,并把游码移回零处
二、选择题(下列各题只有1个选项符合题意。每小题3分,共30分。)
9.某学生发现滴瓶中的溶液有悬浮物,拟用右图所示操作进行过滤,操作上错误的地方有
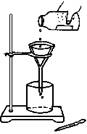 A.4 处 B.3 处
C.2 处 D.1 处
A.4 处 B.3 处
C.2 处 D.1 处
10.某学生做完实验以后,采用以下方法分别清洗所用仪器:
①用稀硝酸清洗做过银镜反应的试管;
②用酒精清洗做过碘升华的烧杯;
③用浓盐酸清洗做过高锰酸钾分解实验的试管;
④用盐酸清洗长期存放过三氯化铁溶液的试剂瓶;
⑤用氢氧化钠溶液清洗盛过苯酚的试管
A.②不对 B.③④不对 C.④⑤不对 D.全部正确
11.实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯 ②固定铁圈位置 ③放上蒸发皿④加热搅拌 ⑤停止加热、余热蒸干 其正确的操作顺序为
A.②③④⑤ B.①②③④⑤ C.②③①④⑤ D.②①③④⑤
12.以下实验:①为检验R-X是碘代烷,将R-X与NaOH水溶液混合后再加入AgNO3溶液时,却出现了褐色沉淀;②实验室里用无水乙醇和浓硫酸共热至140℃制乙烯,却得不到乙烯;③用锌与稀硫酸反应制取氢气,用排水法收集不到氢气;④做醛的还原性实验时,加入新制的Cu(OH)2悬浊液后未出现红色沉淀;⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后再加入银氨溶液,却未出现银镜。其中由于缺少必要的实验步骤而造成失败的实验是
 A.①②③④⑤ B.①③④⑤ C.③④⑤ D.③⑤
A.①②③④⑤ B.①③④⑤ C.③④⑤ D.③⑤
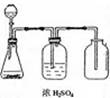
13.右图是一套实验室制取气体的装置,用于发生、干燥和收集气体。下列各组物质中能用这套装置进行的是
A.铜屑和浓硫酸 B.MnO2和浓盐酸
C.锌和稀硫酸 D.CaCO3和盐酸
14.现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ⑧溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
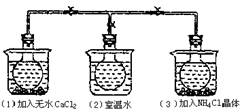 15.如下图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中。在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是
15.如下图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中。在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是
A.CaCl2溶于水时放出热量 B.烧瓶(1)中气体的压强增大
C.NH4Cl溶于水时放出热量 D.烧瓶(3)中气体的压强减小
16.以下实验能获得成功的是
A.用含结晶水的醋酸钠和碱石灰共热制甲烷气体
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
 D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
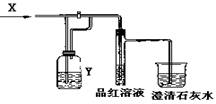
17.下图是一套检验气体性质的实验装置,向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色。据此判断气体X和洗气瓶内溶液Y分别可能是
| A | B | C | D | |
| X | SO2 | H2S | CO2 | Cl2 |
| Y | 饱和NaHCO3溶液 | 浓硫酸 | Na2SO3溶液 | Na2CO3溶液 |
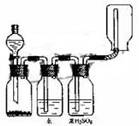 18.右图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
18.右图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
A.锌和盐酸发生氢气
B.二氧化锰和浓盐酸生成氯气
C.碳酸钙和盐酸生成二氧化碳
D.氯化钠和浓硫酸生成氯化氢
三、实验设计与评价(20分)
 19.(9分)拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
19.(9分)拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| 气体 | a | b | c | d |
| C2H4 | 乙醇 | 浓H2SO4 | NaOH溶液 | 浓H2SO4 |
| Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓H2SO4 |
| NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| NO | 稀HNO3 | 铜屑 | H2O | P2O5 |
(1)上述方法中可以得到干燥、纯净的气体是 。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体 ,理由是 。
②气体 ,理由是 。
③气体 ,理由是 。
④气体 ,理由是 。
20.(4分)某中学化学小组查阅资料发现金属氧化物A也能催化氯酸钾的分解,且A和二氧化锰的最佳催化温度均为500℃左右。于是对A和二氧化锰的催化性能进行了定量对照实验。实验时均以收满500mL氧气为准(其他可能影响实验的因素均已忽略)。
表一 用MnO2作催化剂
| 实验序号 | KCIO3质量(g) | MnO2质量(g) | 反应温度(℃) | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
表二 用A作催化剂
| 实验序号 | KCIO3质量(g) | MnO2质量(g) | 反应温度(℃) | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
请回答:上述实验中的待测数据应是 。
完成此研究后,他们准备发表一篇研究报告,请你替他们拟一报告的题目:
21.(7分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现 象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处
、
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
 四、推断题(8分)
四、推断题(8分)
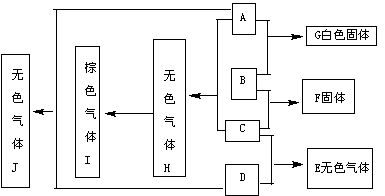
22.(8分)下图中每一个方框内的字母代表一种物质,常温常压下,A、B、C、D、均为单质,且B为金属,其它三个为双原子分子的气体,它们在一定条件下,发生图中所示的化合反应,得到化合物E、F、G、H、I和J,这些化合物在常温常压下的状态及颜色已在图中注明, 有关反应的化学计量数为:
(1)A与B按物质的量之比n(A)∶n(B)=1∶2完全反应生成G
(2)B与C按物质的量之比n(B)∶n(C)=3∶1完全反应生成F
(3)C与D按物质的量之比n(C)∶n(D)=1∶3完全反应生成E
请填空:
(1)物质B是 ,物质D是 。
(2)B与C反应生成F的化学方程式为: 。
(3)A与H反应生成I的化学方程式为: 。
五、综合实验(26分)
23.(13分)Ag/α-Al2O3是石油化学工业的一种重要催化剂,其中Ag起催化作用,α-Al2O3是载体且不溶于硝酸,该催化剂的回收实验如下图所示。其中的转化反应为:
6AgCl+Fe2O3→3Ag2O+2FeCl3
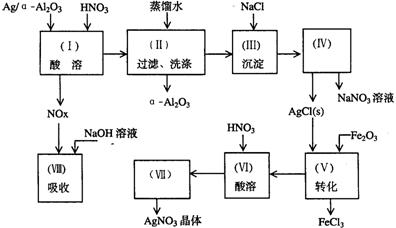
 阅读上述实验流程,完成下列填空:
阅读上述实验流程,完成下列填空:
(1)Ag/α-Al2O3加酸溶解应该选用装置 (选填a、b、c)。
(2)在实验操作(Ⅱ),如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式
。
(3)实验操作(Ⅳ)所需玻璃仪器为 (填写三种)。
(4)实验操作(Ⅶ)从AgNO3溶液获得AgNO3晶体需要进行的实验操作依次为:
(多选扣分)。
(a)蒸馏 (b)蒸发 (c)灼烧 (d)冷却结晶
(5)已知:NO+NO2+2NaOH→2NaNO2+H2O;
2NO2+2NaOH→NaNO3+NaNO2+H2O
NO和NO2的混合气体的组成可表示为NOx。该混合气体通入NaOH溶液被完全吸收时,x的值为
(a)x<1.5 (b)x=1.2 (c)X≥1.5
(6)已知Ag/α-Al2O3中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 和 。
24.(13分)烟草制品燃烧时,所产生的烟雾中存在对人体健康有害的物质包括烟焦油、烟碱(如尼古丁)、CO、烟草生物碱、丙烯醛类、芳香胺、脂肪烯、酚类等一千多种有害物质。下图是检验点燃的香烟烟雾中有害成分的初步方法:
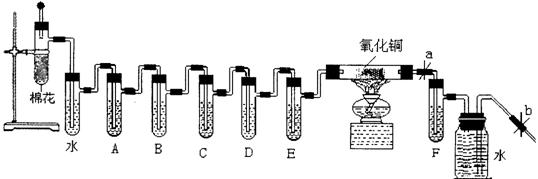
用于检验的试剂有:①乙醇,②澄清石灰水,③饱和NaOH溶液,④酸性高锰酸钾溶液,⑤浓硫酸,⑥银氨液,⑨氯化汞溶液,⑧氧化铜。
(1)将香烟燃烧后的产物进行吸收分析,使燃烧产物依次通过空气冷却、蒸馏水、乙醇……后面的药品顺序由你排定(用序号填入空格)A ,B ,C ,D ,E ,F (尼古丁和丙烯酸成分要单独取样分析)。
(2)要使香烟点燃后继续燃烧而不熄灭,怎样操作能得到保证 ;这是依据什么原理使香烟继续燃烧的?
(3)当更换第三支烟后,取出 中的略带黄色的样液5mL于试管中,后加入2mL银氨液放在水浴中加热,写出发生的银镜反应方程式 ;
(4)当燃尽第七支烟后,再取出 中的褐色样液5mL于试管,后向其中滴加数滴HgCl2溶液,产生白色溶液说明有尼古丁。
(5)通过观察硬质试管中的氧化铝颜色是否变化,来证明燃着的香烟产物中有无 CO?有人认为不行,他的理由是 。但是本实验还是能验证燃着的香烟产物中有CO产生的,是通过 装置中实验现象 得以证明。