高考总复习有机化学练习题(烃五)
班级_______姓名________得分________
1. 1体积某烃的蒸气燃烧生成的二氧化碳比水蒸气多1体积(相同状况),且该烃完全燃烧时需要7倍其体积的氧气,则该烃可能有的同分异构体中可用于合成橡胶的有:
A. 1种 B. 2种 C. 3种 D. 4种
2. 某气态烃在一密闭容器中与氧气混和,完全燃烧后容器的压强与燃烧前容器的压强相等,燃烧前后的温度均保持在150℃,则该气态烃是:
A. C2H6 B. C3H6 C. CH4 D. C2H4
3. 实验测得乙烯与氧气混和气体的密度与空气相同,可知其中乙烯的质量分数是:
A. 25.0% B. 72.4% C. 27.6% D. 75.0%
4. 把m摩C2H4跟n摩H2 混合在密闭容器中,在适当条件下,反应达到平衡时生成p摩C2H6,若将所得平衡混和气体完全燃烧生成二氧化碳和水,需要氧气的量是:
A. 3m+n摩 B. 3m+n/2摩
C. 3m+3p+n/2摩 D. 3m+n/2-3p摩
5. 完全燃烧相同质量的下列各烃,消耗氧气最多的是:
A. CH4 B. C2H4 C. C2H2 D. C6H14
6. 乙烯和某气态烃组成的混和气体完全燃烧时,所需氧气体积是混和气体的4.5倍(相同状况),则该气态烃是:
A. C2H6 B. C3H6 C. C4H8 D. C2H4
7. 在室温下,1升某气体分别与4升氧气混和,在引燃后将气体通过浓硫酸,剩余气体回复至室温时体积变为2升,则该气体是:
①乙烷 ②乙烯 ③乙炔 ④甲烷
A. 只有② B. 只有①②③ C. 只有④ D. 以上均不可能
8. 乙烯中含有杂质烃,当点燃224毫升以上的该气体(标准状况)后,把产生的二氧化碳通过足量的澄清石灰水,共生成了2.1克沉淀,则乙烯可能含有下列气体中的:
A. 丙烯 B. 乙烷 C. 乙炔 D. 甲烷
9. 两种气态烃以任意比例混和,在105℃时1升该混和烃与9升氧气混和,充分燃烧后恢复到原状态,所得的气体仍是10升。下列各组混和烃中不符合此条件的是:
A. CH4 C2H4 B. CH4 C3H6 C. C2H4 C3H4 D. C2H2 C3H6
10. 某烷烃和炔烃的混和气体1升,在催化剂作用下与氢气加成直致完全生成烷烃,在相同条件下测得产物的体积为0.2升,则混和气体中,烷烃与炔烃的体积比为:
A. 1︰4 B. 2︰3 C. 3︰2 D. 4︰1
11. 1.01×105帕、428K时将体积为8升的某烃与适量的氧气组成的混和气体燃烧使之完全反应,再恢复到原温度和压强,测得生成混和气体体积为9升,则此烃分子中的碳原子数为:
A. 4 B. 5 C. 6 D. 8
12. 在能常情况下,某气态烃与氧气的混和气体的总体积为n升,电火花引燃充分燃烧后,将混和气体通过浓硫酸,恢复到原来温度和压强时,气体体积减少到4/7n升,则该烃可能是:
A. 甲烷 B. 乙烯 C. 丙烷 D. 丁炔
13. 140℃时,1体积某烃和4体积O2混和,完全燃烧后恢复到原来的温度和压强,体积不变,该分子式中所含的碳原子数不可能是:
A. 1 B. 2 C. 3 D. 4
14. 常温常压下,一种气态烷烃与一种气态烯烃的混和物共1升,完全燃烧后,恢复到原状况,得到1.2升二氧化碳,则该混和气体中一定含有:
A. 甲烷 B. 乙烯 C. 乙烷 D. 环丙烷
15. 1升某气态烃与7升氧气混和点燃,产生的气体通过浓硫酸,浓硫酸增重3.2克,则该烃可能的分子式为(体积均在标准状下测定):
A. C3H8 B. C4H8 C. C6H14 D. C3H6
16. 通式为CnH2n-2的一种气态烃完全燃烧后生成的CO2和H2O的物质的量之比为4︰3,这种烃的链状同分异构体有(不考虑结构的稳定性与否):
A. 5种 B. 4种 C. 3种 D. 2种
17. 常温常压下,50毫升三种气体烃的混和物与足量氧气混和后点燃爆炸,恢复到原来状况时,体积共缩小100毫升,则三种烃可能是
A. CH4 C2H2 C3H4 B. C2H6 C3H6 C4H6
C. CH4 C2H6 C3H8 D. C2H4 C2H6 C2H2
18. 某气态烃含碳85.7%,1摩尔该烃充分燃烧生成的二氧化碳恰好被1.5升、4摩/升的NaOH溶液吸收生成正盐,这种烃的分子式是:
A. C2H6 B. C3H6 C. C4H8 D. C6H14
19. 在20℃,某气态烃与氧气混合装入密闭容器中,点燃爆炸后,又恢复到20℃,此时容器内气体的压强为反应前的一半,经过NaOH溶液吸收后,容器几乎成为真空,此烃的分子式可能为
A. CH4 B. C2H6 C. C3H8 D. C2H4
20. 某烃在氧气中恰好完全燃烧生成等体积的二氧化碳和水蒸气,测得反应后混和气体的密度比反应前减少1/8(均指120℃,1.01×105帕),则该烃的分子式:
A. C4H6 B. C2H4 C. C3H6 D. C4H8
21. 下列各组混气(高于100℃)按1︰1(摩尔比)与同状态下O2完全燃烧之后,其压强未发生改变的是:
A. C2H6和C2H2 B. C2H6和C2H4 C. C2H4和C2H2 D. CH4和C2H4
22. 两种气态烃以任意比例混和,在105℃时1升该混和烃与9升氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为10升。下列各组混和烃中不符合此条件的是:
A. CH4 C2H4 B. CH4 C3H6 C. C2H4 C3H4 D. C2H2 C3H6
23. amL气态烃混合物与足量的氧气混合点燃爆炸后,恢复到原来状态(常温常压下),体积共缩小amL,则气态烃的可能组合是:
A. CH4,C2H4,C3H4 B. C2H6,C3H6,C4H6
C. CH4,C2H6,C3H8 D. C2H4,C2H2,CH4
24. a毫升3种气态烃的混和物和足量氧气混和点燃爆炸后恢复到原来状态(常温常压),气体体积共缩小了2a毫升(不考虑CO2的溶解)。则这3种烃可能的组合是:
A. CH4,C2H4,C3H4任意体积比
B. CH4,C3H6,C2H2保持C3H6︰C2H2=1︰2(物质的量之比)
C. C2H6,C4H6,C2H2同条件下体积比为2︰1︰2
D. C3H8 ,C4H8 ,C2H2质量比为11︰14︰26
25. 实验室里用电石(主要成分为CaC2)与水(常用食盐水)反应制乙炔时,由于电石中还含有CaS、Ca3P2、Ca3As2等杂质,同时会产生有毒、有恶臭。对下述反应有不利影响的气体,这些气体可用饱和CuSO4溶液除去:
HC≡CH+H2O![]() CH3CHO(沸点20.8℃,易挥发)
CH3CHO(沸点20.8℃,易挥发)
(1)请写出用电石与水反应制备乙炔的化学反应方程式
(2)用下列仪器及导管以电石为原料制取乙醛,如果气体流向为从左到右,正确的连接顺序是(除G以外,短的导管图中均已略去):
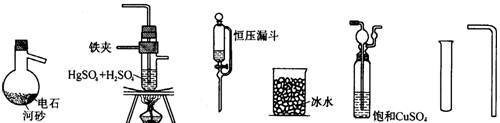
A B C D E F G
接 接 接 接 接 置于 中。
(3)写出含硫气体杂质产生和除去的化学反应方程式
26. “汽车尾气污染”已倍受世人关注。汽车内燃机中,汽油气化后与空气按一定比例混合进入气缸,引擎用电火花点燃。燃烧使汽缸内温度迅速升高,气体体积急剧膨胀,产生压力推动活塞。燃烧时产生的有害气体通过尾气排出污染大气。为简化讨论,以辛烷(C8H18)代表汽油的成分,并设空气中O2占1/5体积,请回答下列问题:
(1)设辛烷气与空气的体积比(相同条件下)为a。要使辛烷正好完全燃烧,a的值为(用小数表示,设此量为a¢);
(2)若辛烷与空气的体积比大于a¢,则尾气所含污染大气的有害气体中,相对含量会增多的是(写化学式) ,产生这种气体的化学方程式是 ;
(3)若辛烷与空气的体积比小于a¢,则尾气所含污染大气的有害气体中,相对含量会增多的是(写化学式) ,产生这种气体的反应方程式是 .
27. 某烃A,B的分子式均为C6H10,它们的分子结构中无支链或侧链。
(1)A为环状化合物,它能与Br2发生加成反应,A的名称是 ;
(2)B为链状烯烃,它与Br2加成后的可能产物只有两种, B的结构简式是 。
28. 1摩尔某有机物A能与1摩尔氢气发生加成,反应的产物是2,2,3-三甲基戊烷,A可能是 。
29. A、B、C、D、E是五种气态烃,其中A、B、C能使溴水褪色。1摩尔C与2摩尔氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子。A与C、B与E分别具有相同的通式,A在催化剂存在下与氢气反应可得到B,在同温同压下B与氮气的密度相同,D是最简单的有机物,E没有同类的异构体,则五种气态烃的名称分别是:
。
30. A、B、C、D四种有机物中的碳原子数相同.标准状况下烃A对氢气的相对密度为13;烃B跟氢溴酸反应生成C;C跟D混和后加入氢氧化钠并加热,能生成B。
(1)试写出A、B、C、D的结构简式 ;
(2)写出有关反应的化学方程式 .
31. 气体A只含X、Y两种短周期元素,X的原子序数大于Y的原子序数,B、D、E是中学化学中的常见气体,各物质有如下图所示的转化关系:
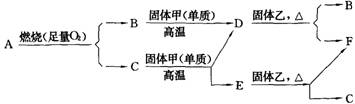
(1)若气体A中,X与Y的质量比小于3,则气体A中一定有_______________(写分子式),判断的理由是 .
(2)若气体A的分子为线型分子,且X与Y两种元素的质量比在数值上等于X的相对原子质量,则A气体的燃烧反应方程式为 。
(3)C与固体甲在高温下的反应方程式为: 。
(4)B、C、E的沸点从低到高的顺序为___________________.
A. B>C>E B. E<B<C C. B<E<C D. E>C>B
32. 取两支洁净的试管,分别盛足量的氨水和烧碱溶液,接着再放入0.1摩的化合物甲,结果都会产生9克气体M,盛氨水的试管会同时产生一种沉淀,盛烧碱溶液的试管也有白色沉淀产生,但振荡试管后,沉淀随之消失。9克气体M在足量的空气中完全燃烧后只产生26.4克二氧化碳和16.2克水,另外又已知甲分子式为AxByCz,且x+y+z=22;试求化合物甲的分子式,并写出它与水反应的化学方程式。
33. 某有机化合物M,其分子式为AxByCz,且x+y+z=22。已知M放入水中即水解生成白色沉淀E和无色气体F。白色沉淀E不溶于氨水,能溶于氢氧化钠溶液。取0.1摩尔M放入足量水中,能收集到9克气体F。将该气体在空气中完全燃烧,只生成26.4克二氧化碳和16.2克水,求:
(1)气体F的分子式
(2)有机化合物M的分子式
(3)写出M与过量的氢氧化钠溶液反应的化学方程式。
[1] B
2 C、D
3 B
4 B
5 A
6 C
7 D
8 A
9 B、D
[1]0 D
[1]1 B
[1]2 D
[1]3 D
[1]4 A
[1]5 A、B
[1]6 B
[1]7 D
[1]8 B
[1]9 C、D
20 D
21 A、D
22 B、D
23 A
24 A、D
25(1)CaC2+2H2O→HC≡CH↑+Ca(OH)2 (2)C A E B D F D (3)CaS+2H2O=H2S↑+Ca(OH)2 H2S+CuSO4=CuS↓(黑)+H2SO4
26 (1)a¢=0.016 (2)CO 2C8H18+17O2![]() 16CO+18H2O或2C8H18+(25-x/2)O2
16CO+18H2O或2C8H18+(25-x/2)O2![]() xCO+(16-x)CO2+18H2O (3)NO、NO2或NOx N2+O2
xCO+(16-x)CO2+18H2O (3)NO、NO2或NOx N2+O2![]() 2NO 2NO+O2=2NO2
2NO 2NO+O2=2NO2
27 (1)环已烯 (2)CH3-CH=CH-CH2-CH=CH2(不能是CH3-CH2-CH=CH-CH=CH2,想想看,为什么?)
28 3,3-二甲基-2-乙基-1-丁烯、3,4,4-三甲基-2-戊烯、3,4,4-三甲基-1-戊烯
29 A是乙炔、B是乙烯、C是1,3-丁二烯、D是甲烷、E是环丙烷
30 (1)A是CH≡CH B是CH2=CH2 C是CH3CH2Br D是CH3CH2OH (2)略
31 (1)H2 X与Y的质量比小于3,即XY的个数比小于1︰4,也就是C、H个数之比小于1︰4 (2)2C2H2+5O2![]() 4CO2+2H2O (3)H2O(g)+C
4CO2+2H2O (3)H2O(g)+C![]() CO+H2 (4)B
CO+H2 (4)B
32 (C2H5)3Al (C2H5)3Al+3H2O=3C2H6+Al(OH)3↓
33 (1)C2H6 (2)Al(C2H5)3或AlC6H15 (3)Al(C2H5)3+NaOH+H2O=NaAlO2+3CH3CH3↑或Al(C2H5)3+3H2O=Al(OH)3↓+3CH3CH3↑,Al(OH)3+NaOH=NaAlO2+2H2O