高考能力测试步步高化学基础训练22
基础训练22 氨 铵盐
(时间60分钟,赋分100分)
●训练指要
氨气的结构、性质和用途;氨气的制备;NH![]() 和铵盐。
和铵盐。
一、选择题(每小题3分,共39分)
1.某白色晶体A与浓硫酸共热有气体B放出,与浓氢氧化钠溶液共热有气体C放出,B、C相遇又生成A。则A是
A.Na2CO3 B.(NH4)3PO4
C.NH4Cl D.NH4HCO3
2.下列4瓶质量分数不同的氨水,其中密度最大的是
A.29%的氨水 B.2.2%的氨水
C.34%的氨水 D.15%的氨水
3.在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是
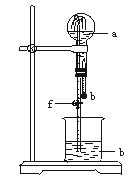
| a | b | |
| A | NO2 | 水 |
| B | CO2 | 4 mol·L-1 NaOH溶液 |
| C | Cl2 | 饱和食盐水 |
| D | NH3 | 1 mol·L-1盐酸 |
4.工业上用氨和二氧化碳反应合成尿素,已知下列物质在一定条件下均能与水反应产生H2和CO2。H2是合成氨的原料,CO2供合成尿素用。若从原料最优转化角度考虑,选用哪种物质作原料较好
A.CO B.石脑油(C5H12、C6H14)
C.CH4 D.焦炭
5.下列是合成氨的简要流程示意图:
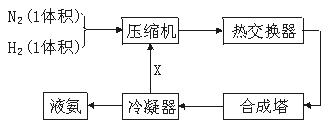
沿X路线回去的物质是
A.N2和H2 B.催化剂
C.N2 D.H2
6.下列各组气体,在通常条件下能稳定共存的是
A.NH3、O2、HCl B.N2、H2、HCl
C.CO2、NO、O2 D.H2S、O2、SO2
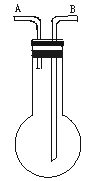
7.在右图装置中,烧瓶是干燥的,位置不得移动,则由A口进气可收集的气体有
A.NO B.SO2
C.CH4 D.NH3
8.某合成氨厂合成氨反应中,测得合成塔入口气体体积比为N2∶H2∶NH3=6∶18∶1,出口气体体积比为N2∶H2∶NH3=9∶27∶8,则氮的转化率为
A.20% B.75% C.25% D.50%
9.某硫铵中混有另一种氮肥,经实验测得此硫铵的含氮量为35.1%,则此硫铵中混入的另一种氮肥是
A.硝酸铵 B.碳酸氢铵
C.氯化铵 D.尿素
10.等体积等物质的量浓度的NH4H2PO4、(NH4)2HPO4、(NH4)3PO4分别与等物质的量浓度的NaOH溶液反应,恰好作用完全生成正盐,则消耗NaOH溶液的体积比为
A.1∶2∶3 B.3∶2∶1
C.1∶1∶1 D.6∶3∶2
11.废切削液中,含2%~5%的NaNO2,直接排放会造成环境污染,下述试剂能使其转化为不引起二次污染的N2的是
A.H2O2 B.NH4Cl
C.NaCl D.浓H2SO4
12.1 L 0.1 mol·L-1的氨水中,所含粒子的物质的量正确的是
A.0.1 mol NH3分子
B.NH3分子和NH3·H2O分子共有0.1 mol
C.0.1 mol NH3·H2O分子
D.NH3分子、NH3·H2O分子和NH+4共有0.1 mol
13.烧瓶中盛有(用向下排空气法收集的)氨气,经测定其密度为同温同压下氢气密度的9.5倍,以此进行“喷泉”实验,进入烧瓶中液体的体积最多可占烧瓶容积的
A.7/8 B.5/6 C.6/7 D.3/4
二、非选择题(共61分)
14.(8分)(2002年全国高考题)制取氨气并完成喷泉实验(图中夹持装置均已略去)
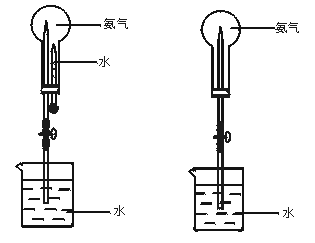
图1 图2
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。
(4)如果只提供如图2的装置,请说明引发喷泉的方法。
15.(8分)氨水是一种混合物,其中溶质的粒子有(填粒子符号) 等分子和离子,而最多的是 。向氨水里加入足量盐酸,氨水原有粒子中数目减少得最多的一种是 ,新增加的粒子是 。
16.(11分)限用一种试剂,经过一次实验(可加热)就能鉴别:Na2CO3、(NH4)2SO4、NH4Cl、KNO3四种无色溶液。[供选择的试剂有:AgNO3溶液,NaOH溶液、Ba(OH)2溶液、盐酸]该试剂是 。所发生反应的离子方程式、实验现象和被鉴别的物质分别记录如下:
| 序号 | 实验现象 | 反应的离子方程式 | 被鉴别的物质 |
| (1) | |||
| (2) | |||
| (3) |
17.(10分)取一根镁条置于坩埚内点燃。得到氧化镁和氮化镁混合物的总质量为0.470 g,冷却后加入足量水,将反应产物加热蒸干并灼烧,得到氧化镁质量为0.486 g。
(1)写出氮化镁与水反应生成氢氧化镁和氨的化学方程式。
(2)计算燃烧所得混合物中氮化镁的质量分数。
18.(10分)标况下,在1 L水中溶解了560 L氨气,且测得所得氨水的密度为0.9 g·
cm-3,求此氨水中溶质的质量分数和物质的量浓度各是多少?
19.(14分)已知NH3和Cl2在常温下混合可发生下列化学反应:2NH3+3Cl2===6HCl+N2或8NH3+3Cl2===6NH4Cl+N2,现有Cl2和NH3共a L,混合后充分反应得气体体积为b
L,若![]() <
<![]() ,求b L气体的组分及被氧化的氨的体积(体积均在同温同压下测得)。
,求b L气体的组分及被氧化的氨的体积(体积均在同温同压下测得)。
高考能力测试步步高化学基础训练22答案
一、1.C
2.解析:氨水随浓度的增大,其密度减小。
答案:B
3.BD
4.解析:依关系C![]() CO2
CO2![]() CO(NH2)2和3H2
CO(NH2)2和3H2![]() 2NH3
2NH3![]() CO(NH2)2。
CO(NH2)2。
答案:B
5.A 6.B
7.解析:收集密度比空气小,但不与空气反应的气体。
答案:CD
8.C
9.解析:硫铵[(NH4)2SO4]的含氮量为21.2%,而尿素中含量为46.7%。
答案:D
10.C 11.B 12.D 13.B
二、14.(1)2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
(2)向下排空气 碱石灰
(3)打开止水夹,挤出胶头滴管中的水,氨气极易溶解于水,致使烧瓶内气体压强迅速减小
(4)打开夹子,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,氨气与水接触,即发生喷泉。
15.NH3、NH3·H2O、NH![]() 、OH-、H+
NH3·H2O
NH3·H2O
Cl-
、OH-、H+
NH3·H2O
NH3·H2O
Cl-
16.Ba(OH)2 (1)只有白色沉淀
Ba2++CO![]() ===BaCO3↓
Na2CO3
===BaCO3↓
Na2CO3
(2)有白色沉淀,并有刺激性气味气体
2NH![]() +SO
+SO![]() +Ba2++2OH-
+Ba2++2OH-![]() BaSO4↓+2NH3↑+H2O (NH4)2SO4
BaSO4↓+2NH3↑+H2O (NH4)2SO4
(3)有刺激性气味气体
NH![]() +OH-
+OH-![]() NH3↑+H2O NH4Cl
NH3↑+H2O NH4Cl
17.(1)Mg3N2+6H2O===2NH3↑+3Mg(OH)2↓ (2)0.17
18.0.298 15.8 mol·L-1
19.N2和HCl
![]() (a+b) L
(a+b) L