�߿��������Բ�����ѧ����ѵ��25
����ѵ��25 ��ѧƽ�� Ӱ�컯ѧƽ�������
��ʱ��60���ӣ�����100�֣�
��ѵ��ָҪ
��ѵ�����������ѧƽ��ı�־����������Чƽ����ص��Ӧ�ã���ѧƽ����йؼ��㼰��ѧƽ�ⳣ������������ԭ���뻯ѧƽ���ƶ���
һ��ѡ���⣨ÿС��5�֣���45�֣���
1.(2003�괺���߿���)��Ӧ��A��g����3B��g��![]() 2C��g������H��0��ƽ�������������¶Ƚ��ͣ�������������ȷ����
2C��g������H��0��ƽ�������������¶Ƚ��ͣ�������������ȷ����
A.����Ӧ���ʼӴ��淴Ӧ���ʱ�С��ƽ��������Ӧ�����ƶ���
B.����Ӧ���ʱ�С���淴Ӧ���ʼӴ�ƽ�����淴Ӧ�����ƶ���
C.����Ӧ���ʺ��淴Ӧ���ʶ���С��ƽ��������Ӧ�����ƶ���
D.����Ӧ���ʺ��淴Ӧ���ʶ���С��ƽ�����淴Ӧ�����ƶ���
2.��2001��ȫ�������⣩��һ���¶��£�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯����������ͼ�����б�������ȷ���Ǫ�
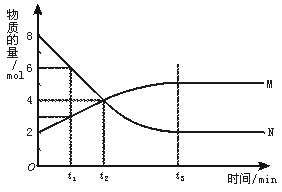
A.��Ӧ�Ļ�ѧ����ʽΪ��2M![]() N
N
B.t2ʱ�����淴Ӧ������ȣ��ﵽƽ�⪤
C.t3ʱ������Ӧ���ʴ����淴Ӧ���ʪ�
D.t1ʱ��N��Ũ����MŨ�ȵ�2����
3.��һ���¶��µĶ����ܱ������У����������������ٸı�ʱ��������Ӧ��A(s)��2B(g) ![]() C(g)��D(g)�Ѵ�ƽ����Ǫ�
C(g)��D(g)�Ѵ�ƽ����Ǫ�
A.��������ѹǿ���������������������������������� B.���������ܶȪ�
C.B�����ʵ���Ũ�ȡ�������������������������D.����������ʵ���
4.��һ���ݻ�ΪV L���ܱ������з���2��L��A��g����1��L��B��g������һ�������·������з�Ӧ��
3A(g)��B(g) ![]() nC(g)��2D(g)��
nC(g)��2D(g)��
�ﵽƽ���A���ʵ���Ũ�ȼ���![]() ����������ƽ��Ħ����������
����������ƽ��Ħ����������![]() ����÷�Ӧ�Ļ�ѧ����ʽ��n��ֵ��
����÷�Ӧ�Ļ�ѧ����ʽ��n��ֵ��
A.1���������������������� B.2���������������������� C.3������������������������������D.4��
5.��һ���̶��ݻ����ܱ������У�����һ���¶Ƚ������·�Ӧ��H2��g����Br2��g��![]() 2HBr��g������֪����1
mol H2��2 mol Br2�ﵽƽ���������a mol HBr������ͬ�����£�����ʼʱ�����H2��Br2��HBr�ֱ�Ϊx mol��y mol��z
mol(����Ϊ0)�ұ���ƽ��ʱ������ֺ��������䡣�����ƶ���һ����ȷ���Ǫ�
2HBr��g������֪����1
mol H2��2 mol Br2�ﵽƽ���������a mol HBr������ͬ�����£�����ʼʱ�����H2��Br2��HBr�ֱ�Ϊx mol��y mol��z
mol(����Ϊ0)�ұ���ƽ��ʱ������ֺ��������䡣�����ƶ���һ����ȷ���Ǫ�
��x��y��zӦ����Ĺ�ϵΪ��4x��z=2y��
�ڴﵽƽ��ʱHBr�����ʵ���Ϊ![]() a mol��
a mol��
�۴ﵽƽ��ʱHBr�����ʵ���Ϊa mol��
��x��y��zӦ����Ĺ�ϵΪx��y=z����
A.�٢ڡ�����������������B.�ڢۡ�����������������C.�ۢܡ�����������������D.�٢ڢ۪�
6.��֪HF�����д�������ƽ�⣺��
2��HF��3![]() 3��HF��2����HF��2
3��HF��2����HF��2![]() 2HF��
2HF��
��ƽ��ʱ��������ƽ��Ħ������Ϊ42 g��mol��1����(HF)3���������Ϊ��
A.��10�������������������������������������������������� B.��10����
C.��10�������������������������������������������������� D.��10����
7.��һ���ܱ������г���1 mol CO2��3 mol H2����850��ʱ����������ﵽ��ʽ��ʾƽ�⣺CO2��H2![]() CO��H2O����֪�ﵽƽ��ʱ����0.75 mol CO����ô��H2��Ϊ9 mol��������������ƽ��ʱ����CO��ˮ���������ʵ���֮�Ϳ���Ϊ��
CO��H2O����֪�ﵽƽ��ʱ����0.75 mol CO����ô��H2��Ϊ9 mol��������������ƽ��ʱ����CO��ˮ���������ʵ���֮�Ϳ���Ϊ��
A.1.2 mol������������������������������������������B.1.5 mol��
C.1.8 mol������������������������������������������������ D.2.5 mol��
8.��һ���̶��ݻ����ܱ������У�����3 L X(g)��2 L Y(g)����һ�������·������з�Ӧ��4X(g)��3Y(g) ![]() 2Q(g)��nR(g)���ﵽƽ����������¶Ȳ��䣬��������ѹǿ��ԭ������5%��X��Ũ�ȼ���1��3����÷�Ӧ����ʽ�е�nֵ��
2Q(g)��nR(g)���ﵽƽ����������¶Ȳ��䣬��������ѹǿ��ԭ������5%��X��Ũ�ȼ���1��3����÷�Ӧ����ʽ�е�nֵ��
A.4���������������������� B.5���������������������� C.6���������������������� D.7��
9.��һ����ƽ��״̬�ķ�Ӧ��X(s)��3Y(g) ![]() 2Z(g)����H��0��Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ���������
2Z(g)����H��0��Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ���������
�ٸ��� �ڵ��¡��۸�ѹ���ܵ�ѹ���ݼ��������������Z��
A.�٢ۢݡ����������������������������������������������� B.�ڢۢݪ�
C.�ڢۢޡ����������������������������������������������� D.�ڢܢ�
������ѡ����(��55��)��
10.(12��)������ܱ������ڼ���a mol PH4I���壬��һ���¶��·������·�Ӧ����
PH4I��s��![]() PH3��g����HI(g)��
PH3��g����HI(g)��
4��H3��g��![]() ��4��g����6H2��g����
��4��g����6H2��g����
2HI��g��![]() H2��g����I2��g����
H2��g����I2��g����
��������Ӧ����ƽ����HIΪb mol��I2(g)Ϊc mol��H2Ϊd mol����
(1)ƽ��������ڣ�4��g���ͣ�H3��g�������ʵ���(�ô���ʽ��ʾ)���������������������������������� ��
(2)a,b,c���ߵĹ�ϵΪa������������������ (�b,c�Ĵ���ʽ)����
(3)b,c,d���ߵĹ�ϵΪb���������������� (�c,d�Ĵ���ʽ)����
11.(12��)��120��ʱ�ֱ���������ĸ���Ӧ����
A.2H2S��O2===2H2O��2S��
B.2H2S��3O2===2H2O��2SO2��
C.C2H4��3O2===2H2O��2CO2��
D.C4H8��6O2===4H2O��4CO2��
(1)����Ӧ���ݻ��̶��������ڽ��У���Ӧǰ�������ܶȣ�d����������ѹǿ��p���ֱ���Ϲ�ϵʽdǰ��d����pǰ��p������������������ �����Ϲ�ϵʽdǰ��d����pǰ��p���������� ������д��Ӧ�Ĵ��ţ�����
��2������Ӧ��ѹǿ�㶨�ݻ��ɱ�������ڽ��У���Ӧǰ�������ܶȣ�d�������������V���ֱ���Ϲ�ϵʽdǰ��d����Vǰ��V������������������ ������dǰ��d����Vǰ��V����������������д��Ӧ�Ĵ��ţ���
12.(9��)��֪t�棬p kPaʱ�����ݻ�ΪV L�ܱ������ڳ���1 mol A��1
mol B���������º�ѹ��ʹ��ӦA(g)��B(g) ![]() C(g)�ﵽƽ��ʱ��C���������Ϊ40%���Իش��й����⣺
C(g)�ﵽƽ��ʱ��C���������Ϊ40%���Իش��й����⣺
(1)��ʹ�¶Ⱥ�ѹǿ�����������º㶨���䣬���ܱ������ڳ���2 mol A��2 mol B����Ӧ�ﵽƽ��ʱ���������ݻ�Ϊ���������� ��C���������Ϊ���������� ��
(2)����ѡһ�ݻ��̶�������ܱ��������Կ����¶�Ϊt�棬ʹ1 mol A��1 mol B��Ӧ�ﵽƽ��״̬ʱ��C�����������Ϊ40%������ܱ��������ݻ�Ϊ���������� ��
13. (10��)�Կ��淴ӦaA��g����bB��g��![]() cC(g)��d�ģ�g���ﵽƽ��ʱ�������ʵ����ʵ���Ũ���������¹�ϵ��
cC(g)��d�ģ�g���ﵽƽ��ʱ�������ʵ����ʵ���Ũ���������¹�ϵ��![]() =K(Ϊһ����)��K��Ϊ��ѧƽ�ⳣ�����䷴Ӧ��Kֵֻ���¶��йء����з�Ӧ��CO��g����H2O��g��
=K(Ϊһ����)��K��Ϊ��ѧƽ�ⳣ�����䷴Ӧ��Kֵֻ���¶��йء����з�Ӧ��CO��g����H2O��g��![]() CO2��g����H2��g����Q����850��ʱ��K��1����
CO2��g����H2��g����Q����850��ʱ��K��1����
(1)�������¶ȵ�950��ʱ���ﵽƽ��ʱK�������� 1(����ڡ���С�ڡ����ڡ�)��
(2) 850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0 mol CO,3.0 mol H2O��1.0 mol CO2��x mol H2����
�ٵ�x��5��0ʱ������ƽ���������������� (�����Ӧ�����淴Ӧ��)�����ƶ�����
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ������������������������� ��
(3)��850��ʱ������x��5.0��x��6��0���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa����b������a������������ b(����ڡ���С�ڡ����ڡ�)��
14.��12�֣���2002���Ϻ��߿��⣩��һ��������ܱ������У��������»�ѧ��Ӧ��
CO2��g����H2��g��===CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺��
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=������������������������ ��
��2���÷�ӦΪ������������������������ ��Ӧ��ѡ�����ȡ����ȣ�����
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬�������������������������������� ��
a.������ѹǿ���䪤
b.���������c(CO)���䪤
c.v����H2��=v����H2O����
d.c(CO2)=c(CO)��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)=c(CO)��c(H2O)�����жϴ�ʱ���¶ȡ�
�߿��������Բ�����ѧ����ѵ��25��
һ��1.C 2.D��3.BC��4.A 5.A��6.C��7.C 8.C��9.C��
����10.(1)n��P4����![]() ��d��c��
mol��
��d��c��
mol��
n��PH3������![]() (4c��d)+b��
mol
(4c��d)+b��
mol
(2)b+2c����(3) ![]() (d��4c)
(d��4c)
11.(1)B��C ��2��D A��
12.(1)![]() V �̡�40������2��
V �̡�40������2��![]() V �̪�
V �̪�
13.(1)С�� (2)���淴Ӧ����x��3��0 (3)С�ڪ�
14.��1��K=![]()
(2)���� ��3��bc (4)830