高三化学复习辅导
重要考点与认知要求:
1、了解这些元素的单质和氢化物的重要性质,并进行比较。
2、了解这些元素的氧化物的重要性质。
3、以Na2O2为例,了解过氧化物的性质。
4、掌握硫酸和硝酸的制备原理、性质和用途。
5、了解磷酸和硅酸的主要性质和用途。
6、了解常见盐类的性质和用途。
7、了解常见化肥的基本性质。
8、了解硫、氮、碳的氧化物对大气的污染,以及防止大气污染。
9、了解一些生活用水的净化及工业污水的处理方法。
复习要点:
1、要掌握以下重要物质的相互关系。
(1)有关O2、H2、H2O、H2O2的转化关系。
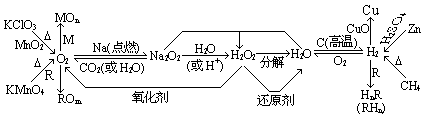
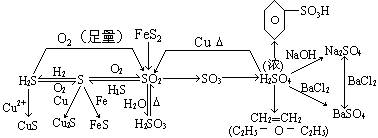
(2)硫及其重要化合物
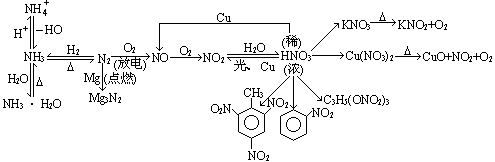
(3)氮气其重要化合物
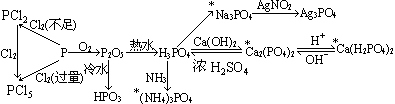
(4)磷及其重要化合物
(5)碳及其重要化合物
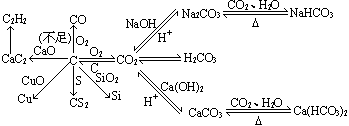
(6)硅及其重要化合物
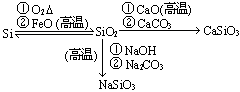
2、非金属的单质、氢化物、氧化物往往在常温下呈气态,因此对于它们的实验室制法、性质、主要用途作一归纳是十分重要的。
(1)常见气体的制备、性质、用途:
| 气体 | 制备反应原理 | 颜色、气味 | 溶解性 | 特性 | 用途 |
| H2 | Zn+H2SO4==ZnSO4+H2 | 无色、无臭 | 难溶 | 可燃性、还原性 | 燃料、还原剂 |
| O2 | 2KClO3 | 无色、无臭 | 难溶 | 氧化性、供呼吸 | 氧化剂、呼吸 |
| N2 | NH4Cl+NaNO2 | 无色、无臭 | 难溶 | 稳定、不活泼 | 保护气、制化肥 |
| Cl2 | MnO2+4HCl==MnCl2+Cl2+2H2O | 黄绿色、刺激性 | 可溶(反应) | 氧化性、有毒 | 化工原料、漂白粉 |
| HCl | 2NaCl+H2SO4 | 无色、刺激性 | 极易溶 | 酸性 | 化工试剂 |
| H2S | FeS+2HCl==H2S+FeCl2 | 无色、臭鸡蛋气味 | 可溶 | 还原性、剧毒 | 还原剂、鉴别 |
| NH3 | 2NH4Cl+Ca(OH)2 2H2O | 无色、刺激性 | 极易溶 (反应) | 易液化、弱碱性 | 致冷剂、化肥 |
| CH4 | CH3COONa+NaOH CH4 | 无色、无臭 | 难溶 | 可燃 | 气体燃料 |
| C2H4 | CH3CH2OH | 无色、略有甜香气味 | 难溶 | 加成、聚合 | 石油化工原料 |
| C2H2 | CaC2+2H2O®C2H2+Ca(OH2) | 无色、无臭 | 微溶 | 可燃、加成 | 焊接、有机化工 |
| CO | HCOOH | 无色、无臭 | 难溶 | 剧毒、可燃、还原 | 还原剂(冶炼) |
| CO2 | CaCO3+2HCl==CaCl2+CO2+H2O | 无色、无臭 | 可溶(反应) | 弱酸性、不支持燃烧 | 灭火、化工原料 |
| SO2 | Na2SO3+H2SO4==Na2SO4+SO2+H2O | 无色、刺激性 | 易溶(反应) | 漂白性、有毒 | 漂白纺织物 |
| NO | 3Cu+8HNO3(稀)==3Cu(NO3)2+2NO+ 4H2O | 无色、无臭 | 难溶 | 剧毒、易被氧化 | 制NHO3中间产物 |
| NO2 | Cu+4HNO3( 浓)==Cu(NO3)2+2NO2 +2H2O | 红棕色、刺激性 | 易溶(反应) | 有毒、氧化性 | 制HNO3 |
(2)常见气体的实验室制取、尾气吸收装置:
|
| 尾气吸收 | ||||
|
分子式 装置 制取气体 的装置 |
|
|
|
|
|
|
| O2
CH4 | O2 | NH3 CH4 | NH3 | |
|
| H2
C2H2 | H2S CO2 NO2 | H2 | H2S NO2 | |
|
| NO C2H4 | Cl2 HCl SO2 | Cl2
SO2 | HCl | |
注:
①因为C2H2、C2H4的气体密度很接近空气,所以不宜用向下排气法收集。
②因为NO极易与空气中氧气反应生成NO2所以只能用排水法收集。
思考:对于NH3和HCl这2种污染性气体的尾气吸收装置为什么要选用倒置的漏斗?
 收集
收集 气体 气体
气体 气体