高三第一学期化学期末考试
可能用到的相对原子质量:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
第Ⅰ卷(选择题 共41分)
把答案填在下列表格中
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
一. 选择题(本题包括18小题,共41分。每小题只有一个选项符合要求,其中第1~13小题,每小题2分;第14―18小题,每小题3分。)
1. 火药是我国古代的“四大发明”之一,我国最早发明的黑火药后来传入了波斯,波斯人将其中一种成份称为“中国盐”。这种成份的化学式是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
2. 下列说法错误的是
A. 铅笔不含铅 B. 纯碱不是碱 C. 水银不含银 D. 重水不是水
3.“纳米材料”是指粒子直径在几纳米到几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物具有的性质是
A. 有丁达尔现象 B. 能全部透过半透膜
C. 所得液体一定能导电 D. 所得溶液一定为悬浊液或乳浊液
4. 下列属于分子晶体的化合物是
A. 石英 B. 干冰 C. 碳化硅 D. 食盐
5. 在元素周期表短周期中的X和Y两种元素可组成化合物![]() ,下列说法正确的是
,下列说法正确的是
A. ![]() 晶体一定是离子晶体
晶体一定是离子晶体
B. X和Y一定不属于同一主族
C. X和Y可能属于同一周期,也可属于两个不同周期
D. 若Y的原子序数为m,X的原子序数一定是![]()
6. 在两个容积相同的容器中,一个盛有![]() 和
和![]() 的混和气体,一个盛有
的混和气体,一个盛有![]() 气体。在同温同压下,两容器内的气体一定具有相同的
① 原子数 ② 分子数 ③ 质子数 ④ 电子数 ⑤ 质量
气体。在同温同压下,两容器内的气体一定具有相同的
① 原子数 ② 分子数 ③ 质子数 ④ 电子数 ⑤ 质量
A. ①② B. ②③ C. ③④⑤ D. ①②③⑤
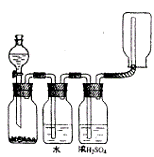
7. 如下图所示。此装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
A. 氯化铵和消石灰生成氨气 B. 锌和稀硫酸生成氢气
C. 二氧化锰和浓盐酸生成氯气 D. 碳酸钙和稀盐酸生成二氧化碳
8. 若溶液中由水电离产生的![]() ,满足此条件的溶液一定可以大量共存的离子的是
,满足此条件的溶液一定可以大量共存的离子的是
A. ![]() 、
、![]() 、
、![]() 、
、![]() B.
B. ![]() 、
、![]() 、
、![]() 、
、![]()
C. ![]() 、
、![]() 、
、![]() 、
、![]() D.
D. ![]() 、
、![]() 、
、![]() 、
、![]()
9. 下列离子方程式中,正确的是
A. 铜片投入稀硝酸中:![]()
B. 铝片溶于氢氧化钠溶液:![]()
C. 氨气通入醋酸溶液中:![]()
D. 碳酸氢钠的水解:![]()
10. 在一定的温度和压强下,在可变容器中,反应![]()
![]()
![]() 达到平衡后,再后容器中通入一定量的
达到平衡后,再后容器中通入一定量的![]() ,又达到平衡,
,又达到平衡,![]() 的体积分数
的体积分数
A. 增大 B. 减小 C. 不变 D. 无法判断
11. 室温时,向体积均为![]() 的盐酸中分别加入
的盐酸中分别加入![]() 金属M,反应完毕后再分别加入
金属M,反应完毕后再分别加入![]() 金属N。则两次共加入金属的全过程中,放出气体最多的是
金属N。则两次共加入金属的全过程中,放出气体最多的是
|
| A | B | C | D |
| 第一次加入M |
|
|
|
|
| 第二次加入N |
|
|
|
|
12. 向![]() 、
、![]() 、
、![]() 混合液中,通入过量
混合液中,通入过量![]() 后,溶液蒸干并充分灼烧,得到固体剩余物的组成一定是
后,溶液蒸干并充分灼烧,得到固体剩余物的组成一定是
A. ![]() 、
、![]() 、
、![]() B.
B. ![]() 、
、![]() 、
、![]()
C. ![]() 、
、![]() 、
、![]() D.
D. ![]() 、
、![]()
13.“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用。下列化学反应不符合“绿色化学”概念的是
A. 制![]()
![]()
![]()
B. 制![]()
![]()
C. 消除硫酸厂尾气排放:![]()
D. 消除硝酸厂尾气排放:![]()
14. 在同温同压下,下列各组热化学方程式中,![]()
![]() 的是
的是
A. ![]() ;
;![]()
![]() ;
;![]()
B. ![]() ;
;![]()
![]() ;
;![]()
C. ![]() ;
;![]()
![]() ;
;![]()
D. ![]() ;
;![]()
![]() ;
;![]()
15. 将![]() 溶液加水稀释或加入少量的
溶液加水稀释或加入少量的![]() 晶体时,都会引起
晶体时,都会引起
A. 溶液的pH增加
B. 溶液中的![]() 增大
增大
C. 溶液的导电能力减弱
D. 溶液中的![]() 减小
减小
16. 用![]()
![]() 和
和![]()
![]() 的混合物配成
的混合物配成![]() 溶液,已知该溶液pH = 4.7,则下列判断正确的是
溶液,已知该溶液pH = 4.7,则下列判断正确的是
A. ![]() 的电离程度小于
的电离程度小于![]() 的水解程度
的水解程度
B. ![]() 的存在对
的存在对![]() 的水解有促进作用
的水解有促进作用
C. ![]()
D. ![]()
17. X、Y、Z三种主族元素位于同一周期表中连续的三个不同周期,原子序数:![]() ,其中Y原子的次外层电子数为2,X的次外层电子数与Y、Z原子的次外层电子数均不相同,X与Y的族序数之和等于Z的族序数。已知X的氢氧化物难溶于水;Y的最高价氧化物的水化物是一种强酸。由此推出X、Y、Z依次是
,其中Y原子的次外层电子数为2,X的次外层电子数与Y、Z原子的次外层电子数均不相同,X与Y的族序数之和等于Z的族序数。已知X的氢氧化物难溶于水;Y的最高价氧化物的水化物是一种强酸。由此推出X、Y、Z依次是
A. ![]() 、
、![]() 、
、![]() B.
B. ![]() 、
、![]() 、
、![]()
C. ![]() 、
、![]() 、
、![]() D.
D. ![]() 、
、![]() 、
、![]()
18. ![]() 的
的![]() 溶液,恰好与
溶液,恰好与![]()
![]() 的
的![]() ,溶液完全反应,则元素
,溶液完全反应,则元素![]() 在还原产物中的化合价是
在还原产物中的化合价是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
第Ⅱ卷(非选择题 共59分)
二. 实验题(包括2小题,共21分)
19.(7分)下面几位学生在实验室做探究性实验,请根据要求回答下列问题。
(1)甲学生在一个月内共需要![]() 的
的![]() 溶液,现在该学生要在实验室进行配制并保存该溶液。甲学生开列的实验用品为:蒸馏水、烧杯、托盘天平(带砝码)、玻璃棒和试剂瓶,还缺少的必要仪器和药品是
。
溶液,现在该学生要在实验室进行配制并保存该溶液。甲学生开列的实验用品为:蒸馏水、烧杯、托盘天平(带砝码)、玻璃棒和试剂瓶,还缺少的必要仪器和药品是
。
(2)乙同学想用实验证明高锰酸钾溶液的紫红色是的![]() 颜色,而不是
颜色,而不是![]() 的颜色。他设计的实验步骤如下:
的颜色。他设计的实验步骤如下:
A. 将高锰酸钾晶体加热分解,所得固体质量减少
B. 观察氯化钾溶液没有颜色,表明溶液中![]() 无色
无色
C. 在高锰酸钾溶液中加入适量的锌粉振荡,静置后见紫红色褪去,表明![]() 为紫红色。你认为上述实验步骤没有意义的是
(填序号)。
为紫红色。你认为上述实验步骤没有意义的是
(填序号)。
(3)丙学生为了将![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 组成的固体混合物逐个溶解而分离,分别选用了五种试剂
① 水 ② 氢氧化钠 ③ 氨水 ④ 盐酸 ⑤ 二氧化碳,然后按编号顺序依次进行了实验。
组成的固体混合物逐个溶解而分离,分别选用了五种试剂
① 水 ② 氢氧化钠 ③ 氨水 ④ 盐酸 ⑤ 二氧化碳,然后按编号顺序依次进行了实验。
你若做上述分离实验,请将你选用的试剂及使用试剂顺序依次写出(可用丙学生已选中的,也可以重新选择)。 。
20.(14分)根据下列叙述的实验装置和操作,回答有关问题。
(1)按图M所示装置,用两种不同操作分别进行实验。
① 先夹紧止水夹a,再使A管开始反应,实验中B中观察到的现象是 。
B中发生反应的离子方程式(或化学方程式)是 。
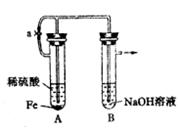
图M
② 打开止水夹a,使A管开始反应一段时间后再夹紧止水夹a,实验中在B观察到的现象是 。
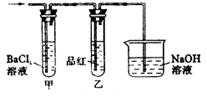
图N
(2)上述装置的实验结束后,取A管内反应所得溶液,隔绝空气小心蒸干后,再高温煅烧(有关装置及操作已略去),最后留下红色固体。将分解时产生的气体按右上图N所示装置依次通过洗气装置,结果甲内出现白色沉淀,乙内溶液红色褪去,试回答:
① 用化学方程式说明试管甲产生白色沉淀的原因(用方程式表示) 。
② 根据实验现象,写出图M中A内溶液蒸干后,在高温灼烧分解时发生的化学方程式 ,该反应的氧化剂是 ,氧化产物是 。
三. 填空题(本题包括4小题,共28分。)
21.(3分)白磷(![]() )在空气中充分燃烧生成一种粉末状的氧化物,该氧化物与水化合生成磷酸。已知
)在空气中充分燃烧生成一种粉末状的氧化物,该氧化物与水化合生成磷酸。已知![]() 该氧化物与水完全反应生成
该氧化物与水完全反应生成![]() 磷酸。
磷酸。![]() 白磷完全燃烧放出
白磷完全燃烧放出![]() 的热量。该白磷燃烧的热化学方程式为
。
的热量。该白磷燃烧的热化学方程式为
。
22.(8分)在100℃时,将![]() 的
的![]() 气体充入
气体充入![]() 抽空的密闭容器中,隔一定时间,对该容器内的物质进行分析,得到如下数据
抽空的密闭容器中,隔一定时间,对该容器内的物质进行分析,得到如下数据
|
| 0 | 20 | 40 | 60 | 80 | 100 |
|
| 0.100 |
| 0.050 |
|
|
|
|
| 0.000 | 0.060 |
| 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应的化学方程式:
。达到平衡时,![]() 的转化率为
的转化率为
%,表中![]() 、
、![]() 、
、![]() 、
、![]() 之间的关系
(选填“>”“<”或“=”)。
之间的关系
(选填“>”“<”或“=”)。
(2)若在相同情况下,最初向该容器充入的是![]() 气体,要达到上述同样的平衡状态,
气体,要达到上述同样的平衡状态,![]() 的起始浓度是
的起始浓度是
![]() 。
。
23.(8分)有A、B、C、D四种单质,在一定条件下,A、B、C分别与D发生化合反应相应地生成X、Y、Z(X、Y、Z每个分子中都含有10个电子),而B和C发生化合反应生成W,另外又知这些单质和化合物之间发生如下反应:
① ![]() ②
② ![]()
![]()
③ ![]()
![]()
试回答下列问题:
(1)单质D的化学式是 ;
(2)反应①②③的化学方程式是:
①
②
③
24.(9分)新型高能钠硫电池以熔融的钠、硫为电极,以钠离子导电的陶瓷为固体电解质。该电池放电时为原电池,充电时为电解池,反应原理为:
![]()
![]()
![]()
(1)放电时![]() 发生 反应,
发生 反应,![]() 作
极。
作
极。
(2)充电时![]() 所在电极与直流电源 极相连。
所在电极与直流电源 极相连。
(3)放电时负极反应为 ;
充电时阳极反应为 。
(4)用此电池作电源电解饱和![]() 溶液,当阳极产生
溶液,当阳极产生![]() (标准状况)气体时,消耗金属
(标准状况)气体时,消耗金属![]() 的质量为
。
的质量为
。
四. 计算题(本题包括2小题,共10分)
25.(2分)实验室用![]() 还原
还原![]()
![]() ,当大部分固体变红时,停止加热。冷却后,称得剩余固体的质量为
,当大部分固体变红时,停止加热。冷却后,称得剩余固体的质量为![]() 。当用去
。当用去![]() 时,生成水的质量是
时,生成水的质量是 ![]() 。
。
26.(8分)在密闭容器中,将碳酸氢钠和过氧化钠混合粉末加热到250℃,使其充分反应,最后测得残余固体由两种化合物组成,分别为![]() 和
和![]() ,且
,且![]() ,试通过计算回答:
,试通过计算回答:
(1)原混合物中碳酸氢钠物质的量为 ,过氧化钠物质的量为 。
(2)反应后容器内气体物质及其物质的量: , , , , ,
(可不填满,也可补充)。

【试题答案】
一.(第1~13小题,每题2分,第14~18小题,每题3分,共41分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | B | D | A | B | C | A | B | C | C | C | A | D | B | C | A | D | B | B |
二. 实验题(共21分)
19.(7分)
(1)药匙;![]() 容量瓶;氯化钠;胶头滴管 2分
容量瓶;氯化钠;胶头滴管 2分
(2)A 2分
(3)①③②⑤④(其它合理答案均给分) 3分
20.(14分)
(1)
① 液面上升,并出现白色沉淀,然后沉淀迅速变为灰绿色,最后变为红褐色。 2分
![]() 2分
2分
![]() 2分
2分
② 打开止水夹时,溶液中的导管有气体泡出,夹紧止水夹后出现白色沉淀,
一段时间内不变色。 2分
(2)
① ![]() 2分
2分
② ![]()
![]() 2分
2分
![]()
![]() 各1分,共2分
各1分,共2分
三. 填空题(共28分)
21.(3分)![]() ;
;![]() 3分
3分
22.(8分)
(1)![]()
![]()
![]() 2分
2分
60 ![]() 各2分,共4分
各2分,共4分
(2)0.200 2分
23.(8分)
(1)![]() 2分
2分
(2)① ![]() 2分
2分
② ![]()
![]() 2分
2分
③ ![]()
![]() 2分
2分
24.(9分)
(1)氧化;正 各1分,共2分
(2)负 1分
(3)![]()
![]() (或
(或![]() )
各2分,共4分
)
各2分,共4分
(4)69 2分
四. 计算题(共10分)
25.(2分)
![]() 2分
2分
26.(8分)
(1)![]() ;
;![]() 各2分,共4分
各2分,共4分
(2)![]() ;
;![]() ;
;![]() ;
;![]() 各1分,共4分
各1分,共4分
解析:![]() 和
和![]() 的反应可分为以下几种情况:
的反应可分为以下几种情况:
(1)![]() 时(
时(![]() 适量)剩余固体:
适量)剩余固体:![]()
(2)![]() 过量但比值
过量但比值![]() 时剩余固体:
时剩余固体:![]() 和
和![]()
(3)![]() 过量 剩余固体:
过量 剩余固体:![]()
题目所指应为第2种情况,又因为![]() 过量,所以
过量,所以![]() 应为
应为![]() ,
,![]() 应为
应为![]() 。
。
![]()
![]() ――
―― ![]()
又根据“![]() ”守恒:
”守恒:
![]()
又根据“![]() ”守恒:
”守恒: ![]()
“![]() ”守恒 ∴ 生成
”守恒 ∴ 生成![]() 为
为![]() 生成
生成![]() 为
为![]()
【试卷分析】
本次考试是河西区高三统一考试。试题题量不大,共26题,1小时30分钟,满分100分。
考试试题难度不大,知识覆盖了《元素化合物》《基本理论》《化学实验》等部分内容,对一些重点内容进行了深入的挖掘。预计得分应在70―85之间。
| 年级 | 高三 | 学科 | 化学 | 版本 | 人教大开本、3+x | 期数 | |||||||
| 内容标题 | 第一学期高三化学期末考试
| ||||||||||||
| 分类索引号 | G.624.6 | 分类索引描述 | 考试试题与题解 | ||||||||||
| 主题词 | 天津河西区2003―2004学年度第一学期高三化学期末考试 | 栏目名称 | 名校题库 | ||||||||||
| 供稿老师 | 王岭 | 审稿老师 | |||||||||||
| 录入 | 一校 | 二校 | 审核 | ||||||||||