高三化学基础测试6
-、选择题
1.下列试纸在使用时,不能用水润湿的是( )
A. 红色石蕊试纸
B. 蓝色石蕊试纸
C. 淀粉碘化钾试纸
D. 广范pH试纸
2.下列操作正确的是( )
A.滴定管用蒸馏水洗净后,用所装溶液润洗再装液
B.锥形瓶用蒸馏水洗净后,再用待测液润洗后装一定量的待测液
C.滴定过程中,眼睛注视着滴定管内液面位置的变化
D.滴定过程中,眼睛注视着锥形瓶内溶液颜色的变化
3.有以下四组物质:
①FeCl2、A1(N03)3、MgSO4、NH4N03四种溶液;
③Mn02、FeS、Cu0、C四种黑色固体;
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液;其中只用一种试剂(允许加热)就能将组内物质区别开的是( )
A. 只有①③
B. 只有①②③
C. 只有①③④
D. 全部
4.某同学用托盘天平称量固体药品时,称量前指针未调零点,称量时样品放置天平的左盘。天平平衡时用了10g砝码,游码指示0.5 g,则药品的真实质量是( )
A. >10.5 g
B. <10.5 g
C. =10.5 g
D. 无法确定
5.下列各组稀溶液,不用其他试剂或试纸,仅利用溶液间的相互反应,就可以将它们区别开的是( )
A. 硝酸钾 硫酸钠 氯化铜 氯化钡
B. 硫酸 硫酸铝 氯化钠 氢氧化钠
C. 氯化钡 硫酸钠 碳酸钠 氢氧化钠
D. 硫酸镁 碳酸钠 硫酸氢钠 氢氧化钠
6.下列实验不能达到目的的是
A.向FeCl2溶液中滴入KSCN溶液,检验FeCl2是否氧化变质
B.淀粉水解后的溶液中加新制Cu(OH)2,加热,检验淀粉是否水解完全
C.混有乙酸和乙醇的乙酸乙酯用Na2C03溶液除杂提纯
D.用分别溶于水的方法鉴别溴蒸气和N02气体
7.下列试剂可用带胶塞的无色试剂瓶保存的是( )
A.纯碱溶液
B.液溴
C.氢氟酸
D.硝酸银溶液
8.由于易被氧化而不宜长期存放的是 ( )
①KMn04②H2S溶液③FeS04溶液④Cu(N03)2溶液⑤Na2SO3溶液
A.只有①②③
B.只有②③⑤
C.只有②④
D.只有①⑤
9.下列中的“黄色”不属于因化学反应而产生的现象是( )
A.无色试剂瓶中的浓硝酸呈黄色
B.用玻璃片靠近在玻璃导管口燃着的硫化氢的火焰,玻璃片附有的固体呈黄色
C.久置的碘化钾溶液呈黄色
D.单质硫置于水中振荡后静置,沉淀物呈淡黄色
10.在实验中,为防止下列情况发生,采取的措施错误的是( )
A.制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片
B.在用系列实验装置制取![]() 和检验
和检验![]() 的实验中,尾气污染空气,应用水吸收尾气
的实验中,尾气污染空气,应用水吸收尾气
C.用加热![]() 的方法制得的氧气中带有紫色,应在靠近试管口地方放一团棉花
的方法制得的氧气中带有紫色,应在靠近试管口地方放一团棉花
D.用电石制乙炔,产生气体的速率过快,应逐滴滴入饱和食盐水
11.在5支编号的试管里分别装有K2CO3、KNO3、K2SO4 、KOH、和Ba(OH)2溶液,现需要用最少种类的试剂将它们一一区别开来,则所需试剂的种类是( )
A. 用1种试剂
B. 用2种试剂
C. 用3种试剂
D. 不用任何试剂
12.下列各组混合物的分离或提纯方法不正确的是( )
A.用渗析法分离![]() 胶体和
胶体和![]() 溶液的混合物
溶液的混合物
B.用结晶法提纯NaCl和KNO3混合物中的KNO3
C.有蒸馏法分离乙醇和苯酚的混合物
D.用加热法分离碘和氯化铵的混合物
13. 下列叙述正确的是( )
A.用水吸收Cl2或NH3制得水溶液时,所用吸收装置完全相同
B.实验室制取Cl2或HCl气体时,可以用相同的气体发生装置
C. 氢氟酸密封在玻璃试剂瓶中
D.存放烧碱溶液或溴水时,均可用橡胶塞密封
14.下列实验不能获得成功的是( )
A.用浓溴水除去苯中混有的苯酚杂质
B.淀粉与稀硫酸充分反应后,加入适量新制氢氧化铜浊液,加热产生红色沉淀
C.只用一种试剂鉴别Na2S溶液、NaCl溶液、Na2SiO3溶液、Na2S2O3溶液
D.用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸杂质
二、填空题
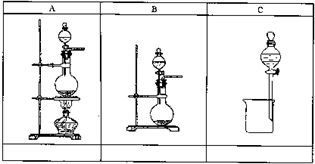 |
1.A、B、C是中学化学实验中常见的几种使用分液漏斗的装置图。
(1)请从①~⑩中选出必须使用分液漏斗的实验,把编号填入最适宜的装置图A~C下面的空格中(多选要倒扣分):
①酒精和浓硫酸混合加热制乙烯 ②浓盐酸和二氧化锰混合加热制氯气
③分离苯和硝基苯的混合物 ④用氯化钠和浓硫酸加热制取氯化氢
⑤浓硫酸跟亚硫酸钠制二氧化硫 ⑥用浓硝酸跟铜反应制二氧化氮
⑦用饱和亚硝酸钠溶液跟饱和氯化铵溶液共热制氮气 ⑧用电石跟水反应制乙炔
⑨分离乙酸和乙醇的混合物 ⑩从溴水中用苯提取溴单质
(2)上述装置中,真正起到分液作用的是_________(填A或B或C)。可应用于两种___________物质的分离。
2.下图为常用玻璃仪器组成的七种实验装置,根据需要可在其中加入液体或固体试剂。请选择适宜装置的序号填于空白处(多选、漏选或错选均扣分)。
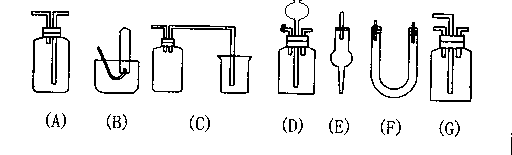
(1)既能用于收集 02又能用于收集 NO的装置是
(2)能用作干燥C02气流的装置是 。
(3)能用于实验室制取Cl2并检验中Cl2性质的连续实验中,除去Cl2中的HCl杂质的最佳装置是 。
(4)合成NH3实验中,可用于干燥、混合并能观察H2和N2的体积比的装置是 。
(5)接在气体的连续实验中间,用于达到控制气流使其平稳目的的装置是 。
(6)用于尾气吸收并能防止液体倒吸到其他装置中的是 。
3.可用于分离或提纯物质的方法有:A.分馏 B.盐析 C.过滤 D.重结晶 E.升华F.渗析 G.电解 H.加热分解I.蒸馏 下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(把选用的方法的标号填人括号内)
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒。( )
(2)除去Fe(OH)3胶体中混有的Cl-离子。( )
(3)除去乙醇中溶解的微量食盐。( )
(4)分离石油中各种不同沸点范围的成分。( )
(5)除去固体碘中混有的少量碘化钠。( )
(6)除去氧化钙中的碳酸钙。( )
4.下列操作不正确的是____________
A.用氨水清洗做过银镜反应的试管
B.用酒精清洗有硫沉淀的试管
C.将金属锂放在煤油中保存
D.苯中溶有苯酚的杂质,可向其中加入适量的浓溴水,然后过滤除去苯酚
E.用分液漏斗分离乙醛和水的混合物
F.制硅酸溶胶时,先往试管中装入5-10mL1mol/L的盐酸,再加入1mL水玻璃,然后用力振荡
三、实验题
1.下列是自制电源并电解饱和食盐水实验。所需仪器如下图,所选用的实验用品还有食盐、硫酸铜溶液、酚酞溶液、蒸馏水、烧杯、玻璃棒,内层附有浓NaOH的气球等。电解时,要求电解器右管附近溶液出现红色,回答下列问题。
 |
(1)补充下列实验步骤,直至反应开始进行。
①配制饱和食盐水,并滴2~3滴酚酞;
②安装电解装置:将___________ 电极胶塞插入电解器左管, 电极胶塞插入右管,从漏斗中注入食盐水至充满两管后再分别关闭活塞;
③安装电源装置:将适量CuSO4溶液注入U形管中,并插入铁棒和铜棒,组装为一个原电池,然后将多个原电池进行串联;
④连接电源与电解装置:将连接Pt片的导线与电源的 棒相连,连接铁片的导线与电源的______棒相连。
(2)电解时,U形管中可观察到的现象有_____________ ;如果Ag 棒代替铁棒(其它不变),由于不能再作电源,电解立即停止,其原因是:_____________;
(3)当右管附近出现红色时可停止电解,此区域出红色的原因是:____________;
(4)实验完毕撤去装置时必须处理有毒的Cl2,其简单操作方法______________________。
2.实验装置如图:
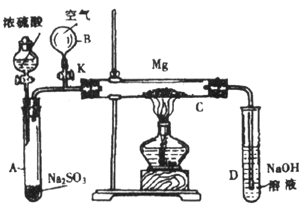
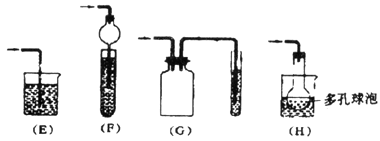
先关闭K,使A中反应进行,加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质。实验完成后将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。请回答:
(1)C中全部产物有 , , ;
(2)本实验先使A中反应进行,再加热C装置,其目的是 ;
(3)停止实验时,先打开K,再停止滴加浓硫酸,熄灭酒精灯,橡胶气胆B在实验中的作用是 ;
(4)若无装置B、K使用普通导管,本实验的尾气吸收装置可以选用图中 装置;(填写序号,多选扣分)
(5)C中的Mg应放在不锈钢垫片上而不能直接接触管壁的原因 。
1. 氯磺酸是无色液体,密度1.79 g/cm3,沸点约152 ℃。氯磺酸有强腐蚀性,遇湿空气发出强烈的白色烟雾,它属于危险品,制取氯磺酸的典型反应是在常温下进行:
HCl(g)+SO3=HSO3Cl
在实验室里制取氯磺酸可用下列仪器装置(下图中铁夹、固定仪器等已略去)。
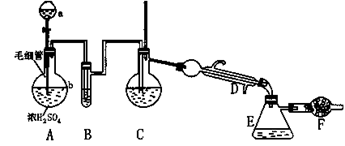
用到的试剂、药品有:①密度1.19 g/cm3浓盐酸;②密度1.84 g/cm3、质量分数为98.3%的浓硫酸;③发烟硫酸;④无水氯化钙;⑤水。制备时要在常温下使干燥的氯化氢气体和三氧化硫反应,至不再吸收HCl时表示氯磺酸已大量制得。其后在干燥HCl气体中将氯磺酸分离出来。
(1)仪器中应盛入的试剂与药品(填序号):A的a____________ ,B ___________ ,C_______ ,F________________ 。
(2)A的分液漏斗下边接有的毛细管是重要部件。在发生气体前要把其灌满a中液体,在发生气体时要不断的均匀地放出液体,这是因为__________________________
(3)实验过程中何时需要加热_________________________________ ,应在哪件装置下用酒精灯加热(填代码字母)________________。
(4)若不加F装置可能发生的现象_________________,有关反应的化学方程式为_____________。
(5)在 F之后还应加什么装置______________,其作用是________________________
4.实验室用干燥、纯净的![]() 与熔融的Sn反应制SnCl4:
Sn+2Cl2SnCl4同时放大量的热,已知
与熔融的Sn反应制SnCl4:
Sn+2Cl2SnCl4同时放大量的热,已知![]() 常温下是无色液体,沸点:114 ℃,遇潮湿空气便发生水解反应,产生白色烟雾。Sn的熔点:231 ℃,下图是制取
常温下是无色液体,沸点:114 ℃,遇潮湿空气便发生水解反应,产生白色烟雾。Sn的熔点:231 ℃,下图是制取![]() 的实验装置
的实验装置
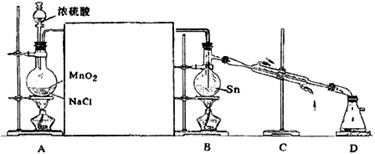
试回答以下问题:
(1)装置A中反应的化学方程式 。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内,并注明其中盛放的药品。
(3)进行实验时,应先点燃(填写字母,下同)
处的酒精灯,当反应生成![]() 时,应熄灭
处的酒精灯,理由是
。
时,应熄灭
处的酒精灯,理由是
。
(4)装置C的作用是 。
(5)进行此实验,D装置后应当连接的装置及作用是(按从左到右的顺序写出仪器名称及其中的药品) 。
参考答案
-、选择题
1.D 2.A、D 3.D 4.D 5.B、D
6.B 7. A 8.B 9.D 10. B
11.可以选用硫酸铝溶液,用硫酸铝溶液分别与上述溶液反应,有无色气体和白色沉淀产生的原溶液是碳酸钾,有白色沉淀产生且白色沉淀消失的原溶液是氢氧化钾,只有白色沉淀产生的原溶液是氢氧化钡溶液,利用鉴别出来的氢氧化钡溶液加入到剩余的两种液体中,产生白色沉淀的原溶液是硫酸钾,没有现象的是硝酸钾。也可以使用一种试剂如酚酞指示剂。答案:A
12.D 13.B 14.A、B
二、填空题
1. (1)
| 2,4,7 | 5,6,8 | 10 |
(2)C;互不相溶
2. (1)A、B (2)A、E、F (3)A (4)G (5)D (6)C
3. (1)C (2)F (3)I (4)A (5)E (6)H
4. A、B、D、E
三、实验题
1.(1)②Pt、Fe 或Cu、Fe ④(2)铁棒变细,铜棒加厚,溶液颜色变浅,Ag与Cu均不能与Cu2+反应,不能形成有功率的电池(3)由于H+放电使水的电离平衡破坏,导致[OH-]>[H+]溶液显碱性(4)在左管尖嘴处套上沾有浓NaOH溶液的气球,开启活塞,通过静水压将气体排尽,
2.(1)S、MgO、MgS
(2)排净空气(防止Mg和![]() 、
、![]() 反应)
反应)
(3)防止倒吸
(4)F、G、H
(5)防止Mg和玻璃中的![]() 反应
反应
3.(1) ①②③④
(2) 用以保证密度比浓H2SO4小的浓盐酸能顺利流到浓H2SO4底部,不致使酸液飞溅,且顺利产生HCl气。
(3) C中发烟H2SO4不再吸收HCl气体时,表示已生成足量氯磺酸,此时在其下加热以蒸出沸点比浓H2SO4低的氯磺酸。;C
(4)出现大量白雾;HSO3Cl+H20——H2SO4+HCl
(5)尾气的吸收装置(1分);防止HCl逸入空气造成污染
4.(1)2NaCl+3H2SO4+MnO22NaHSO4+Cl2↑+MnSO4+2H2O
(2)
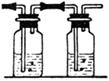
(饱和食盐水)(浓硫酸)
(只要合理,其他装置也可)
(3)B、B 依靠反应热维持Sn的熔化。
(4)使![]() 蒸气冷凝
蒸气冷凝
(5)连接干燥管,装有碱石灰,防止水蒸气进入锥形瓶使![]() 发生水解。 连接
发生水解。 连接![]() 的尾气吸收装置,装有NaOH溶液,吸收
的尾气吸收装置,装有NaOH溶液,吸收![]() ,保护环境。 (或连接干燥管,装有碱石灰,防止空气中水蒸气进入锥形瓶,使
,保护环境。 (或连接干燥管,装有碱石灰,防止空气中水蒸气进入锥形瓶,使![]() 发生水解;吸收
发生水解;吸收![]() ,保护环境。)
,保护环境。)