高考化学复习热点-有机化学
一、选择题:(本题包括5小题,每小题3分,共15分,每小题只有一个选项符合题意.)
1、下列物质,不属于运输中易燃易爆危险品的是( )
A、三硝基甲苯 B、酚醛塑料 C、三硝基苯酚 D、乙醛
2、实验室制备下列物质时,不可用浓H2SO4参与的是( )
![]() A、由 制取硝基苯
B、用乙酸和乙醇制备乙酸乙酯
A、由 制取硝基苯
B、用乙酸和乙醇制备乙酸乙酯
C、用NaI制HI D、由乙醇制乙烯
3、下列关于乙酸乙酯的各种说法中正确的是( )
A、酯化时需要用水浴加热,才可进行
B、乙酸乙酯中含有乙酸时,可用NaOH溶液除去
C、乙酸乙酯是一种优良的溶剂
D、酯化反应中,酸羟基中的18O原子在产物酯中
4、下列不属于取代反应的是( )
A、由醋酸钠和碱石灰制甲烷 B、皂化反应
![]() C、由乙醇制乙醚
D、银镜反应
O
C、由乙醇制乙醚
D、银镜反应
O
![]() 5、扑热息痛是一种优良的解热镇痛药,其结构简式为HO― ―NH―C―CH3,它的性质叙述不正确的是( )
5、扑热息痛是一种优良的解热镇痛药,其结构简式为HO― ―NH―C―CH3,它的性质叙述不正确的是( )
A、常温下是白色晶体 B、难溶于NaOH溶液
C、微溶于冷水,易溶于热水 D、与FeCl3有显色作用
二、选择题:(本题包括15小题,每小题3分,共45分,每小题有一个或两个选项符合题意,若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确给1分,都正确给3分,但只要一个选错,该小题就为0分.)
阅读下面材料做6、7两小题:
![]()
![]() 实验室制乙烯时,反应如下:CH3CH2OH 浓H2SO4 CH2=CH2↑+H2O,浓H2SO4的作用是催化剂、吸水剂,做催化剂时,先与乙醇反应,生成两种产物,其中含有碳原子的物质在高温条件下再生成硫酸,同时生成乙烯.
实验室制乙烯时,反应如下:CH3CH2OH 浓H2SO4 CH2=CH2↑+H2O,浓H2SO4的作用是催化剂、吸水剂,做催化剂时,先与乙醇反应,生成两种产物,其中含有碳原子的物质在高温条件下再生成硫酸,同时生成乙烯.
6、浓H2SO4和乙醇反应所得含有碳原子的物质是( )
A、醇 B、醛 C、酯 D、醚
7、生成硫酸和乙烯的反应是( )
A、复分解反应 B、取代反应 C、酯化反应 D、消去反应
8、同温同压下,由A、B两有机物组成的混合气体中,无论A、B物质的量之比如何改变,完全燃烧n mol该混合物时,耗氧量保持不变的是( )
A、C2H4、C2H4O B、C2H6、C3H8
![]()
![]() O
O
O
O
C、CH![]() CH、CH3CH
D、HCH、C6H12O6
CH、CH3CH
D、HCH、C6H12O6
9、充分燃烧有机物A 0.002mol,用去O2 0.48g,若将燃烧所得气体导入过量澄清石灰水中,得沉淀1.4g,则A的分子式为( )
A、C7H8O2 B、C7H6O2 C、C7H6O D、C4H8O
10、能被皮肤吸收,并具有毒性的物质是( )
![]()
![]()
![]() A、CH3OH B、 ―OH C、 ―NO2 D、 ―COOH
A、CH3OH B、 ―OH C、 ―NO2 D、 ―COOH
![]() 11、对于碱性而言:NaOH>Na2CO3>Na―O―
>NaHCO3,下列各组在溶液中不能共存的是( )
11、对于碱性而言:NaOH>Na2CO3>Na―O―
>NaHCO3,下列各组在溶液中不能共存的是( )
![]() A、NaOH和NaHCO3 B、Na2CO3和 ―OH
A、NaOH和NaHCO3 B、Na2CO3和 ―OH
![]() C、Na2CO3和NaHCO3
D、NaOH和 ―ONa
C、Na2CO3和NaHCO3
D、NaOH和 ―ONa
12、某有机物的分子式为C3H8O3,其中3个碳原子以C―C单键相连,关于其性质描述,正确的是( )
A、只含该有机物的液体,可做抗冻剂
B、通常该有机物是一种液体,且易溶于水、乙醇、乙醚
C、该有机物可用于合成治疗心血管病的药品
D、该有机物可与NaOH发生不可逆水解反应
13、下列各组,可用一种试剂鉴别的是( )
A、淀粉溶液、乙醇、苯、四氯化碳 B、乙烯、乙烷、乙炔、乙酸
C、甲酸、乙醛、甲酸乙酯、乙酸乙酯 D、苯酚、苯乙烯、甲苯、乙苯
14、下列体系经反应后,PH值降低的是( )
A、SCN-加到Fe3+中
B、由NH3・H2O、AgNO3配制银氨溶液
![]() C、Fe3+与 ―OH显色
C、Fe3+与 ―OH显色
![]() D、在 ―OH中滴加溴水产生白色沉淀
D、在 ―OH中滴加溴水产生白色沉淀
15、下列物质与Na2O2放置在一起较长时间后,颜色发生变化的有( )
![]() O
O
![]() A、Na2SO3 B、FeCl2
C、 ―OH D、HCH
A、Na2SO3 B、FeCl2
C、 ―OH D、HCH
16、制备乙醛通常有三种方法:
(1)发酵法:粮食在一定条件下发酵成乙醇,再由乙醇氧化为乙醛
HgSO4
(2)![]()
![]() 乙炔水化法:CH
乙炔水化法:CH![]() CH+H2O CH3CHO
CH+H2O CH3CHO
加温、加压
催化剂
(3)乙烯氧化法:2CH2=CH2+O2 2CH3CHO
加温、加压
下列对于这三种合成方法的评价正确、客观的是( )
A、发酵法只涉及氧化一步反应,但要浪费大量粮食
B、乙炔水化法中,催化剂毒性大、成本低、但副反应少
C、乙烯氧化法成本低、反应快、产率高,被当今工业普遍采用
D、乙炔水化法本质是加成反应,生成醛的产率较低
17、下列有机物中不可能存在的是( )
A、乙二酸二乙酯 B、二乙酸乙二酯
C、二乙酸二乙酯 D、乙二酸乙二酯
![]()
![]() 18、1mol的HO― ―CH2―O―CH=CH2可与( )mol的溴水反应
18、1mol的HO― ―CH2―O―CH=CH2可与( )mol的溴水反应
CH2―CH=CH2
A、3 B、4 C、5 D、6
![]() 19、3.26g液态酯CnH2n+1C―OCH2CnH2n+1,用25.0ml, 2mol/L NaOH溶液进行回流,
O
19、3.26g液态酯CnH2n+1C―OCH2CnH2n+1,用25.0ml, 2mol/L NaOH溶液进行回流,
O
溶液回流后,为完全中和,需用盐酸26.0ml,0.5mol・L-1,则n的值是( )
A、0 B、1 C、2 D、3
20、下列说法正确且解释合理的是( )
A、苯酚跟碳酸氢钠溶液反应放出二氧化碳,这是因为苯酚的酸性强于碳酸
B、乙二醇和丙三醇都属于醇类,这是因为它们互为同系物
![]()
![]() C、1mol HC―H和1mol CHO都能和4mol Cu(OH)2发生反应,这是因为它们都可
O
CHO
C、1mol HC―H和1mol CHO都能和4mol Cu(OH)2发生反应,这是因为它们都可
O
CHO
以得到2mol氧原子
D、乙酸和丙醇互为同分异构体,这是因为它们的分子量相等
三、选择题:(本题包括5小题,每小题4分,共20分,每小题只有一个选项符合题意.)
21、能用前面两种物质在一定条件下经一步反应制备第三种物质的是( )
![]()
![]() A、 ,H2O, ―OH
B、S、O2、SO3
A、 ,H2O, ―OH
B、S、O2、SO3
![]()
![]() C、CH2=CH2,Cl2, CH2=CH―Cl
D、 ―COONa,碱石灰,
C、CH2=CH2,Cl2, CH2=CH―Cl
D、 ―COONa,碱石灰,
22、乙二酸,又称草酸,通常在空气中易被氧化变质,而其两分子结晶水(H2C2O4・2H2O)却能在空气中稳定存在.在分析化学中常用H2C2O4・2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是( )
A、草酸是二元强酸,其电离方程式为H2C2O4=2H++C2O42-
B、草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C、乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D、将乙二酸滴加到浓H2SO4上使之脱水分解,分解产物是CO2和H2O
23、下列过程中涉及氧化还原反应的是( )
A、橡胶老化 B、胶体的渗析 C、制皂中的盐析 D、配制银氨溶液
24、分子式为C8H16O2的有机物A,能在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有( )
A、1种 B、2种 C、3种 D、4种
![]()
![]()
![]() 25、已知2 ―CHO+OH-→
―COO-+ ―CH2OH+H2O,关于该反应,下列说法正确的是( )
25、已知2 ―CHO+OH-→
―COO-+ ―CH2OH+H2O,关于该反应,下列说法正确的是( )
A、OH-的主要作用只是中和了酸,使反应右移,而不起催化剂的作用
B、该反应实质上是碱催化下的歧化反应
C、加入过量OH-后,产物都将转变成钠盐
D、因产物中有酸根和醇,且有碱做催化剂,所以该反应实际上是酯的水解
四、(本小题包括2小题,共18分)
26、(5分)由酒精制无水乙醇可经以下步骤:
a. 首先蒸馏,除去大部分水;
b. 在a的馏份中加入CaO并再次蒸馏制得无水酒精;
c. 在无水酒精中加入P2O5,再次蒸馏,可得无水乙醇;
(1)整套装置要严密不漏气是因为________________________________
(2)加入CaO的作用是(用化学方程式表示)_____________________
![]() O
O
(3)![]() 加入P2O5除水,生成磷酸(HO―P―OH),但同时也有副反应,试写出其中
加入P2O5除水,生成磷酸(HO―P―OH),但同时也有副反应,试写出其中
OH
![]() 一种副反应为________________________.
O
一种副反应为________________________.
O
27、(13分)某课外活动小组对甲酸(HC―OH)进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应.
(1)在甲酸进行银镜反应前,必须在其中加入一定量的________,因为________.
(2)写出甲酸进行银镜反应的化学方程式_____________________________.
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作________(写字母):
A、用洁净的试管;
B、在浓度为2%的NH3・H2O中滴入稍过量的浓度为2%的硝酸银;
C、用前几天配制好的银氨溶液;
D、在银氨溶液里加入稍过量的甲酸;
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:
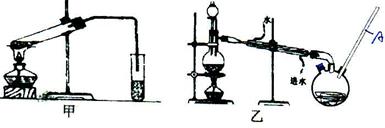 |
(4)乙装置中长导管A的作用是___________________.
(5)写出甲酸和甲醇进行酯化反应的化学方程式______________________.
(6)选择甲装置还是乙装置好?________,原因是______________________.
(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有________、
________两种必备用品.
(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释_____________________.
![]() 五、(本题包括3小题,共20分.)
OH
五、(本题包括3小题,共20分.)
OH
![]() 28、(6分)(1)有机物要达到一定的分子量才能产生沉淀,在 溶液中加入少量的溴水,看不到白色沉淀,这是因为(用化学方程表示)_____________.
28、(6分)(1)有机物要达到一定的分子量才能产生沉淀,在 溶液中加入少量的溴水,看不到白色沉淀,这是因为(用化学方程表示)_____________.
![]()
![]()
![]() (2)CH2―CH―CHO转变成CH3C=CH2需经过________、________、________
(2)CH2―CH―CHO转变成CH3C=CH2需经过________、________、________
OH CH3 CH3
(反应类型)等合理反应过程.
29、(6分)(1)通常情况下,烃的衍生物中含有氧且为气体的是_____________________.
(2)某有机物是含有C:H:O=1:1:1且C原子数在同系列中最少的,该有机物是________________.
(3)低级酯都是具有香味的液体,区别于甲酸乙酯和乙酸乙酯可用________(填试剂名).
30、(8分)(1)涤纶是一种高分子化合物,又称的确良,可用来制衣,其结构为
![]()
![]() O O
O O
![]()
![]()
![]()
![]() [C― ―C―O―CH2―CH2―O] n,制备涤纶的两种单体是CH2―OH和_________,其反应类型是____________________.
CH2―OH
[C― ―C―O―CH2―CH2―O] n,制备涤纶的两种单体是CH2―OH和_________,其反应类型是____________________.
CH2―OH
(2)乙二醇有多种脱水方式,其中之一是两个分子成六元环,写出反应化学方程式___________________.
六、(本题包括1题,共16分)
![]() O
O
31、醛类物质R―C―H可与HCN发生加成反应:
![]()
![]() O
OH
O
OH
R―C―H+HCN→R―CH―CN
所得产物中含有―CN,它在酸性条件下可发生水解反应:
![]()
![]() OH
OH
OH
OH
R―CH―CN+2H2O![]() R―CH―COO-+NH4+
R―CH―COO-+NH4+
A、B都是烃类化合物,A中碳原子数是B中的2倍,且C可发生银镜反应,F为环状物:
H2O HCl+NaCN HCl 浓H2SO4
![]()
![]()
![]()
![]()
![]() B
C
D E F
B
C
D E F
![]()
![]() 催化剂、加温加压
△
催化剂、加温加压
△
O2 催化剂
O3
![]() A
G
A
G
催化剂、加温加压 △
浓H2SO4
H
根据以上信息,回答下列问题:
(1)写出下列物质的结构简式A________ B________ C________ D ________
E________ F ________ G ________H ________
(1)写出下列过程的方程式:
a.由A→G _________________________________________
b.由C→D ____________________________________________
c.由E→F __________________________________________
d. 由G+E→H_______________________________________
七、(本题包括2小题,共14分)
32、分子中碳原子数相邻的两种饱和一元羧酸混合物1.0g,经加水稀释后与
1mol・L-1的NaOH溶液20ml正好中和,试求混合酸的组成,写出它们的结构简式与质量分数.
33、常温下由烷烃A和单稀烃B组成的混合气体,已知(a)将1L混合气体充分燃烧,在同条件下得到2.5L CO2气体;(b)B分子中碳原子数比A分子多,且最多为4个.
(1)求A、B所有可能的组合及体积比
| 可能组合 | 体积比 | |
| A | B | |
(2)1200C时取1L该混合气与9LO2混和充分燃烧,当恢复到1200C和燃烧前的
压强时,体积增大6.25%,试通过计算确定A和B的分子式.
【有机化学单元检测答案】
一、二、三、选择题:
1、B 2、C 3、C 4、D 5、B 6、C 7、D 8、C 9、B 10、BC
11、AB 12、BC 13、AC 14、CD 15、BC 16、C 17、C 18、B
19、C 20、C 21、D 22、C 23、A 24、B 25、B
四、26、(1)乙醇易挥发易燃烧,防止发生火灾
![]()
![]() O
O
![]() (2)吸收水份(3)HO―O―OCH2CH3
(2)吸收水份(3)HO―O―OCH2CH3
OH
27、(1)NaOH,银镜反应必须在碱性条件下进行.
O
(2)H―C―OH+2[Ag(NH3)2]++2OH-→CO2+2Ag↓+4NH3+2H2O
(3)B、C、D、E、F (4)冷凝回流甲醇,平衡内外大气压强.
![]()
![]() (5)HCOOH+CH3OH
(5)HCOOH+CH3OH![]() HCOOCH3+H2O
HCOOCH3+H2O
(6)乙,因为甲醇有毒,需密封操作.
(7)沸石,Na2CO3, (8)甲酸甲酯在在NaOH溶液中发生水解.
![]()
![]() 五、 OH OH Br
五、 OH OH Br
![]()
![]()
![]() 28(1) + Br2→ +HBr
28(1) + Br2→ +HBr
(2)消去、加成、消去
29、(1)甲醛(2)乙二醛(3)银氨溶液
![]() 30、(1)HOOC― ―COOH,缩聚
30、(1)HOOC― ―COOH,缩聚
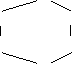 (2)2HOCH2CH2OH
(2)2HOCH2CH2OH![]()
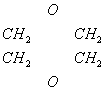 +2H2O
+2H2O
六、31、(1)A:CH3CH2CH2CH3 B、CH![]() CH C、CH3CHO
CH C、CH3CHO
![]()
![]() D、CH3CHCN
E、CH3CHCOOH
D、CH3CHCN
E、CH3CHCOOH
OH OH
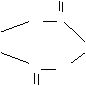 F、
F、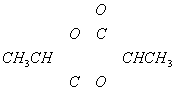 G、CH3COOH
G、CH3COOH
O
![]() O
O
![]() H、 CH3―CH―OC―CH3
H、 CH3―CH―OC―CH3
COOH
![]() (2)a: CH3CH2CH2CH3+5O2
(2)a: CH3CH2CH2CH3+5O2![]() 4CH3COOH+2H2O
4CH3COOH+2H2O
![]() b: CH3CHO+HCl+NaCN→CH3―CHCN+NaCl
b: CH3CHO+HCl+NaCN→CH3―CHCN+NaCl
OH
![]() O
O
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() c: 2CH3CHCOOH
c: 2CH3CHCOOH![]() CH3CH
CH3CH![]() CHCH3+2H2O
CHCH3+2H2O
OH O
H O
![]()
![]()
![]()
![]()
![]()
![]() d: CH3CHCOOH+CH3COOH
d: CH3CHCOOH+CH3COOH![]() CH3C―O―C CH3+H2O
CH3C―O―C CH3+H2O
OH COOH
七、32、提示:设两种羧酸的平均组成为CnH2nO2,平均摩尔质量为R.
CnH2nO2 ~ NaOH
R 1
1.0g 20mol×10-3L/m×1mol/L
R=50,
甲酸的摩尔质量为46,乙酸摩尔质量为60,46<50<60故为甲酸和乙酸的混合物.
![]() 据:
据:![]() 50
50 ![]() 故n(HCOOH):n(CH3COOH)=5:2
故n(HCOOH):n(CH3COOH)=5:2
甲酸质量分数为:![]()
乙酸的质量分数为1-65.7%=34.3%
33、(1)提示:据平均组成中含碳2.5,则A、B的可能组合和体积比为:
| A | B | 体积比 |
| CH4 | C4H8 | 1 :1 |
| CH4 | C3H6 | 1:3 |
| C2H6 | C3H6 | 1:1 |
| C2H6 | C4H8 | 3:1 |
(2)CxHy+(x+![]() )O2→xCO2+
)O2→xCO2+![]() H2O
△v
H2O
△v
1 x+![]() x
x
![]() -1
-1
1 (1+9)×6.25%
即![]() -1=10×6.25%
y=6.5
-1=10×6.25%
y=6.5
则A、B混合物平均组成为 C2.5H6.5
通过讨论:A为C2H6,B为C4H8.