高三化学选择题练习(五)
( )班级 姓名 学号 得分
一、选择题(本题共24分。有8小题,每小题3分。每小题只有一个选项符合题意)
( D )1. 下列各组物质皆由原子构成的是
①二氧化碳②碳化硅③金刚石④白磷⑤钠蒸气⑥镁单质⑦单晶硅⑧碘单质⑨石墨⑩氯化氢
A.①③⑤⑥⑦ B.②④⑥⑧⑩C.②③④⑤⑦⑧ D.②③⑤⑦⑨
( C )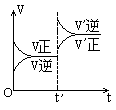 2. 对达到平衡状态的可逆反应:X+Y
2. 对达到平衡状态的可逆反应:X+Y![]() W+Z,在t'时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是
W+Z,在t'时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是
A.X、Y、W为气体,Z不是气体
B.X、Y为气体,W、Z中有一种是气体
C.W、Z为气体,X、Y中有一种是气体
D.W、Z中有一种为气体,X、Y都不是气体
( B)3. 有A、B、C、D四种一元酸的溶液,实验表明:
①物质的量浓度相同的A、C溶液中,分别滴入甲基橙试液后,A溶液呈黄色而C中不变色;②物质的量浓度相同的B、C的钠盐溶液相比较,B的钠盐溶液pH小于C的钠盐溶液pH;③A酸跟D的盐反应生成A的盐和D酸.由此可以确定四种酸的酸性由强到弱的顺序正确的是
A.BACD B.BCAD C.DACB D.CDAB
 ( B )4. 白铁(镀锌的铁)片完全溶解于盐酸后,加入过量的NaOH溶液,放置一段时间后,滤出沉淀物,将其放在氧气中灼烧,最后得到红色粉末,干燥后称重, 这些粉末的质量与原镀锌的白铁片质量相等, 又知锌是两性元素, 则原白铁片上锌的质量分数为
( B )4. 白铁(镀锌的铁)片完全溶解于盐酸后,加入过量的NaOH溶液,放置一段时间后,滤出沉淀物,将其放在氧气中灼烧,最后得到红色粉末,干燥后称重, 这些粉末的质量与原镀锌的白铁片质量相等, 又知锌是两性元素, 则原白铁片上锌的质量分数为
A.24.6% B.30% C.43.1% D.74%
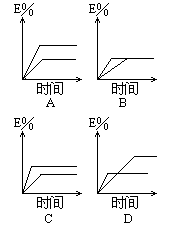
( B )5. 对可逆反应X (气)+Y (气)![]() E (气)下列四幅图
E (气)下列四幅图
中各有一条曲线(A、B、C、D)表示化学反应速率和化学
平衡的变化情况,其中表示加入催化剂后变化的曲线是
( C )6. X、Y、Z三种元素的离子具有相同的电子层结构,X的离子半径大于Y离子半径.Y与Z可形成ZY2型离子化合物,这三种元素原子序数的关系是
A.xyz B.zxy C.zyx D.yxz
( D)7. 某元素的原子核外有5个电子层,最外层有3个电子,该元素及其化合物不可能具有的性质 A.该元素单质是导体 B.该元素单质在一定条件下能与盐酸反应
C.该元素的氧化物的水化物显碱性 D.该元素最高化合价呈+5价
( A )8. 下列晶体或分子①硅晶体②金刚石③CCl4④NH3⑤CO2⑥石墨
具有正四面体空间构型的是
A.只有①②③ B.只有②③ C.只有①② D.除④外都是
二、选择题(本题共50分。有10小题,每小题5分。每小题有1~2个正确答案)
( D )9. 在一定条件下,可逆反应X(气)+3Y(气)![]() 2Z(气)达到平衡时,有37.5%的Y转化为Z,有25%的X转化为Z,则起始时,充入容器中的X与Y的物质的量之比为
2Z(气)达到平衡时,有37.5%的Y转化为Z,有25%的X转化为Z,则起始时,充入容器中的X与Y的物质的量之比为
A.13 B.31 C.32 D.12
( C)10. 元素X的原子核内只有1个质子.元素Y的阳离子电子层结构和氖原子电子层结构相同,Y、Z和E在周期表里位于同一周期.X和E、Z分别能形成气态氢化物XE和X2Z,它们的水溶液是酸.Z跟Y能形成离子化合物Y2Z.与氖同周期的元素F的气态氢化物FX3,其水溶液能使酚酞试液变红.则X、Y、Z、E、F的元素符号是
A.H、Li、O、F、N B.H、K、Se、Br、P C.H、Na、S、Cl、N D.H、Mg、S、O、N
( A )11. 取20g混有二氧化锰的氯酸钾,加热至恒重.在一定温度下将残留的固体加入10g水中有7.9g固体未溶解,再加入5g水有5.3g固体残渣未溶,再加水,残渣不减少.则原混合物中可能含有的KClO3质量为
A.14.7g B.6.9g C.12.1g D.17.6g
( BD )12. 有属于短周期的A、B两种元素,A原子半径小于B原子半径,两元素可形成AB2的化合物.下列有关A、B两元素的叙述正确的是
A.A、B可能属于同一周期 B.A是B的前一周期元素
C.A只能属于金属元素 D.A可能是第二周期中的IIA族元素或IVA族元素
( BD )13. 下列分子的结构中,所有原子的最外层电子不能都满足8电子稳定结构的是
A.CO2 B.CH4 C.PCl3 D.NO2
( BD )14. 下列每组有三种物质的量的浓度相等的溶液,分别将它们取等体积充分混合后,不会产生沉淀的是
A.AgNO3、NaBr、稀HNO3 B.FeCl3、HCl、KSCN
C.CaCl2、NaHCO3、NaOH D.NaAlO2、Ba(OH)2、HCl
( B )15. 将锌片和铜片用导线连接置于同一稀硫酸溶液中,下列各叙述正确的是
A.正极附近SO42-的浓度逐渐增大 B.正负极附近SO42-的浓度基本不变
C.负极附近SO42-浓度逐渐减小 D.正极附近H+的浓度逐渐增大
( C )16. 下列各组物质的沸点按由低到高顺序排列的是
A.NH3、CH4、NaCl、Na B.H2O、H2S、MgSO4、SO2
C.CH4、H2O、NaCl、SiO2 D.HI、HBr、HCl、HF
( B )17. 在足量的下列物质中投入等量金属钠,在相同条件下放出气体最多的是
A.稀硫酸 B.氯化铵饱和溶液 C.水 D.乙二醇溶液
( C )18. 下列化学反应中,能产生Al(OH)3沉淀的是
①AlCl3溶液与过量氨水混合②NaAlO2溶液与过量盐酸混合
③NaAlO2溶液中通入过量CO2气体④明矾溶液与小苏打溶液混合
A.①② B.①④ C.①③④ D.②③
作业:( B )1. 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所
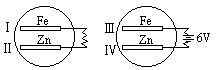 示),经过一段时间后,首先观察到溶液变红的区域是
示),经过一段时间后,首先观察到溶液变红的区域是
A.Ⅰ和Ⅲ附近 B.Ⅰ和Ⅳ附近
C.Ⅱ和Ⅲ附近 D.Ⅱ和Ⅳ附近
( B )2. 关于化学键的下列说法正确的是
A.构成分子晶体的微粒一定含有共价键 B.由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子里D.不同元素组成的多原子分子里的化学键一定是极性键
( A )3. A和B均为主族元素,A原子最外层电子排布为n层1个电子,B原子最外层电子排布为n层6个电子对由A、B所形成的化合物的判断,正确的是
A.不一定是离子化合物 B.肯定是强电解质
C.其化学式肯定是A2B D.化合物中B的化合价一定是-2
( BD )4. 对于可逆反应中反应物的转化率的叙述中错误的是
A.
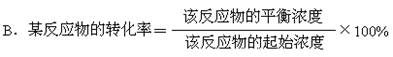 同一反应中,达到平衡时,各反应物的转化率不一定相等
同一反应中,达到平衡时,各反应物的转化率不一定相等
C.反应物的转化率大小可表示可逆反应进行的程度
D.在同一反应中,反应达到平衡时转化率一定大于未达到平衡时的转化率
( C )5. 下表给出几种氯化物的熔点和沸点
| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点(℃) | 801 | 712 | 190 | -68 |
| 沸点(℃) | 1465 | 1418 | 57 |
关于表中所列四种氯化物的下列说法:①氯化铝在加热时升华,②四氯化硅晶体属于分子晶体,③1500℃时氯化钠的分子组成可用NaCl表示,④氯化铝晶体是典型的离子晶体,其中与表中数据一致的是:
A.只有③ B.只有①和② C.只有①②③ D.全都一致
 ( D )6. 氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生.下列叙述不正确的是
( D )6. 氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生.下列叙述不正确的是
B.NH4H固体投入少量水中,有两种气体产生
C.NH4H中的H-离子半径比锂离子半径大 D.NH4H溶于水后,形成的溶液显酸性