高三化学选择题练习(二)
班级 姓名 学号 得分
一、选择题(本题共24分。有8小题,每小题3分。每小题只有一个选项符合题意)
( D )1.下列选项中说明乙醇作为燃料的优点的是( )
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种再生能源 ④燃烧时放出大量热量
A. ①②③ B. ①②④ C. ①③④ D. ②③④
( D )2.当下列物质:①大理石 ②钟乳石 ③锅垢 ④贝壳 ⑤蛋
壳,分别滴加醋酸时,会产生相同气体的
A.只有①② B.只有④⑤ C.只有①②③ D.是①②③④⑤
( D )3.下列盛放试剂的方法正确的是
A.氢氟酸或浓硝酸存放在带橡皮塞的棕色玻璃瓶中
B.汽油或煤油存放在带橡皮塞的棕色玻璃瓶中
C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中
D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中
( B )4.下列各组物理量中,都不随取水量的变化而变化的是
A.水的沸点;蒸发水所需热量
B.水的密度;水中通人足量CO2后溶液的pH
C.水的体积;电解水所消耗的电量 D.水的物质的量;水的摩尔质量
( C )5.有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式和应当具有的性质为
A. I2O4 强氧化性 B. I3O5 强还原性
C. I4O9 强氧化性 D. I4O7 强还原性
( D)6.过氧化氢俗称双氧水,它是一种液体,易分解为水和氧气,常作氧化剂、漂白剂和消毒剂,为贮存、运输、使用的方便,工业上常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3・3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是
A. MnO2 B. H2S C. 稀盐酸 D. NaHCO3
( D )7.实验室可用下图所示装置干燥、收集某气体R,并吸收多余的R,则R是
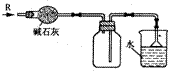
A. CH4 B. HCl C. Cl2 D. NH3
( C )8.用一定量的铁与足量的稀硫酸及足量的CuO制单质铜,有人设计了以下两种方案:
若按实验原则进行操作,则两者制得单质铜的量为
A.一样多 B.①多 C.②多 D.无法判断
二、选择题(本题共50分。有10小题,每小题5分。每小题有1~2个正确答案)
( B )9.在含有硫离子,且能使酚酞变红的无色溶液中,能大量共存的离子组是
A. Na+、Cu2+、Br-、Ba2+ B. Na+、SO32-、SO42-、K+
C. K+、MnO4-、NO3-、Na+ D. K+、Ca2+、SO32-、Cl-
( C )10.下列画有横线的物质在反应中不能完全消耗的是
A. 将含少量CO2的CO气体通入盛有足量Na2O2的密闭容器中,并不断用电火花引燃
B. 将l mol Mg置于10 L空气(标况)中,使之在高温下反应
C. 标准状况下,将11.2L H2S与22.4L O2混合点燃
D. 在强光持续照射下,向过量的Ca(ClO)2的悬浊液中通入少量CO2
( AC )11.“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用丙炔合成二甲基丙烯酸甲酯( ![]() )的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是
)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是
A.CO和CH3OH B.CO2和H2O C.H2和CO D.CH3OH和H2
( B )12.某白色固体可能由①NH4Cl、②AlCl3、③NaCl、④AgNO3、⑤KOH中的一种或几种组成,此固体投入水中得澄清溶液,该溶液可使酚酞呈红色,若向溶液中加稀硝酸到过量,有白色沉淀产生。则对原固体的判断不正确的是
A. 肯定存在① B. 至少存在②和⑤
C. 无法确定是否有③ D. 至少存在①、④、⑤
( D )13.将一定量铁粉和硫粉的混合物共热,充分反应后冷却,再加入足量稀硫酸,得到标准状况下的气体11.2L,则原混合物的组成可能是(n代表物质的量)
A. n(Fe)<n(S),总质量等于44g B. n(Fe)>n(S),总质量等于44g
C. n(Fe)=n(S),总质量大于44g D. n(Fe)>n(S),总质量小于44g
(BD )14.下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol L-1的(NH4)2SO4溶液中,c(SO42- )>c(NH4+ )>c(H+)>c(OH-)
B.0.2m01 L-1的Na2CO3溶液中,c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
C.0.1mol L-1的NH4Cl溶液与0.05mol L-l的NaOH溶液等体积混合,c(Cl- ) >c(Na+ ) >c(NH4+ ) >c(OH- ) >c(H+)
D.c(NH4+)相等的(NH4)2SO4溶液,(NH4)2CO3溶液和NH4C1溶液,
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4C1)
( D )15.由于碳碳双键(![]() )中的π―键不能自由旋转,因此
)中的π―键不能自由旋转,因此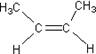 和
和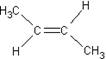 是两种不同的化合物,互为顺反异构体。则分子式为C3H4Cl2的化合物的烯烃异构体有
是两种不同的化合物,互为顺反异构体。则分子式为C3H4Cl2的化合物的烯烃异构体有
A. 4种 B. 5种 C. 6种 D. 7种
( AC )16.据某科学杂志报道,国外有一研究所发现了一种新的球形分子,它的分子式为C60Si60它的分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60、也有Si60结构。下列叙述不正确的是
A.该物质有很高的熔点、很大的硬度 B.该物质形成的晶体属分子晶体
C.该物质分子中Si60被包裹在C60里面 D.该物质的相对分子质量为2400
( C )17.氢气是工业合成氨的原料之一,有一种来源是取自石油气,例如丙烷。有人设计了以下反应途径,假如反应都进行,你认为最合理的是
![]()
![]() A.C3H8
C + H2 B.C3H8
C3H6 +
H2
A.C3H8
C + H2 B.C3H8
C3H6 +
H2
![]() C.C3H8
+ H2O CO + H2
C.C3H8
+ H2O CO + H2
![]()
![]() D.C3H8 + O2
CO2 + H2O
H2O H2 ↑ + O2↑
D.C3H8 + O2
CO2 + H2O
H2O H2 ↑ + O2↑
( C )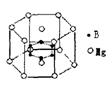 18.2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录。该化合晶体结构中的晶胞如右图所示。镁原子间形成正六棱柱,六个硼原子位于棱柱内。则该化合物的化学式可表示为
18.2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录。该化合晶体结构中的晶胞如右图所示。镁原子间形成正六棱柱,六个硼原子位于棱柱内。则该化合物的化学式可表示为
A.Mg14B6 B.Mg2B C.MgB2 D. Mg3B2
作业:
( A )1.自英国科学家狄拉克提出反粒子存在的预言,人类开始在茫茫宇宙中寻找反物质的例证。后又聚焦于反物质的合成研究。1997年人类首次合成了9个反氢原子。2002年是人类合成反物质的丰收年,合成了5万个反氢原子,也是对狄拉克诞辰100周年祭典的一份厚礼。你认为反氢原子的组成应该为
A.由1个带负电荷的质子与一个带正电荷的电子构成。
B.由1个带正电荷的质子与一个带负电荷的电子构成。
C.由1个不带电荷的中子与一个带负电荷的电子构成。
D.由1个带负电荷的质子与一个带负电荷的电子构成。
( D )2.环己基氨基酸钙 ![]() 约比蔗糖甜30倍,曾广泛用于食品中,但近年来发现它能致癌而禁止使用。下列溶剂中不能溶解该化合物是
约比蔗糖甜30倍,曾广泛用于食品中,但近年来发现它能致癌而禁止使用。下列溶剂中不能溶解该化合物是
A.H2O B.CH3OH C.NH3(液) D.CCl4
( A )3.2002年10月26日,俄罗斯特种部队在解救歌剧院人质时,使用的气体中可能有芬太奴,芬太奴的结构简式为 ![]() ,它是一种医疗上速效强力镇痛药。下列关于芬太奴的说法不正确的是
,它是一种医疗上速效强力镇痛药。下列关于芬太奴的说法不正确的是
A.分子式为:C19H23N2O B.芬太奴属于芳香族化合物
C.芬太奴显碱性 D.芬太奴既能与盐酸反应,又能与热的氢氧化钠溶液反应
( D )4.某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g)![]() H2(g)+CO2(g) △H>0
H2(g)+CO2(g) △H>0
当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
A.升温 B.加入催化剂 C.再加入n molCO和n molH2O D. 再加入2n molCO2和2n molH2