普化电化学题库
一、选择题(每小题有1个正确答案)
1. 钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A.2H++2e-=
H2 B.Fe2++2e-
= Fe
C.2H2O+O2+4e-=
4OH- D.Fe3++e-
= Fe2+
2. 下列关于铜电极的叙述, 不正确的是
A.铜锌原电池中铜是正极
B.用电解法精炼粗铜时铜作阳极
C.在镀件上电镀铜时可用金属铜作阳极
D.电解稀硫酸制H2、O2时铜作阳极
3.在外界提供相同电量的条件,Cu2+或Ag+分别按Cu2++2e-→Cu或
Ag++e-→Ag在电极上放电,其析出铜的质量为1.92g,则析出银的质量为
A.1.62g B.6.48g C.3.24g D.12.96g
4.用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是
A.稀NaOH溶液 B.HCl溶液
C.酸性MgSO4溶液 D.酸性AgNO3溶液
4.对于原电池的电极名称,下列叙述中正确的是
A、电子流入的为负极 B、比较活泼的为正极
C、电子流入的为正极 D、发生氧化-还原反应的为正极
5.埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是 ( )
A.在含铁元素较多的酸性土壤中 B.在潮湿疏松的碱性土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多,潮湿透气的中性土壤中
6.下列变化一定不可逆的是 ( )
A.溶解 B.水解 C.电解 D.电离
7.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是 ( )
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
8.用石墨电极电解某酸、碱或盐的溶液时,在相同的条件下,阴阳两极收集到的气体的体积比是2∶1,则下列结论正确的是 ( )
A.阴极一定是H2,阳极一定是O2 B.电解后溶液的pH一定变大
C.电解后溶液的pH一定不变 D.电解后溶液的浓度一定变大
9. 银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
![]()
在此电池放电时,负极上发生反应的物质是 ( )
A.Ag B.Zn(OH)2 C.Ag2O D.Zn
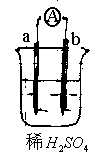 10.a的金属活动性比氢强,b为碳棒,关于下列装置的说法中不正确的是
10.a的金属活动性比氢强,b为碳棒,关于下列装置的说法中不正确的是
A.a发生氧化反应 b.发生还原反应
B.碳棒上有气体逸出,溶液的PH值增大。
C.导线上有电流,电流方向从a→b
D.反应后a极质量减小
11.铁和足量的稀![]() 反应时,加入少量
反应时,加入少量![]() 固体,下列叙述正确的是
固体,下列叙述正确的是
A.反应速率减慢,产生![]() 的量不变
的量不变
B.反应速率加快,产生![]() 的量不变
的量不变
C.反应速率不变,产生![]() 的量增加
的量增加
D.反应速率加快,产生![]() 的量减少
的量减少
12、将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,即构成甲烷燃料电池,已知通入甲烷的一极,其电极反应式为:![]() 通入氧气和另一极,其电极反应式是:
通入氧气和另一极,其电极反应式是:![]() 下列叙述正确的是( )
下列叙述正确的是( )
(A)通入甲烷的电极为正极
(B)正极发生氧化反应
(C)该电池使用一段时间后应补充氢氧化钾
(D)通入O2的电极发生的是氧化反应
1. 用电极X和Y电解硫酸铜溶液时,X极质量减小,Y极质量增加,符合以上情况的是 ( )
A X、Y都是惰性电极 B X是铜,Y是银
C X是铂,Y是银 D X是阴极,Y是阳极
2. 菜刀上沾有食盐水后,置于空气中一段时间会生锈,其原理是 ( )
| 正极 | 负极 | |
| A | Fe-2e = Fe2+ | 2H2O+O2+4e = 4OH- |
| B | 2H++2e = H2 | Fe-2e = Fe2+ |
| C | 2H2O+O2+4e = 4OH- | Fe-3e = Fe3+ |
| D | 2H2O+O2+4e = 4OH- | Fe-2e = Fe2+ |
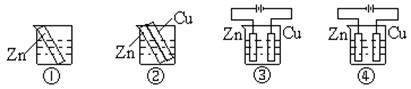
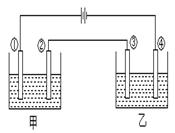
3.下列装置中的纯锌棒都浸在相同浓度的稀硫酸中,锌棒腐蚀速度从快到慢的顺序是 ( )
A ③④②① B ②③①④ C ④②①③ D ③②①④
4.已知由AgNO3的稀溶液与稍过量的KI稀溶液可制得AgI溶胶甲,由KI的稀溶液与稍过量的AgNO3溶液可制得AgI溶胶乙,则下列说法正确的是 ( )
A 甲和乙混和,仍然是AgI溶胶
B 甲中胶粒带正电荷,乙中胶粒带负电荷
C 甲与乙混和后,将得到AgI沉淀
D 甲与乙混和后既有溶胶又有沉淀
5.有人设计将两根Pt丝做电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气而构成燃料电池。该电池中反应的化学方程式为:CH4 + 2O2 + 2KOH = K2CO3 + 3H2O; 则关于此燃料电池的下列说法中错误的 ( )
A 通入甲烷的电极为电池的负极,通过氧气的电极为正极
B 在标准状况下,每消耗5.6LO2,理论上可向外提供9.6×104C的电量(一个电子所带电量为1.6×10-19C)
C 通入甲烷的电极的电极反应为:CH4 + 10OH- -8e == CO32- + 7H2O
D 放电一段时间后,溶液的pH值升高
7.为了使埋在地下的钢管不易生锈, 有人设计将钢管 ①用导线与铅相连;
②用导线与锌相连; ③用导线与碳棒相连; ④跟直流电源的负极相连;
⑤跟直流电源的正极相连。其中正确的是 ( )
A ①⑤ B ②③ C ②④ D ③④
8.白铁皮(表面镀Zn)发生析氢腐蚀,有0.2mol电子发生转移,下列说法不正确的是( )
A 有6.5g锌被腐蚀 B 2.8g铁被腐蚀
C 正极上H+被还原 D 在标准状况下有2.24L气体放出
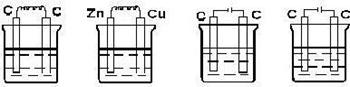 |
9.下列装置中属于原电池的是 ( ) 属于电解池的是 ( )
A B C D
稀硫酸 稀硫酸 稀硫酸 硫酸铜
10.用铂电极电解某溶液一段时间,该溶液浓度增大而pH减小,该溶液是( )
A NaOH B CuCl2 C H2SO4 D CuSO4
11.用惰性电极分别电解下列各物质水溶液一段时间后,向剩余电解质溶液中加入适量的水,能使溶液恢复到电解前浓度的 ( )
A AgNO3 B Na2SO4 C CuCl2 D H2SO4
12.以石墨电极电解NaCl、NaBr、NaI的混合溶液,初始阴阳两极上产物各是( )
A H2 和Cl2 B H2和Br2 C H2和I2 D Na和I2
13.用U型管电解滴有甲基橙指示剂的KNO3溶液,两极发生的现象是 ( )
A 阴阳极析出的气体体积比为1∶2 B 阴阳极析出的气体体积比为2∶1
C 通电一段时间后,阴极区甲基橙显黄色,阳极区甲基橙显橙色或红色
D 通电一段时间后,阴极区甲基橙显橙色或红色,阳极区甲基橙显黄色
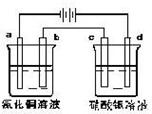 14.如右图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成的物质的量的比例关系是( )
14.如右图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成的物质的量的比例关系是( )
A 1∶1∶1∶1 B 2∶2∶1∶1
C 2∶2∶4∶1 D 1∶2∶2∶4
15.在甲电解池中盛有足量的硫酸钠溶液,乙电解池中盛有足量的硫酸铜溶液,
通以相同的电量分别进行电解(电极材料均为石墨),当甲池中收集到11.2L
氢气(标准状况)时,乙池析出的铜质量为 ( )
A 128g B 64g C 32g D 16g
16.将电极M和N插入电解质溶液X中并通以直流电,发现M的质量减小而N的质量增重。下列情况中有可能与上述现象相符的 ( )
A X是硫酸溶液 B M是阴极、N是阳极
C M是石墨电极,N是铜电极 D M是铜电极,N是石墨电极
17.在盛饱和碳酸钠溶液的烧杯中,插入惰性电极,恒温下通电一定时间后( )
A 溶液的pH值将增大
B 钠离子数和碳酸根离子数的比值将变小
 C 溶液的浓度逐渐增大,有一定量晶体析出
C 溶液的浓度逐渐增大,有一定量晶体析出
|
|
D 溶液的浓度不变,有晶体析出
20.用铂电极电解下表中各组物质的水溶液(如右
图),电解一段时间后,甲、乙两池中溶液PH均
减小,而在①和④两极,电极产物的物质的量之比为1:2的是 ( )
| A | B | C | D | |
| 甲 | KOH | H2SO4 | Na2SO4 | CuSO4 |
| 乙 | CuSO4 | AgNO3 | HCl | HNO3 |
.把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上 有大量气泡产生,则四种金属的活动性顺序由强到弱为( )
A.a>b>c>d B.a>c>d>b
C.c>a>b>d D.b>d>c>a
8、再250C时,将两个铜电极插入一定量的Na2SO4饱和溶液中,进行电解,通电一段时间后,阴极逸出amol气体,同时有WgNa2SO4.10H2O晶体析出,若温度不变,剩余溶液里溶质质量分数是
A:![]() B:
B:![]() C:
C:![]() D:
D:![]()
C.在干燥致密不透气的土壤中 D.在含碳粒较多,潮湿透气的中性土壤中
2.胶体微粒能做布朗运动的原因是 ( )
①水分子对胶粒的撞击②胶体微粒有吸附能力③胶粒带电④胶体微粒质量较小,所受重力小
A.①② B.①③ C.①④ D.②④
.Fe(OH)3胶体溶液中,[Fe(OH)3]n粒子带正电,为了使带正电粒子聚沉,下列物质中用量最少最有效的电解质是 ( )
A.Na3PO4 B.FeCl3 C.BaCl2 D.KCl
9.电解含下列离子的水溶液,若阴极析出相等质量的物质,则消耗的电量最多的是( ) A.Ag+ B.Cu2+ C.Na+ D.K+
11.下列过程需通电后才能进行的是 ( )
A.电离 B.电解 C.电化腐蚀 D.熔融
14.下列事实与胶体知识有关的是 ( )
①用盐卤点豆腐②水泥硬化③电泳电镀④明矾净水⑤在油脂的皂化液中加入食盐析出肥皂
A.②③④ B.①③⑤ C.①②⑤ D.全部都是
15.在电解水时,常加入一些稀硫酸,其目的是 ( )
A.使溶液酸性增强 B.
22.将某溶液逐滴加入Fe(OH)3溶胶内,开始时产生沉淀,继续滴加时沉淀又溶解,该溶液
是 ( )
A.2 mol/L H2S04 B.2 mol/L NaOH溶液
C.2 mol/L MgS04溶液 D.硅酸胶体
23.电泳实验发现,硫化砷胶粒间阳极移动,下列不能使硫化砷胶体凝聚的措施是( )
A.加入Fe2(SO4)3溶液 B.加入硅酸胶体
C.加热 D.加入Fe(OH)3胶体
24.下列液体中,不会出现丁达尔现象的分散系是:①鸡蛋清溶液 ②水 ③淀粉溶液 ④蔗糖溶液 ⑤Fe(OH)3溶液 ⑥肥皂水 ( )
A.④⑤ B.③④ C.②④⑥ D.④
17.下列关于胶体的叙述,不正确的是 ( )
A.有色玻璃是固溶胶 B.雾、云、烟都是气溶胶
C.用滤纸能把胶体中的分散质与分散剂分离 D.胶粒大小直径在1nm~100nm之间
C.加快电解的速度 D.使溶液的氧化性增强
9、在A、B、C三个烧杯中分别盛有同体积,同摩尔浓度的NaNO3、HCl和KCl溶液,用石墨作电极,将它们串联进行电解,一段时间后,电解液pH值增大的的烧杯是 。pH值不变的烧杯是 。A、C两杯阳极电极反应式分别是 , 。如果把A、B、C杯中电极都换成铁和石墨,并用导线连接,(不与电源相连。)则各杯中铁片受腐蚀情况。(写明腐蚀类型、快慢。)及原因是 。
二、填空题
23.电解饱和食盐水时,电解槽的阳极是由 制成,阳极反应式 ,阴极是由 制成,阴极反应式 ,电解的离子方程
式 电解的化学方程式 。若在两极分别滴入酚酞试液,现象是 。设置隔膜的作用是 。
24.下图各容器中盛海水,铁会在其中发生变化。按铁极腐蚀的速度由快至慢的顺序为
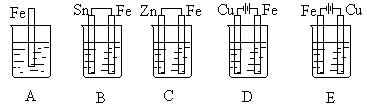
26.下图表示采用惰性电极电解相同物质量浓度,相同体积的KOH、CuSO4、NaCl溶液的情况。如果不考虑电解过程中溶液浓度变化对电极反应的影响,在相同的时间里,放出气体最多的是 溶液,放出气体最少的是 溶液。
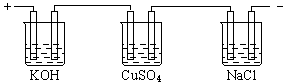
27. 按照下图接通线路,反应一段时间后,回答下列问题(假设所提供的电能可以保证电解反应的顺利进行):
(1)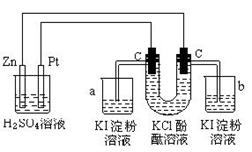 U型管内发生什么现象?
U型管内发生什么现象?
(2)写出有关反应的化学方程式:
(3)在a、b烧杯中发生什么现象:
(4)如果小烧杯中有0.508g碘析出,问大烧杯中,负极减轻多少?
28. 图中p、q为电源两极,A为2价金属X制成,B、C、D为铂电极,接通电源,金属X沉积于B,同时C、D产生气泡。试回答:
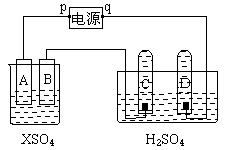
(1)p为 极
(2)A极发生了 反应;C为 极,试管里收集到 ;
D为 极,试管里收集到 ;
(3)C极的电极反应式
(4)当电路中通过0.004mol电子时,B电极上沉积金属X为0.128g,则此金属的原子量为
29. 对于下列装置中的反应,写出相应的电极反应式:
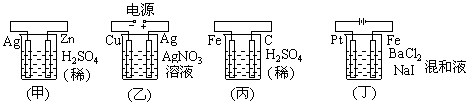
(1)甲装置中,Zn极: ; Ag极
(2)乙装置中,Cu极: ; Ag极
(3)丙装置中,Fe极: ; C极
二、填空题
1、原电池是把 能(氧化还原反应)转化为 能(电子在导线中定向移动)的装置
2、Zn-Cu原电池的正负极与氧化还原反应
负极( )——
电子——发生
反应——现象
正极( )—— 电子(电子流入)——发生 反应——现象 3、钢铁 电化学腐蚀中①析氢腐蚀(在酸性较强的电解质环境下)
负极 ,正极
②吸氧腐蚀(中性或弱酸性电解质溶液如![]() 环境下)
环境下)
负极 正极
 总反应式
总反应式
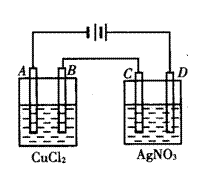
4、右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极方程式:
A________________________________
B________________________________
C________________________________
D________________________________
(2)在A、B、C、D各电极上析出生成物的物质的量比________________________________________________。
三、计算题
31. 将200mL2mol/LAgNO3溶液和200mL1mol/LCu(NO3)2溶液混和,用铜片作电极进行电解,阴极上共有6.4g铜析出时停止电解,若溶液的体积变化忽略不计,则此时溶液中Cu2+的浓度为多少?
32.以石墨为电极,电解500mL3mol/LCuSO4溶液,当收集到5.6L(标况)气体时,再倒接电源的正负极,通电一段时间后,又收集到5.6L(标况)气体,求电解后所得溶液中各物质的物质的量的浓度(设整个过程中溶液的体积不变)和整个通电过程中电路流过的电子的物质的量。
33. 有一种硝酸盐晶体,分子式为M(NO3)z·nH2O,经测定其摩尔质量为242g/mol,取1.21g此晶体溶于水,配制成100mL溶液,将其置于电解池中用惰性材料作电极进行电解,当有0.01mol电子转移时,溶液中全部金属离子即在电极上析出,经测定,阴极增重0.32g
(1)问1.21g此盐晶体物质的量是多少? Z值为多少?
(2)求M的原子量和n值
(3)如电解过程中溶液体积不变,计算电解结束后溶液的pH值