高三毕业班期末化学考试
化学试卷
第Ⅰ卷(选择题共72分)
可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na -23 S-32 Fe-56
一、选择题(本题包括8小题,每小题4分,共32分.每小题只有一个正确选项符合题意.)
1.人的血液总是维持在PH=7.37~7.45范围内,这是由于
A.人体中有大量水分(占体重70%)
B.血液中氯化钠保持一定浓度
C.排出的二氧化碳溶解在血液中
D.血液中HCO3-和H2CO3的浓度稳定在一定范围内
2.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是
A.该粒子不显电性 B.该粒子质量数为4
C.在周期表中与氢元素占同一位置 D.该粒子质量比氢原子大
3.苹果汁是人们喜爱的饮料,由于其中含有亚铁离子,在榨取后不久往往会变为棕黄色,生产上常在其中加入维生素C以防止其变色,这是利用了维生素C的
A.氧化性 B.还原性 C.酸性 D.碱性
4.将SO2通入BaCl2溶液至饱和未见沉淀,继续通入另一气体仍无沉淀,通入的气体可能是
A.CO2 B.NH3 C.NO2 D.H2S
5.航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一。下列有关C2O3的说法正确的是
A.C2O3和CO2)是同素异形体 B.C2O3和CO燃烧产物都是CO2
C.C2O3和CO都是酸性氧化物 D.C2O3和CO2都是碳酸的酸酐
6.室温下,某溶液中水电离出来的H+和OH-浓度的乘积为1×10-24,该溶液中一定不能大量存在的离子是
A.S2O32- B.NH4+ C.NO3- D.HCO3-
![]()
|
|
![]() A.氢气在氧气中燃烧
A.氢气在氧气中燃烧
|
|
|
|
D.金属钾与水反应
8.过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,他可由冰醋酸与过氧化氢在一定条件下制得;他可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒)、细菌、真菌及芽孢,有关过氧乙酸的叙述正确的是
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸可与苯酚混合使用
C.由过氧化氢与醋酸制取过氧乙酸的反应属于氧化还原反应
D.浓过氧乙酸中加入少许紫色石蕊试液,振荡后试液一定呈红色
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。)
9.维生素E在国外美称之“生命奇迹丸”,是一种脂溶性维生素,对抗衰老等有特殊作用,经研究发现维生素E有α、β、γ、δ四种类型,其结构简式如下:
上述互为同分异构体的是
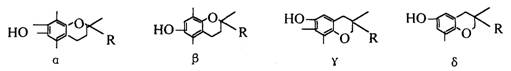
其中R为-CH2CH2CH2[CH(CH3)CH2CH2]2CH(CH3)2即:

A.α β B.β γ C.γδ D.α δ
10.某温度下,在一容积可变的容器中,反应2A(s)十B(g)![]() 2C(g);△H>0,达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol,当采取下列措施能使平衡向正反应方向移动的是
2C(g);△H>0,达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol,当采取下列措施能使平衡向正反应方向移动的是
A.升高温度 B.加入催化效果更好的催化剂
C.A、B、C均增加1mol D.A、B、C的量均减半
11.下列离子反应方程式正确的是
A.氯气与水反应:Cl2 +H2O =Cl-+2H++ClO-
B.氨气通入醋酸溶液中NH3+H+=NH4+
C.氯化铁溶液显弱酸性:Fe3++3H2O![]() Fe(OH)3
+3H+
Fe(OH)3
+3H+
D.碳酸氢钠溶液中加入过量石灰水HCO3-+OH-=CO32-+H2O
12.X和Y两元素的阳离子具有相同的电子层结构。X元素的阳离子半径大于Y元素的阳离子半径。Z和Y两元素的核外电子层数相同,Z元素的原子半径小于Y元素的原子半径。则X、Y、Z三种元素原子序数的关系是
A.X>Y>Z B.Y>X> Z C.Z>X>Y D.Z>Y>X
13.以NA表示阿伏加德罗常数,下列说法正确的是
A.0.1molH3O+中含有NA个电子 B.标准状况下,11.2L臭氧中含有NA个氧原子![]()
C.2g重氧水(H218O)、含有NA个中子 D.84gNaHC03晶体中含有NA个CO32-
14.经测定某溶液中只含NH4+、C1- 、H+、OH-四种离子,下列说法错误的是
A.溶液中四种粒子之间不可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-)
B.若溶液中粒子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+)则溶液中溶质一定为:NH4Cl和NH3·H20
C.若溶液中粒子间满足:c(C1-)>c(NH4+)>c(H+)>c(OH-)溶液中溶质一定只有NH4Cl
D.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
15.已知热化学反应方程式:2H2(气)+O2(气)=2H2O(液);ΔH=-571.6KJ,
2H2O(气)=2H2(气)+O2(气);ΔH=+483.6KJ。则下列说法正确的是
A.每摩尔水气化时所吸收的热量是88.0KJ B.水由液态变气态是一个吸热反应
C.1g氢气燃烧生成气态水可放出120.9KJ热量
D.若将1mol液态水加热分解为氢气和氧气,至少要吸收285.8KJ热量
16.下列说法正确的是
A.强碱与弱酸所生成的盐,其水溶液一定呈碱性
B.离子晶体中可能含有共价键,分子晶体中不一定含有共价键
C.一切四面体空间构型的分子内键角均为109°28′
D.金属氧化物一定是碱性氧化物
17.已知95%(溶质的质量分数)酒精溶液的物质的量浓度为16.52mol/L,试判断47.5%酒精溶液的物质的量浓度为
A.大于8.26mol/L B.等于8.26mol/L C.小于8.26mol/L D.无法判断
18.7.68 g Cu与足量浓硝酸反应,铜全部作用,如果NO3-减少2×10-3mol,则溶液中H+同时减少
A.4.8×10-3mol B.4.4×10-3mol C.3.2×10-3mol D.2.2×10-3mol
第Ⅱ卷(非选择题共78分)
三、(本题包括19、20两小题,共23分)
|
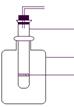 19.(7分)某同学用实验室常见的酸、碱、盐和金属为反应物,并利用
19.(7分)某同学用实验室常见的酸、碱、盐和金属为反应物,并利用
|
|
该装置可制取下列哪些气体 (填序号);若将铜丝
网隔板改为铁丝网隔板,则该装置可用于制取下列何种气体 (填序号),写出反应的离子方程式 。
①O2 ②H2 ③Cl2 ④CO2 ⑤HCl ⑥NO ⑦H2S
20.(16分)在实验室里制取某些有毒气体时,为了尽量防止毒气逸散造成空气污染,有人设计了如下图所示的装置[Ⅰ]。并设想用[Ⅱ]或[Ⅲ]两种简易装置代替[Ⅰ]的b~c部分,以求达到同样的目的。
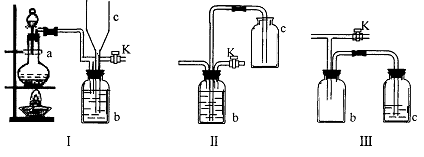
试回答:
(1)若用[Ⅰ]取氯气,b瓶加入的液体一般为_____________。在选取试剂正确且适量的前题下,反应开始后,当关闭活塞K时如若发现c中液面不明显上升,你分析可能的原因是__________________________检查的简单方法是__________________________
(2)装置[1]中b能防止多余气体逸散的原因是:____________________________
(3)欲用[Ⅱ]或[Ⅲ]代替[Ⅰ]中的b~c部分(选用液体相同),是否可行?说明理由。
[Ⅱ]是否可行(填“是”或“否”) ______________ 理由是___________________________
[Ⅲ]是否可行(填“是”或“否”) _____________理由是______________
四、(本题包括21.22两小题,共17分)
21.(5分)X、Y、Z是ⅠA~ⅦA族的三种非金属元素,它们在周期表中的位置如右下图所示,试回答:
| X | ||
| Y | ||
| Z |
(1)X元素单质的化学式是__________,
(2)Y元素的原子结构示意图是__________,
Y与Na所形成的化合物的电子式是__________,
(3)Z元素的名称是_______,从元素原子得失电子的
角度看,Z元素具有______性。(填金属性、非金属性或两性)
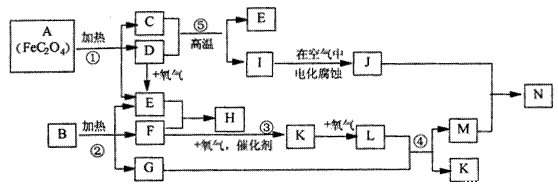 |
22.(12分)已知:D.E.F.K.L为气体,E能使澄清石灰水变浑浊,1是金属,1molA在反应①中转移的电子的物质的量为1mol,B.H是常见的化肥,它们有如下图所示转化关系(部分反应中生成的水已略去):试回答下列:
(1)写出化学方程式;C__________D _____________H ____________N ______________ (2)写出反应方程式
②___________________________ ③ ___________________________
④ ___________________________
(3)写出离子反应方程式 I+M—N+K:____________________________
五、(本题包括23、24两小题,共20分)
23.(10分)分子量为84的烯烃,主链上有4个碳原子,可能有_____种结构式,分别写出它们的结构简式并命名。_________________________________________________________________
24.(10分)有机物A-H能发生下图所示一系列变化
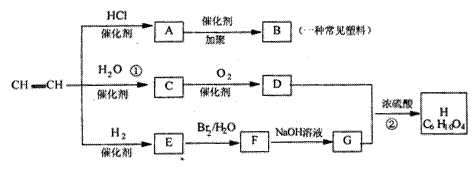

试回答:
(1)写出化学式:A ______________ B______________E______________ F ______________
(2)写出化学方程式:
①_________________________________________________
②_________________________________________________
(3)C、G、H中与等物质的量乙炔燃烧消耗氧气相同的化合物是___________(填字母)
六、(本题包括25、26两小题,共18分)
25.(9分)现有100mL 1 mol·L-1的碳酸钠溶液和100mL 1.25 mol·L-1的盐酸溶液。
(1)若将碳酸钠溶液逐滴滴加到盐酸中,求收集到的CO2在标准状况下的体积。
(2)若将上述盐酸逐滴加入到碳酸钠溶液中,反应完全后,CO2在溶液中的浓度为
0.04 mol·L-1,假定溶液体积不变,求收集到的CO2在标准状况下的体积。
26.(9分)在100mLNaOH溶液中加入NH4NO3 和(NH4)2SO4 的固体混合物,加热使之充分
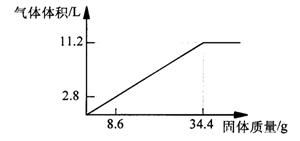 反应,下图表示加入固体的的质量与产生气体的体积(标准状况)的关系。试计算:
反应,下图表示加入固体的的质量与产生气体的体积(标准状况)的关系。试计算:
(1)NaOH溶液的物质的量浓度是
___________ mol·L-1
(2)当NaOH溶液为140mL,固体为
51.6g时,充分反应产生的气体为
___________ L(标准状况)
(3)当NaOH溶液为180mL,固体仍为
51.6g时,充分反应产生的气体为___________L(标准状况)。
高三毕业班期末考试答题卷
化 学 试 卷
高三( )班 姓名 学号 评分
第Ⅰ卷(选择题 共72分) 答题卡
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 答案 |
第Ⅱ卷(非选择题 共78分)
三、(本题包括19、20两小题,共23分)
19.(7分) (填序号); (填序号), 。
20.(16分)(1)_____________。原因是_______________________,______________________
__________________________________________________________________________。
(2)原因是:_____________________________________________________________________。
(3)[Ⅱ]_____,理由是______________________________________________________________。
[Ⅲ]_____,理由是______________________________________________________________。
四、(本题包括(21.22两小题,共17分)
21.(5分)(1)__________,(2)__________,__________,(3)_______,有_________性。
22.(12分) (1)C__________D _____________H ____________N ______________
(2)②___________________________ ③ ___________________________
④ ___________________________
(3)____________________________
五、(本题包括23、24两小题,共20分)
23.(10分) _________, ___________________________________________________________
___________________________________________________________________________
___________________________________________________________________________
___________________________________________________________________________
___________________________________________________________________________
24.(10分)(1)A __________________________ B___________________________
E___________________________ F___________________________
(2)①_________________________________________________________________________。
②_________________________________________________________________________。
(3)___________(填字母)
六、(本题包括25、26两小题,共18分)
25.(9分)
26.(9分)(1)___________ mol·L-1 (2) ___________ L(标准状况) (3)___________L(标准状况)。
高三毕业班期末考试答案卷
第Ⅰ卷(选择题 共72分) 答题卡
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | D | C | B | A | B | D | B | A | B | AC |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 答案 | C | D | AC | AC | CD | B | A | B |
第Ⅱ卷(非选择题 共78分)
三、19.(共7分) ②④⑦,②,2Al+2OH-+2H2O=2AlO2-+3H2↑(或Si+2OH-+H2O=SiO32-+2H2↑)
20.(16分,每空均2分) (1) (6分)饱和食盐水;装置漏气;用湿润的碘化钾淀粉试纸先靠近各边接口处检验,漏气处试纸变蓝 (涂肥皂水等合理方法均可)
(2) (2分)关闭活塞后,若a中仍有气体发生,气体压强增大。将b中液体压入c中,整个装置成为储气装置,不会有气体逸出。 (2) (4分)是,原理与装置I同
(4分)否,c瓶因密闭,体积不能改变,压强增大时有危险
四、21.(每空1分,共5分)
(1)F2(2)![]() ,
,![]() (3)砷,两性
(3)砷,两性
22.(每空2分,共12分) (1)FeO;CO;CO(NH2)2;Fe(NO3)2,或Fe(NO3)2
(2)NH4HCO3 NH3↑+H2O+CO2↑或(NH4)2CO3 2NH3↑+H2O +CO2↑
(3)Fe+4H++NO3-=Fe3++NO↑+2H2O或3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O
五、23.(每空2分,共10分)4;![]() 2,2-二甲基-1-丁烯,
2,2-二甲基-1-丁烯,![]() 2,2-二甲基-2-丁烯,
2,2-二甲基-2-丁烯,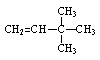 3,3-二甲基-1-丁烯,
3,3-二甲基-1-丁烯,![]() 2-乙基-1-丁烯。
2-乙基-1-丁烯。
24.(10分) (1)CH2=CHCl
, ![]() , CH2=CH2
, CH2Br-CH2Br
(每格1分)
, CH2=CH2
, CH2Br-CH2Br
(每格1分)
(2)CH=CH+H2O
![]() CH3CHO
CH3CHO ![]() (2分)
(2分)
2CH3COOH+HOCH2CH2OH![]() CH3COOCH2CH2OOCCH3+2H2O
(2分) (3)C.G (2分)
CH3COOCH2CH2OOCCH3+2H2O
(2分) (3)C.G (2分)
六、 25.(1)1.4 L )(2)0.38 L
26.(每空3分,共9分) (1)5 mol·L-1 (2)15.68 L (3) 16.8 L