专题训练二:基本理论――化学反应速率、化学平衡
(每题只有一个最佳选项)
1、在2A+B=3C+4D反应中,表示该反应速率最快的数据是
A、υA = 0.5mol/(L・s) B、υB = 0.3mol/(L・s)
C、υC = 0.8mol/(L・s) D、υD = 1.0mol/(L・s)
![]() 2、反应N2(g) + 3H2(g) 2NH3(g),在密闭容器内进行,分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为υ(N2)、υ(H2)、υ(NH3),则三者之间的关系正确的是
2、反应N2(g) + 3H2(g) 2NH3(g),在密闭容器内进行,分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为υ(N2)、υ(H2)、υ(NH3),则三者之间的关系正确的是
A、υ(N2) = υ(NH3) B、3υ(H2) =2υ(NH3)
C、3υ(NH3) = 2υ(H2) D、υ(N2) = 3υ(H2)
![]() 3、下列说法中,可以证明反应N2 + 3H2 2NH3已达到平衡状态的是
3、下列说法中,可以证明反应N2 + 3H2 2NH3已达到平衡状态的是
![]() A、1个N N键断裂的同时,有3个H―H键形成
A、1个N N键断裂的同时,有3个H―H键形成
![]() B、1个N N键断裂的同时,有3个H―H键断裂
B、1个N N键断裂的同时,有3个H―H键断裂
![]() C、1个N N键断裂的同时,有6个N―H键形成
C、1个N N键断裂的同时,有6个N―H键形成
![]() D、1个N N键断裂的同时,有2个N―H键断裂
D、1个N N键断裂的同时,有2个N―H键断裂
4、在5L密闭的容器中充入2molA气体和1 molB气体,在一定条件下发生反应:
![]() 2A(g)+B(g) 2C(g),达到平衡时,在相同温度下测得容器内混合气体的压强是反应前的5/6,则达到平衡时A的转化率为
2A(g)+B(g) 2C(g),达到平衡时,在相同温度下测得容器内混合气体的压强是反应前的5/6,则达到平衡时A的转化率为
A、67% B、50% C、25% D、5%
![]() 5、在一密闭的容器中,反应aA(g) bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则
5、在一密闭的容器中,反应aA(g) bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则
A、平衡向逆反应方向移动 B、物质A的转化率减小了
C、物质B的质量分数增加了 D、a>b
6、在一定体积的密闭容器中加入3L气体R和5L气体Q,在一定条件下发生反应:
![]() 2R(g)+5Q(g) 4X(g)+nY(g),反应达到平衡时,若容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是
2R(g)+5Q(g) 4X(g)+nY(g),反应达到平衡时,若容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是
A、2 B、3 C、4 D、5
![]() 7、在密闭容器中进行反应:X2(g)+ Y2(g) 2R(g),已知X2、Y2、R的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
7、在密闭容器中进行反应:X2(g)+ Y2(g) 2R(g),已知X2、Y2、R的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A、X2为0 mol/L B、Y2为0.35mol/L C、X2为0.2mol/L D、R为0.4mol/L
![]() 8、对于可逆反应:2A+3B 2C △H= -Q (Q>0),下列条件的改变一定可以加快正反应速率的是
8、对于可逆反应:2A+3B 2C △H= -Q (Q>0),下列条件的改变一定可以加快正反应速率的是
A、增大体系压强 B、升高温度 C、增加A的量 D、加入催化剂
![]() 9、乙酸蒸气能形成二聚分子:2CH3COOH(g) (CH3COOH)2(g)
△H = -Q (Q>0),现欲测定乙酸的相对分子质量,应采用的条件为
9、乙酸蒸气能形成二聚分子:2CH3COOH(g) (CH3COOH)2(g)
△H = -Q (Q>0),现欲测定乙酸的相对分子质量,应采用的条件为
A、高温低压 B、低温高压 C、低温低压 D、高温高压
![]()
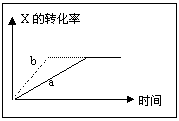 10、题图中a曲线表示一定条件下可逆反应:X(g)+Y(g) 2R(g)+ W(s) △H= -Q (Q>0)的反应过程。若要使a曲线变成b曲线,可采取是下列措施中的:①升温;②降温;③增大体系压强;④减小体系压强;⑤加入催化剂;
⑥分离出R
10、题图中a曲线表示一定条件下可逆反应:X(g)+Y(g) 2R(g)+ W(s) △H= -Q (Q>0)的反应过程。若要使a曲线变成b曲线,可采取是下列措施中的:①升温;②降温;③增大体系压强;④减小体系压强;⑤加入催化剂;
⑥分离出R
A、③⑤ B、①③⑤⑥
C、②④⑤ D、①④⑥
11、一定条件下,在2L的密闭容器中充入2molSO2和一定量O2,发生反应:
![]() 2 SO2 + O2 2 SO3,进行到4 min时测得n(SO2) = 0.4mol,则反应进行到2min时n(SO2)可能为
2 SO2 + O2 2 SO3,进行到4 min时测得n(SO2) = 0.4mol,则反应进行到2min时n(SO2)可能为
A、1.6mol B、1.2mol C、大于1.6mol D、小于1.2mol
12、在相同的条件下(T=500K),有相同体积的甲、乙两容器。甲容器中充入1g SO2和1g O2,乙容器中充入2g SO2和2g O2,,下列的叙述错误的是
A、化学反应速率:乙>甲 B、平衡后氧气的浓度:乙>甲
C、SO2的转化率:乙>甲 D、平衡后SO2的体积分数:乙>甲
![]() 13、在密闭容器中,可逆反应:nA(g) + mB(g) pC(g) △H=Q (Q>0),且m + n > p,处于平衡状态后,则下列说法:①升温时[B] / [C]的值减小 ;②降压时体系内混合气体的平均相对分子质量减小;③加入B,A的转化率提高;④加入催化剂,气体的总物质的量不变;⑤充入C,则A、B的物质的量增大。正确的是
13、在密闭容器中,可逆反应:nA(g) + mB(g) pC(g) △H=Q (Q>0),且m + n > p,处于平衡状态后,则下列说法:①升温时[B] / [C]的值减小 ;②降压时体系内混合气体的平均相对分子质量减小;③加入B,A的转化率提高;④加入催化剂,气体的总物质的量不变;⑤充入C,则A、B的物质的量增大。正确的是
A、③④ B、①②⑤ C、②③⑤ D、全部
![]() 14、已建立化学平衡的可逆反应A+B C,改变条件,使化学平衡向正反应方向移动,有关的叙述正确的是
14、已建立化学平衡的可逆反应A+B C,改变条件,使化学平衡向正反应方向移动,有关的叙述正确的是
A、生成物的百分含量一定增大 B、生成物的产量增加
C、反应物的转化率都增大 D、反应物的百分含量降低
15、在423K、体积相同的三个密闭容器A、B、C中,分别加入a mol碘化氢,b mol碘化氢,c mol 1:1的氢气与碘蒸气的混合气体,若a > b = c,分别达到平衡时,下列说法正确的是
A、从反应开始至达到平衡所需的时间:tA > tB = tC
B、平衡时碘单质的浓度:[I2]A = [I2]B = [I2]C
C、平衡时混合气体中碘蒸气的百分含量:A% = B% = C%
D、平衡时混合气体中碘化氢气体的百分含量:A% > B% > C%
![]() 16、在容积不变的密闭容器中,在一定条件下发生反应:2A B(g) +C(s),且达到平衡。当升高温度时其容器内气体的密度增大,则
16、在容积不变的密闭容器中,在一定条件下发生反应:2A B(g) +C(s),且达到平衡。当升高温度时其容器内气体的密度增大,则
A、若正反应是吸热反应,则A一定为固体
B、若正反应是放热反应,则A一定为气体
C、在平衡体系中加入少量C,该反应向逆反应方向移动
D、压强对该平衡的移动无影响
![]() 17、CO2和H2的混合气体加热到850℃时,可建立下列平衡:CO2+H2 CO+H2O。在一定温度下,反应平衡时有90%的H2变成水,且c(CO2)・c(H2)=c(CO)・c(H2O),则原混合气体中CO2和H2分子数之比是
17、CO2和H2的混合气体加热到850℃时,可建立下列平衡:CO2+H2 CO+H2O。在一定温度下,反应平衡时有90%的H2变成水,且c(CO2)・c(H2)=c(CO)・c(H2O),则原混合气体中CO2和H2分子数之比是
A、1:1 B、5:1 C、9:1 D、1:10
18、在密闭容器中通入A、B两种气体,在一定条件下反应:
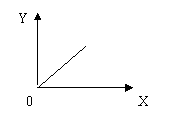
![]() 2A(g) + B(g) 2C(g) △H= -Q (Q > 0 ),达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线所示的变化的是
2A(g) + B(g) 2C(g) △H= -Q (Q > 0 ),达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线所示的变化的是
A、X―温度,Y―生成物C的物质的量
B、X―压强,Y―混合气体的平均相对分子质量
C、X―再加入反应物A,Y―生成物C的体积分数
D、X―再加入反应物A,Y―反应物A的转化率
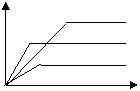
![]() 19、可逆反应:mA(g) + nB(g) pC(g) + qD(g) △H= Q,在温度T1、T2,压强P1、P2下,产物D的物质的量n (D)与反应时间t的关系如图所示,下列各项中不正确的是
19、可逆反应:mA(g) + nB(g) pC(g) + qD(g) △H= Q,在温度T1、T2,压强P1、P2下,产物D的物质的量n (D)与反应时间t的关系如图所示,下列各项中不正确的是

 A、T1 < T2
A、T1 < T2
B、P1 < P2
C、Q < 0
D、m + n < p + q
20、化学反应速率υ和反应物浓度的关系是用实验方法测定的,H2+Cl2=2HCl的反应速率υ可表示为:υ=K[H2]m[Cl2]n,式中K为常数,m、n值可用表中数据确定之。
| [H2] / (mol・L-1) | [Cl2] / (mol・L-1) | υ/ (mol・L-1・s-1) |
| 1.0 | 1.0 | 1.0K |
| 2.0 | 1.0 | 2.0K |
| 2.0 | 4.0 | 4.0K |
由此可推断m、n值正确的是
A、m=1 n=1 B、m=1/2 n=1/2
C、m=1/2 n=1 D、m=1 n=1/2
![]() **21、1mol气体A和n mol气体B在一定条件下,在一密闭的容器中按下式反应生成气体C,
A(g)+nB(g) mC(g) 。反应达到平衡时,测得A的转化率为50%,且反应前后容器内气体压强比为4:3。则n和m的数值可能是
**21、1mol气体A和n mol气体B在一定条件下,在一密闭的容器中按下式反应生成气体C,
A(g)+nB(g) mC(g) 。反应达到平衡时,测得A的转化率为50%,且反应前后容器内气体压强比为4:3。则n和m的数值可能是
A、n=2 m=2 B、n=3 m=3
C、n=1 m=1 D、n=2 m=3
**22、在一定条件下,合成氨反应达到平衡后,混合气体中NH3的体积占25%。若反应前后条件保持不变,则反应后缩小的气体体积与原反应混合物体积的比值是
A、1/5 B、1/4 C、1/3 D、1/2
专题训练二:基本理论――化学反应速率、化学平衡
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| B | C | A | B | C | A | B | B | A | A | D | D | D |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | B | C | B | C | D | C | A |
专题训练二:基本理论――化学反应速率、化学平衡
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| B | C | A | B | C | A | B | B | A | A | D | D | D |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | B | C | B | C | D | C | A |
专题训练二:基本理论――化学反应速率、化学平衡
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| B | C | A | B | C | A | B | B | A | A | D | D | D |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | B | C | B | C | D | C | A |
专题训练二:基本理论――化学反应速率、化学平衡
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| B | C | A | B | C | A | B | B | A | A | D | D | D |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | B | C | B | C | D | C | A |
专题训练二:基本理论――化学反应速率、化学平衡
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| B | C | A | B | C | A | B | B | A | A | D | D | D |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | B | C | B | C | D | C | A |